Clear Sky Science · ar
البوتاسيوم خارج الخلية يغير أشكال المسام لقنوات الأنيونات من عائلة Cys-loop
كيف تستمع الخلايا إلى البوتاسيوم في الخارج
كل فكرة وحركة ونبضة قلب في أجسامنا تعتمد على ذرات مشحونة صغيرة، أو أيونات، تتحرك عبر أغشية الخلايا. البوتاسيوم هو واحد من أهم هذه الأيونات، وتُحافظ مستوياته خارج الخلايا العصبية ضمن نطاق ضيق للغاية. تكشف هذه الدراسة عن طريقة غير متوقعة تستطيع بها خلايا الدماغ استشعار تغيّر البوتاسيوم خارج الخلية مباشرةً وترجمته إلى تغيرات في تدفُّق الكلوريد، أيون أساسي آخر. تكشف الدراسة عن آلية استشعار مخفية في عائلة من مستقبلات الأعصاب وتقترح طرقًا جديدة قد يستخدمها الدماغ لمراقبة بيئته الكيميائية والاستجابة لها.
نوع جديد من مستقبلات البوتاسيوم
حتى الآن، كانت معظم الأجهزة المعروفة لاستشعار البوتاسيوم في الحيوانات قنوات ومضخات تستخدم البوتاسيوم كوقود أو كحمولة، لا كإشارة بحد ذاتها. ركز الباحثون على بروتين قليل الدراسة في ذبابة الفاكهة Drosophila، يُدعى DmAlka، وينتمي إلى عائلة مستقبلات Cys-loop. عادة ما تكون أعضاء هذه العائلة قنوات تفتح عند ارتباط الناقلات العصبية ثم تسمح بإدخال أيونات الكلوريد عبر الغشاء لتخفيف النشاط الكهربائي. وعلى نحو مفاجئ، أوضحت أعمال سابقة أن DmAlka لا يستجيب للغليسين المعتاد وإنما ينشط في الظروف القلوية. هنا يظهر أن DmAlka مضبوط بدقة لنطاق تركيزات البوتاسيوم خارج الخلايا في الظروف الطبيعية، وأن هذا الضبط يؤثر بشدة في كيفية مرور الكلوريد عبر القناة.
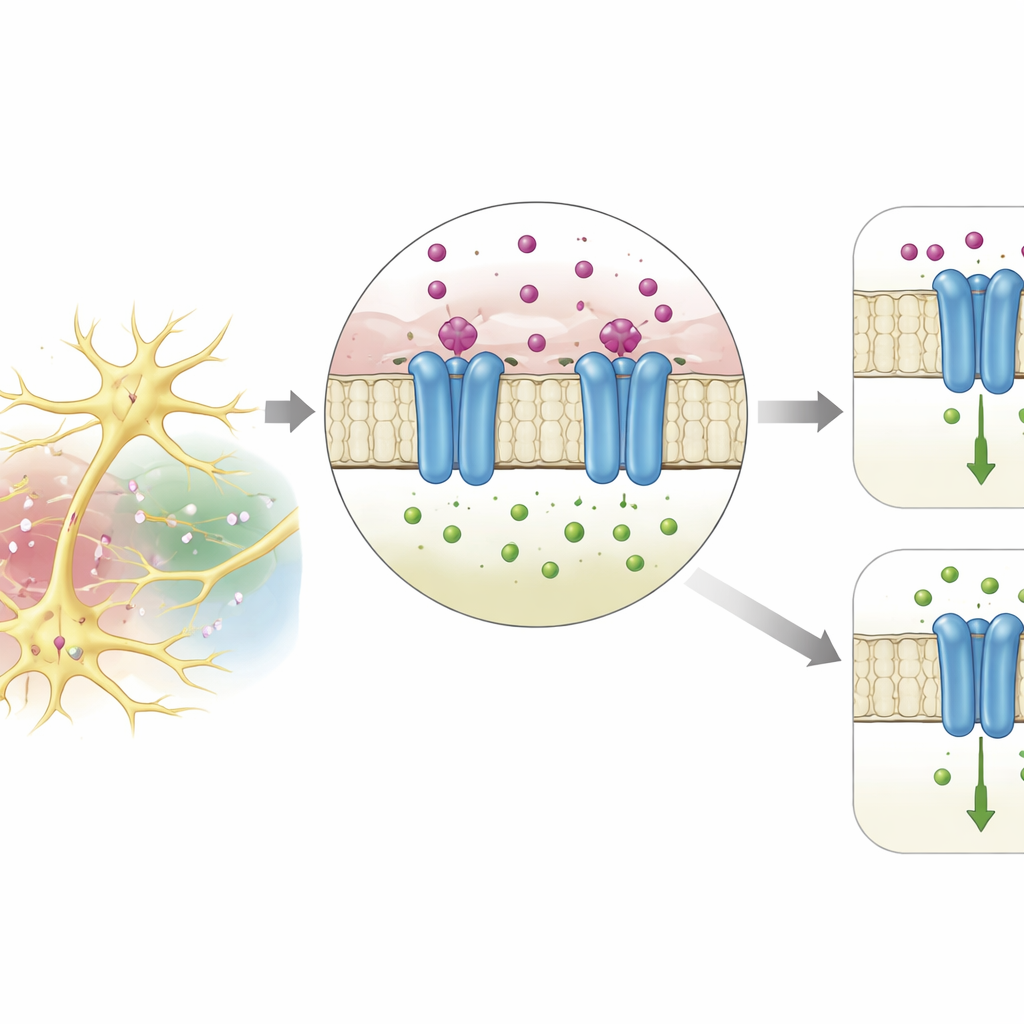
أين يمسك البوتاسيوم
باستخدام برنامج قوي لتنبؤ البنية، نمذج الفريق الشكل ثلاثي الأبعاد لـ DmAlka. كشف النموذج عن جيب صغير عند التقاء الجزء الخارجي الحساس للإشارة من البروتين والمسار العابر للغشاء الذي يحمل الأيونات. في هذا الجيب، يحتضن أيون بوتاسيوم من أربع ذرات أكسجين من أحماض أمينية مجاورة، بترتيب يحاكي عن قرب الطريقة التي يمسك بها البوتاسيوم في قنوات البوتاسيوم الكلاسيكية أو بواسطة جزيئات الماء في المحلول. من خلال تغيير وحدات بنائية فردية تساعد في تشكيل هذا الجيب، تمكن الباحثون من إضعاف أو إلغاء حساسية القناة للبوتاسيوم، مما يؤكد أن هذا الموقع هو بقعة الربط الأساسية. وُجدت سمات مماثلة في بروتينات ذات صلة عبر العديد من مفصليات الأرجل، مما يوحي بأن استراتيجية التعرف على البوتاسيوم هذه محفوظة على نطاق واسع في اللافقاريات.
وضعان يحتويهما المفتاح—يتبدّلان بوجود البوتاسيوم
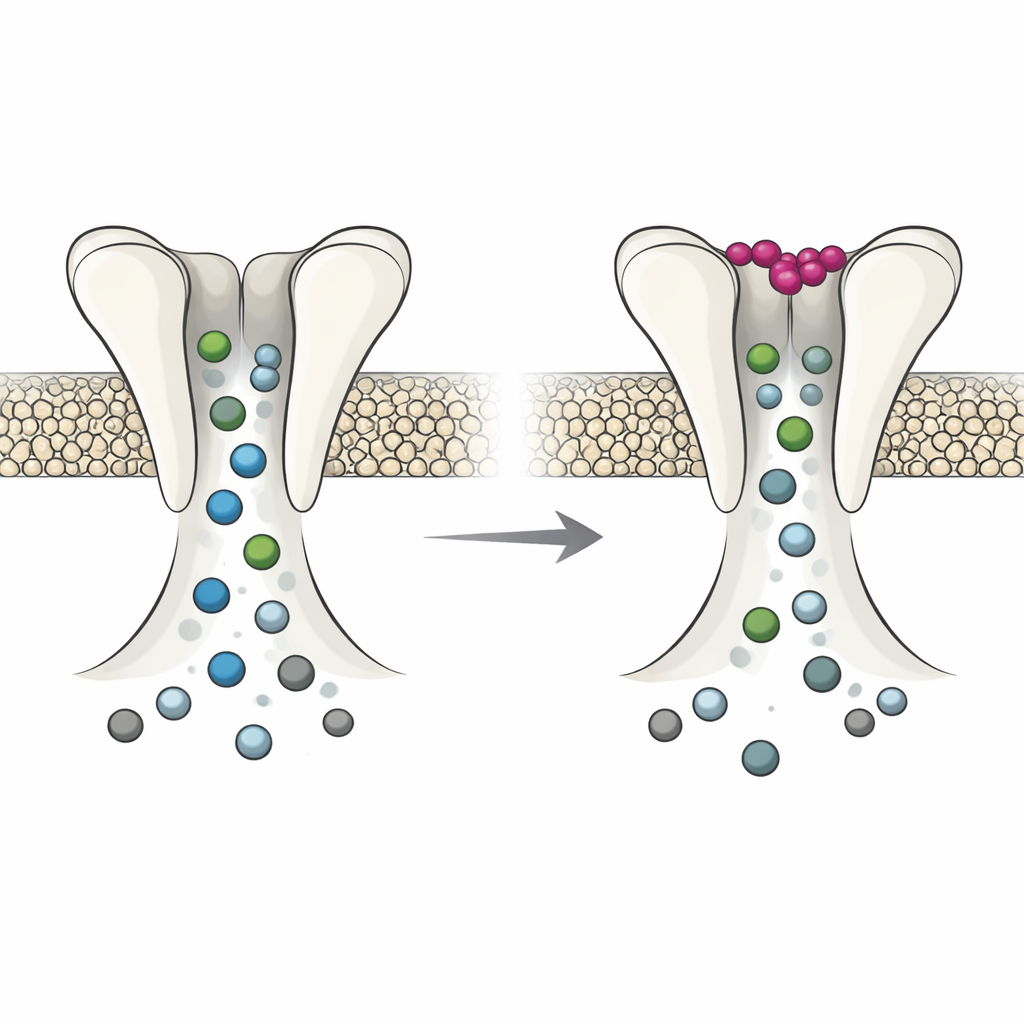
كشفت تجارب كهربية-حيوية في بويضات الضفدع، التي تُستخدم كمختبرات مصغرة لإنتاج القنوات، أن DmAlka يتصرف كمفتاح ذو وضعين. عندما يكون البوتاسيوم خارج الخلية منخفضًا، تكون القناة أكثر احتمالًا للبقاء مفتوحة، وتستجيب بشكل مختلف للظروف القلوية، وتفقد حساسيتها للانطفاء مع الوقت بدرجة أقل. في هذا الوضع، يكون المسار نسبيًا أكثر اتساعًا: يفضّل الكلوريد لكنه يسمح أيضًا لأنيونات سالبة أخرى، مثل البيكربونات، بالمرور بحرية أكبر، ويصبح أقل عرضة للانسداد بواسطة أدوية معينة. عندما يرتبط البوتاسيوم في موقعه الخاص، يتحوّل البروتين كله بشكل طفيف. يضيق المسار ويصبح أكثر اختيارًا للكلوريد، وينقل الأنيونات الأخرى بمعدل أقل، ويظهر استجابة أقوى للجزيئات التي تسد المسام. بعبارة أخرى، يقلب البوتاسيوم خارج الخلية القناة بين حالة مرنة ذات نفاذية واسعة وحالة أضيق مركزة أكثر على الكلوريد.
انعكاسات في الدماغ البشري
من المثير أن الآلية العامة نفسها تبدو موجودة، على الأقل في شكل كامِن، لدى البشر. أحد أنواع مستقبل الغليسين البشري، GlyR α2، يستجيب عادةً للغليسين وليس للبوتاسيوم. من خلال غرْس خصائص رئيسية من جيب البوتاسيوم في DmAlka إلى المستقبل البشري، صنع المؤلفون طفرة اكتسبت حساسية للبوتاسيوم: زيادات البوتاسيوم الخارجي رفعت التيارات الأساسية حتى بغياب الغليسين. أظهروا أيضًا أن متغيرات بشرية طبيعية من GlyR α2، يرتبط بعضها بتغيرات مرتبطة بالصرع، يمكن أن تكتسب استجابة للبوتاسيوم. في هذه المستقبلات البشرية، كما في DmAlka، يحوّل ارتباط البوتاسيوم خصائص المسام، ويغير سهولة مرور الكلوريد والبيكربونات ومدى فعالية بعض المانعَات.
لماذا يهم هذا لصحة الدماغ
نسخة ذبابة الفاكهة من هذه القناة متمركزة بكثافة في الخلايا الدبقية، وهي الخلايا المساندة التي تساعد في المحافظة على توازن البوتاسيوم ودرجة الحموضة حول الخلايا العصبية. تقترح الآلية المكتشفة منطقًا بسيطًا: عندما ينخفض البوتاسيوم خارج الخلية، تفتح DmAlka بطريقة تسمح بدخول المزيد من الكلوريد إلى الخلايا الدبقية ومغادرة المزيد من البيكربونات، مما قد يساعد في استعادة كل من مستويات البوتاسيوم والحموضة في الفراغ المحيط. في البشر، قد يصبح السلوك المضبوط بالبوتاسيوم في مستقبلات الغليسين ذا أهمية في الظروف القصوى، مثل السكتة الدماغية أو النوبات الصرعية، عندما يمكن أن يرتفع البوتاسيوم خارج الخلايا إلى مستويات تفوق الطبيعي بكثير. عمومًا، تكشف هذه الدراسة أن بعض مستقبلات Cys-loop ليست مجرد مستجيبات سلبية للناقلات العصبية؛ بل يمكنها أيضًا أن تعمل كمجسات مباشرة للبيئة الأيونية، رابطًة تغييرات البوتاسيوم خارج الخلية بتبدلات في إشارات الكلوريد عبر الأنواع.
الاستشهاد: Shimomura, T., Kubo, Y., Saitoe, M. et al. Extracellular K+ modulates the pore conformations of Cys-loop receptor anion channels. Nat Commun 17, 3453 (2026). https://doi.org/10.1038/s41467-026-71629-z
الكلمات المفتاحية: استشعار البوتاسيوم خارج الخلية, قنوات الكلوريد, مستقبلات Cys-loop, متغيرات مستقبل الغليسين, توازن الأيونات في الخلايا الدبقية