Clear Sky Science · es
El K+ extracelular modula las conformaciones del poro de los canales aniónicos de receptores de bucle-Cis
Cómo las células "escuchan" el potasio exterior
Cada pensamiento, movimiento y latido del corazón en nuestros cuerpos depende del movimiento de diminutos átomos cargados, o iones, a través de las membranas celulares. El potasio es uno de los iones más importantes, y sus niveles fuera de las neuronas se mantienen dentro de un rango muy estrecho. Este estudio revela una forma inesperada en la que las células cerebrales pueden detectar directamente los cambios en el potasio extracelular y traducirlos en modificaciones del flujo de cloruro, otro ion clave. El trabajo descubre un mecanismo de detección oculto en una familia de receptores neuronales y sugiere nuevas maneras en que el cerebro podría supervisar y responder a su propio entorno químico.
Un nuevo tipo de sensor de potasio
Hasta ahora, la mayoría de los sensores de potasio conocidos en animales eran canales y bombas que usan potasio como combustible o carga, no como señal en sí misma. Los autores se centraron en una proteína poco estudiada de la mosca de la fruta Drosophila, llamada DmAlka, que pertenece a la familia de receptores de bucle-Cis. Los miembros de esta familia suelen formar canales que se abren al unirse a neurotransmisores y permiten que iones de cloruro crucen la membrana para amortiguar la actividad eléctrica. Sorprendentemente, trabajos previos mostraron que DmAlka no responde al neurotransmisor habitual glicina, sino que se activa por condiciones alcalinas (básicas). Aquí, los investigadores muestran que DmAlka también está finamente afinado al rango normal de concentraciones de potasio extracelular, y que esta afinación moldea fuertemente cómo fluye el cloruro a través del canal.
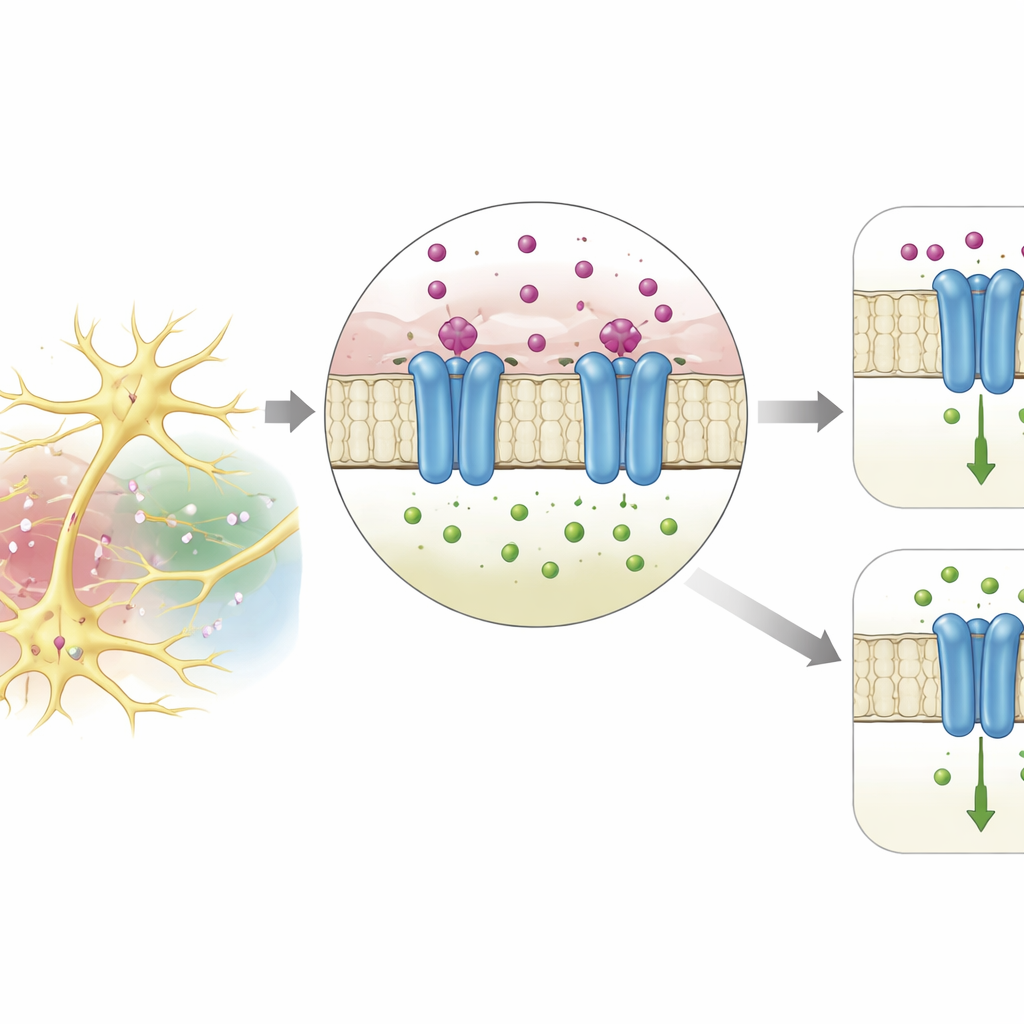
Dónde se agarra el potasio
Usando un potente programa de predicción estructural, el equipo modeló la forma tridimensional de DmAlka. El modelo reveló un pequeño bolsillo en la unión entre la parte externa sensora de señales de la proteína y el poro que atraviesa la membrana y transporta iones. En este bolsillo, un ion potasio queda acunado por cuatro átomos de oxígeno de aminoácidos cercanos, en una disposición que imita de cerca la forma en que el potasio se sostiene en canales clásicos de potasio o por moléculas de agua en solución. Al alterar bloques individuales que ayudan a formar este bolsillo, los investigadores pudieron debilitar o abolir la sensibilidad del canal al potasio, confirmando que este sitio es el punto de anclaje clave. Se encontraron características similares en proteínas relacionadas a lo largo de muchas especies de artrópodos, lo que sugiere que esta estrategia de reconocimiento del potasio está ampliamente conservada en invertebrados.
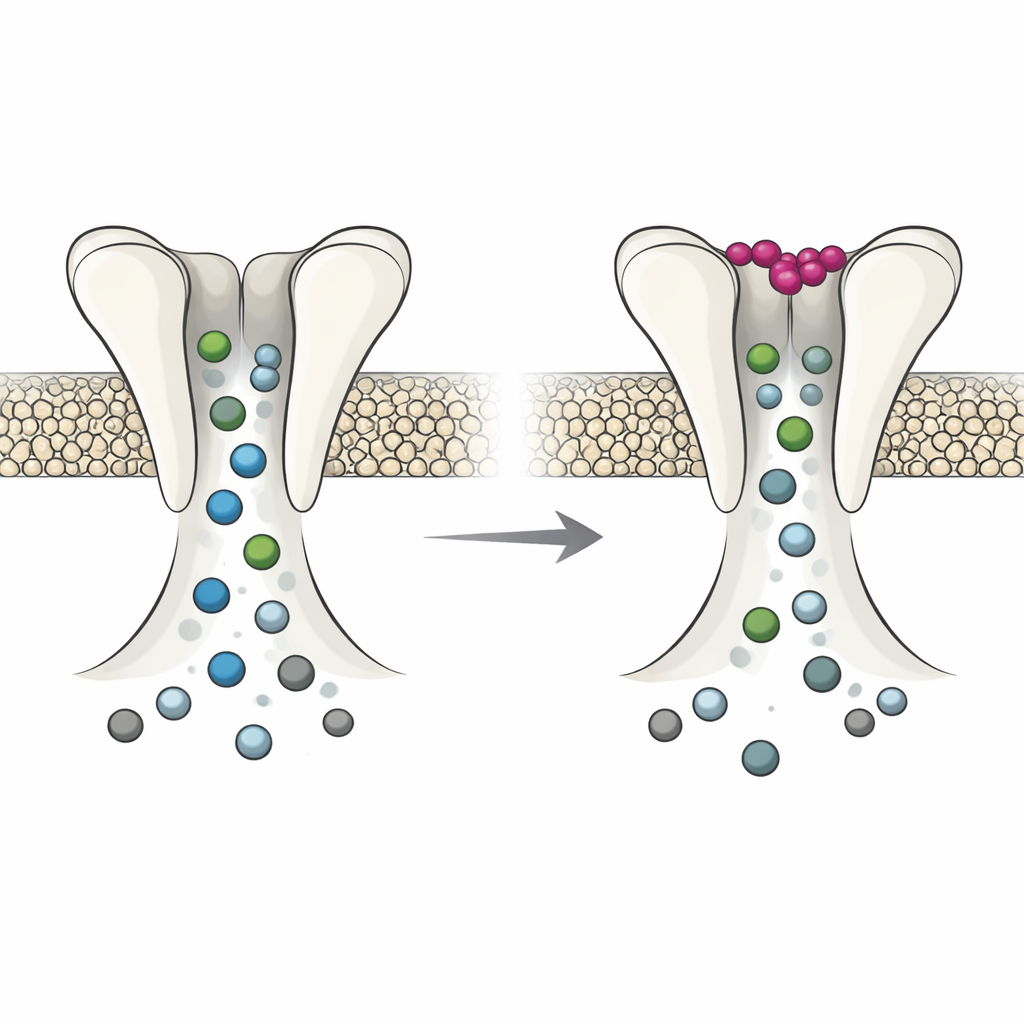
Dos modos, conmutados por potasio
Experimentos de electrofisiología en huevos de rana, que pueden usarse como pequeñas fábricas para producir canales, revelaron que DmAlka se comporta como un interruptor con dos modos. Cuando el potasio extracelular es bajo, el canal tiende a permanecer abierto, responde de forma diferente a condiciones alcalinas y se desensibiliza menos con el tiempo. En este modo, el poro es relativamente holgado: favorece el cloruro pero también permite que otros iones negativos, como el bicarbonato, pasen con mayor facilidad, y se vuelve menos vulnerable al bloqueo por ciertos fármacos. Cuando el potasio se une en su sitio especial, toda la proteína cambia sutilmente. El poro se estrecha y se vuelve más selectivo para el cloruro, conduce peor otros aniones y muestra una respuesta más marcada a moléculas que bloquean el poro. En efecto, el potasio extracelular conmuta el canal entre un estado flexible y ampliamente permeable y un estado más ceñido y centrado en el cloruro.
Resonancias en el cerebro humano
De manera intrigante, el mismo mecanismo general parece existir, al menos en forma latente, en humanos. Un subtipo humano del receptor de glicina, GlyR α2, normalmente responde al neurotransmisor glicina y no al potasio. Al trasplantar características clave del bolsillo de potasio de DmAlka al receptor humano, los autores crearon un mutante que adquirió sensibilidad al potasio: un potasio externo alto aumentó las corrientes basales incluso sin presencia de glicina. También mostraron que variantes humanas naturales de GlyR α2, algunas asociadas con cambios cerebrales relacionados con la epilepsia, pueden adquirir respuesta al potasio. En estos receptores humanos, como en DmAlka, la unión de potasio altera las propiedades del poro, cambiando la facilidad con la que pasan el cloruro y el bicarbonato y la eficacia de ciertos bloqueadores.
Por qué importa para la salud cerebral
La versión de este canal en la mosca está enriquecida en células gliales, las células de soporte que ayudan a mantener el equilibrio de potasio y el pH alrededor de las neuronas. El mecanismo recién descubierto sugiere una lógica simple: cuando el potasio extracelular disminuye, DmAlka se abre de manera que permite que entre más cloruro en las glías y que salga más bicarbonato, lo que podría ayudar a restaurar tanto los niveles de potasio como la acidez en el espacio circundante. En humanos, un comportamiento similar afinado por potasio en receptores de glicina podría volverse importante en condiciones extremas, como un ictus o crisis epilépticas, cuando el potasio extracelular puede dispararse muy por encima de lo normal. En conjunto, este trabajo revela que algunos receptores de bucle-Cis no son solo respondedores pasivos a neurotransmisores; también pueden actuar como sensores directos del entorno iónico, vinculando cambios en el potasio extracelular con alteraciones en la señalización por cloruro a través de especies.
Cita: Shimomura, T., Kubo, Y., Saitoe, M. et al. Extracellular K+ modulates the pore conformations of Cys-loop receptor anion channels. Nat Commun 17, 3453 (2026). https://doi.org/10.1038/s41467-026-71629-z
Palabras clave: detección de potasio extracelular, canales de cloruro, receptores de bucle-Cis, variantes del receptor de glicina, homeostasis iónica glial