Clear Sky Science · it
Il K+ extracellulare modula le conformazioni del poro dei canali anionici della famiglia Cys-loop
Come le cellule ascoltano il potassio esterno
Ogni pensiero, movimento e battito cardiaco nel nostro corpo dipende dal movimento di piccole particelle cariche, o ioni, attraverso le membrane cellulari. Il potassio è uno dei più importanti di questi ioni, e i suoi livelli al di fuori delle cellule nervose sono mantenuti entro un intervallo molto ristretto. Questo studio rivela un modo inaspettato in cui le cellule cerebrali possono rilevare direttamente le variazioni di potassio extracellulare e tradurle in cambiamenti nel flusso di cloruro, un altro ione cruciale. Il lavoro scopre un meccanismo di rilevamento nascosto in una famiglia di recettori neuronali e suggerisce nuove modalità con cui il cervello potrebbe monitorare e rispondere al proprio ambiente chimico.
Un nuovo tipo di sensore per il potassio
Finora, la maggior parte dei sensori di potassio noti negli animali erano canali e pompe che usano il potassio come carburante o come carico, non come segnale in sé. Gli autori si sono concentrati su una proteina poco studiata della Drosophila, chiamata DmAlka, che appartiene alla famiglia dei recettori Cys-loop. I membri di questa famiglia formano tipicamente canali che si aprono quando legano neurotrasmettitori e consentono agli ioni cloruro di attraversare la membrana per smorzare l’attività elettrica. Sorprendentemente, lavori precedenti avevano mostrato che DmAlka non risponde al comune neurotrasmettitore glicina ma è attivata da condizioni alcaline. Qui i ricercatori dimostrano che DmAlka è anche finemente tarata sul normale intervallo di concentrazioni di potassio extracellulare, e che questa taratura influenza profondamente il modo in cui il cloruro attraversa il canale.
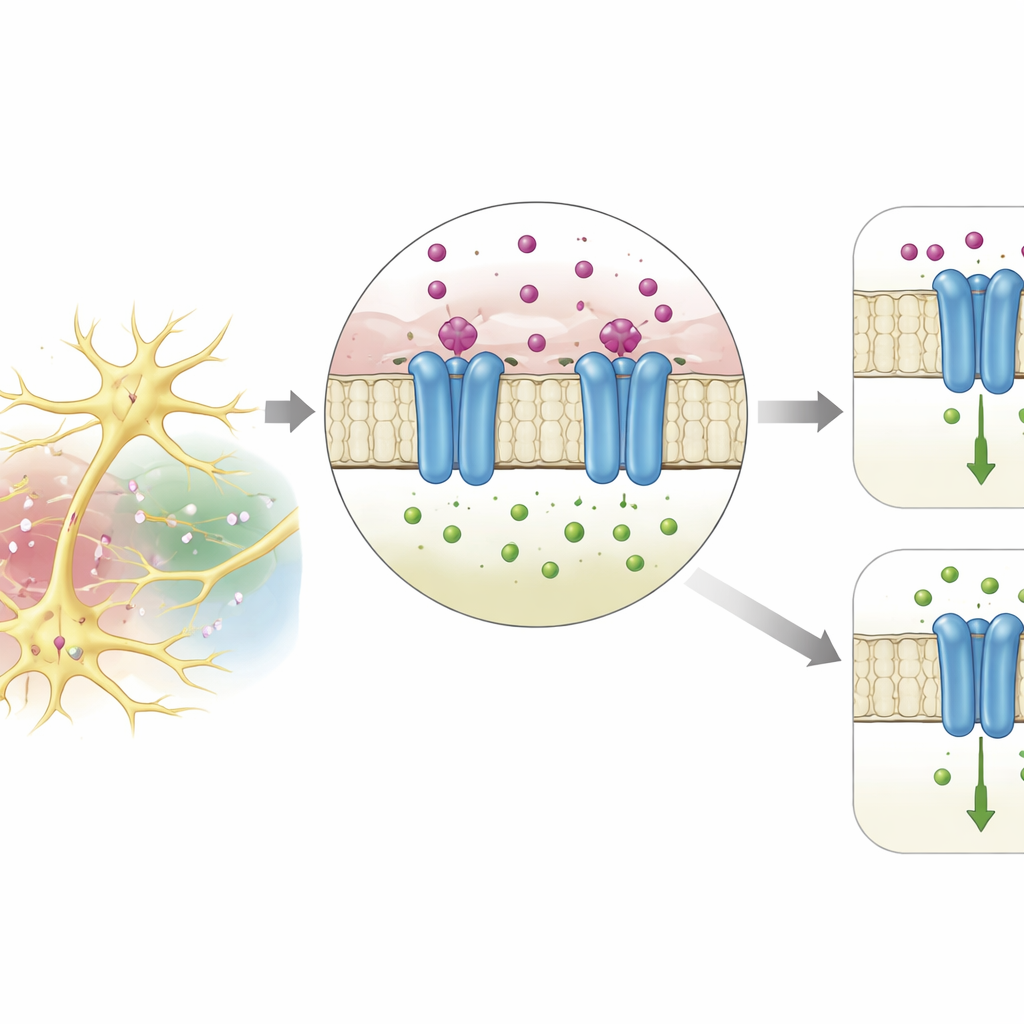
Dove il potassio si ancora
Usando un potente programma di predizione strutturale, il team ha modellato la forma tridimensionale di DmAlka. Il modello ha rivelato una piccola tasca alla giunzione tra la parte esterna sensibile al segnale della proteina e il poro che attraversa la membrana e trasporta gli ioni. In questa tasca, un ione potassio è cullato da quattro atomi di ossigeno provenienti da amminoacidi vicini, in un arrangiamento che imita da vicino il modo in cui il potassio è trattenuto nei classici canali per il potassio o da molecole d’acqua in soluzione. Alterando singoli mattoni che contribuiscono a formare questa tasca, i ricercatori hanno potuto indebolire o abolire la sensibilità del canale al potassio, confermando che questo sito è il punto chiave di aggancio. Caratteristiche simili sono state trovate in proteine correlate in molte specie di artropodi, suggerendo che questa strategia di riconoscimento del potassio sia ampiamente conservata negli invertebrati.
Due modalità, commutate dal potassio
Esperimenti elettrofisiologici in uova di rana, che possono essere usate come mini-fabbriche per produrre canali, hanno rivelato che DmAlka si comporta come un interruttore con due modalità. Quando il potassio extracellulare è basso, il canale tende a rimanere più aperto, risponde in modo diverso alle condizioni alcaline e desensibilizza meno nel tempo. In questa modalità, il poro è relativamente permissivo: favorisce il cloruro ma permette anche il passaggio di altri ioni negativi, come il bicarbonato, in modo più libero, e diventa meno vulnerabile al blocco da parte di alcuni farmaci. Quando il potassio si lega nel suo sito speciale, l’intera proteina si sposta sottilmente. Il poro si restringe e diventa più selettivo per il cloruro, conduce gli altri anioni meno efficacemente e mostra una risposta più marcata a molecole bloccanti del poro. In pratica, il potassio extracellulare commuta il canale tra uno stato flessibile e ampiamente permeabile e uno stato più stretto, focalizzato sul cloruro.
Risonanze nel cervello umano
È intrigante che lo stesso meccanismo generale sembri esistere, almeno in forma latente, anche negli esseri umani. Un sottotipo umano del recettore della glicina, GlyR α2, normalmente risponde al neurotrasmettitore glicina e non al potassio. Trapiantando caratteristiche chiave della tasca per il potassio di DmAlka nel recettore umano, gli autori hanno creato un mutante che ha acquisito sensibilità al potassio: alti livelli di potassio esterno aumentavano le correnti di base anche in assenza di glicina. Hanno inoltre mostrato che varianti umane naturali di GlyR α2, alcune associate a modifiche legate a epilessia nel cervello, possono acquisire reattività al potassio. In questi recettori umani, come in DmAlka, il legame del potassio modifica le proprietà del poro, cambiando quanto facilmente passano cloruro e bicarbonato e quanto efficacemente agiscono certi bloccanti.
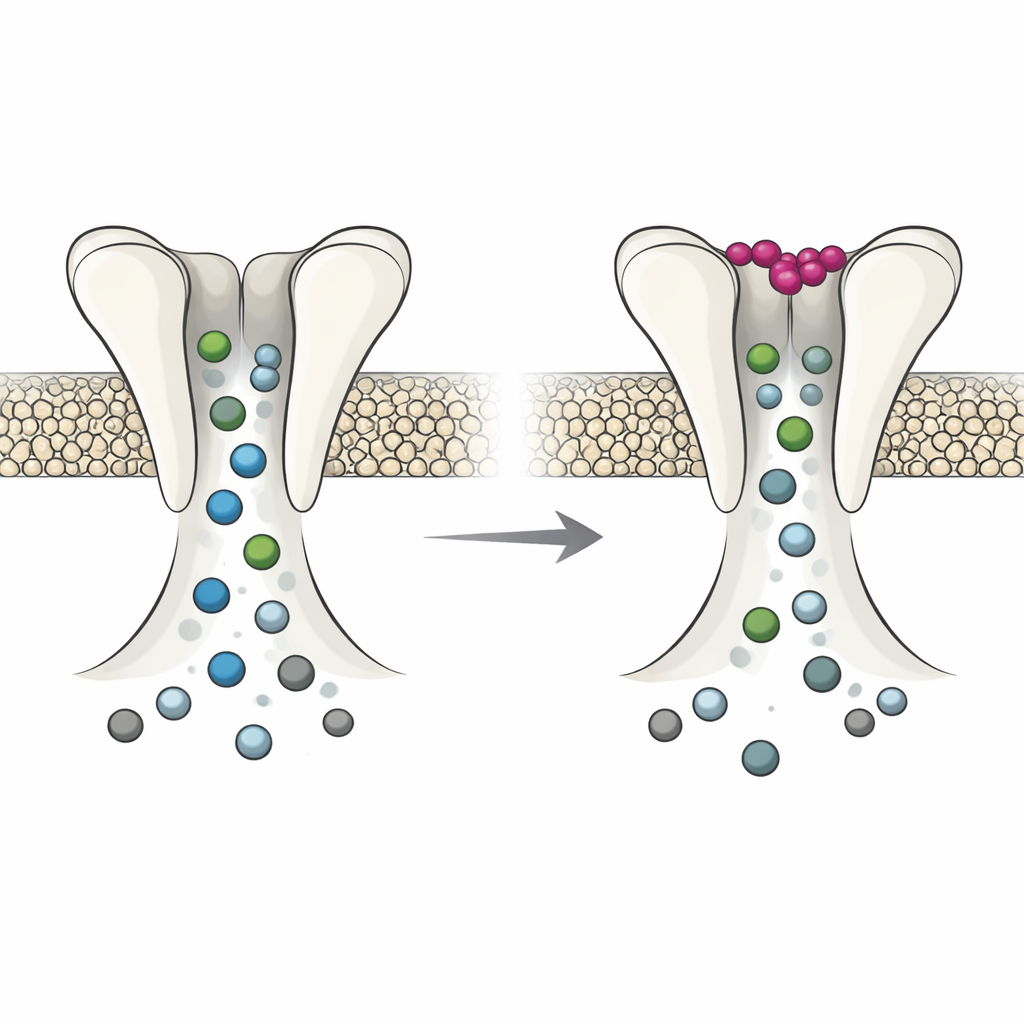
Perché questo è importante per la salute del cervello
La versione della mosca di questo canale è arricchita nelle cellule gliali, le cellule di supporto che aiutano a mantenere l’equilibrio del potassio e il pH intorno ai neuroni. Il meccanismo appena scoperto suggerisce una logica semplice: quando il potassio extracellulare cala, DmAlka si apre in modo da lasciar entrare più cloruro nelle glia e far uscire più bicarbonato, aiutando potenzialmente a ripristinare sia i livelli di potassio sia l’acidità nello spazio circostante. Negli esseri umani, un comportamento simile sintonizzato sul potassio nei recettori della glicina potrebbe diventare importante in condizioni estreme, come ictus o crisi epilettiche, quando il potassio extracellulare può salire ben al di sopra della norma. In complesso, questo lavoro mostra che alcuni recettori Cys-loop non sono solo risponditori passivi ai neurotrasmettitori; possono anche agire come sensori diretti dell’ambiente ionico, collegando le variazioni di potassio extracellulare a cambiamenti nella segnalazione del cloruro attraverso le specie.
Citazione: Shimomura, T., Kubo, Y., Saitoe, M. et al. Extracellular K+ modulates the pore conformations of Cys-loop receptor anion channels. Nat Commun 17, 3453 (2026). https://doi.org/10.1038/s41467-026-71629-z
Parole chiave: rilevamento del potassio extracellulare, canali del cloruro, recettori Cys-loop, varianti del recettore della glicina, omeostasi ionica gliale