Clear Sky Science · pt
K+ extracelular modula as conformações do poro de canais aniônicos da família Cys-loop
Como as células "ouvem" o potássio do lado de fora
Cada pensamento, movimento e batida do coração em nossos corpos depende do movimento de pequenos átomos carregados, ou íons, através das membranas celulares. O potássio é um dos íons mais importantes, e seus níveis fora das células nervosas são mantidos dentro de uma faixa muito estreita. Este estudo revela uma maneira inesperada pela qual as células cerebrais podem detectar diretamente mudanças no potássio extracelular e traduzi-las em alterações no fluxo de cloreto, outro íon-chave. O trabalho descobre um mecanismo sensorial oculto em uma família de receptores neurais e sugere novas formas pelas quais o cérebro pode monitorar e responder ao seu próprio ambiente químico.
Um novo tipo de sensor de potássio
Até agora, a maioria dos sensores conhecidos de potássio em animais eram canais e bombas que usam potássio como combustível ou carga, não como um sinal por si só. Os autores focaram em uma proteína pouco estudada na mosca-da-fruta Drosophila, chamada DmAlka, que pertence à família dos receptores Cys-loop. Membros dessa família tipicamente formam canais que se abrem ao ligarem neurotransmissores e então permitem que íons de cloreto atravessem a membrana para atenuar a atividade elétrica. Surpreendentemente, trabalhos anteriores mostraram que DmAlka não responde ao neurotransmissor usual glicina, mas é ativada por condições alcalinas. Aqui, os pesquisadores mostram que DmAlka também é finamente ajustada à faixa normal de concentrações de potássio extracelular, e que esse ajuste molda fortemente como o cloreto flui através do canal.
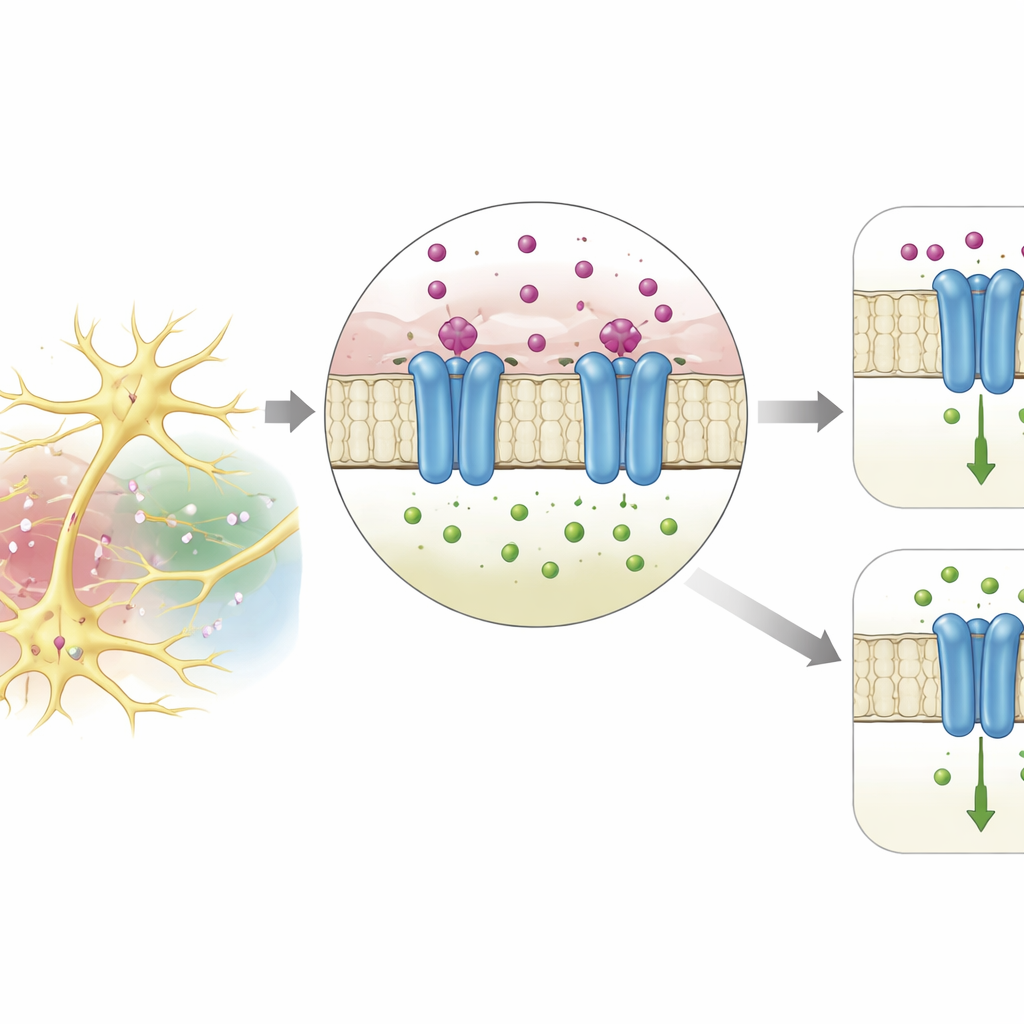
Onde o potássio se prende
Usando um poderoso programa de predição estrutural, a equipe modelou a forma tridimensional de DmAlka. O modelo revelou um pequeno bolso na junção entre a parte externa sensora de sinais da proteína e o poro transmembrana que conduz íons. Nesse bolso, um íon potássio é acolhido por quatro átomos de oxigênio de aminoácidos próximos, em um arranjo que imita de perto a forma como o potássio é retido em canais de potássio clássicos ou por moléculas de água em solução. Ao alterar blocos de construção individuais que ajudam a formar esse bolso, os pesquisadores puderam enfraquecer ou abolir a sensibilidade do canal ao potássio, confirmando que esse sítio é o ponto de ancoragem chave. Características semelhantes foram encontradas em proteínas relacionadas em muitas espécies de artrópodes, sugerindo que essa estratégia de reconhecimento de potássio é amplamente conservada em invertebrados.
Dois modos, alternados pelo potássio
Experimentos eletrofisiológicos em oócitos de rã, que podem ser usados como mini fábricas para produzir canais, revelaram que DmAlka se comporta como um interruptor com dois modos. Quando o potássio extracelular é baixo, o canal tende a permanecer aberto, responde de forma diferente a condições alcalinas e dessensibiliza menos ao longo do tempo. Nesse modo, o poro é relativamente frouxo: favorece o cloreto, mas também permite que outros íons negativos, como bicarbonato, passem mais livremente, e torna-se menos vulnerável ao bloqueio por certos fármacos. Quando o potássio se liga ao seu sítio especial, toda a proteína se desloca sutilmente. O poro se estreita e torna-se mais seletivo para cloreto, conduz outros ânions menos eficientemente e mostra uma resposta mais forte a moléculas que bloqueiam o poro. Em efeito, o potássio extracelular alterna o canal entre um estado flexível e amplamente permeável e um estado mais restrito e focado no cloreto.
Ressonâncias no cérebro humano
Intrigantemente, o mesmo mecanismo geral parece existir, ao menos de forma latente, em humanos. Um subtipo humano do receptor de glicina, GlyR α2, normalmente responde ao neurotransmissor glicina e não ao potássio. Ao transplantar características-chave do bolso de potássio de DmAlka para o receptor humano, os autores criaram um mutante que adquiriu sensibilidade ao potássio: altas concentrações extracelulares de potássio aumentaram correntes basais mesmo na ausência de glicina. Eles também mostraram que variantes humanas naturais de GlyR α2, algumas associadas a alterações relacionadas à epilepsia, podem ganhar responsividade ao potássio. Nesses receptores humanos, assim como em DmAlka, a ligação de potássio altera as propriedades do poro, mudando a facilidade com que cloreto e bicarbonato passam e a eficácia de certos bloqueadores.
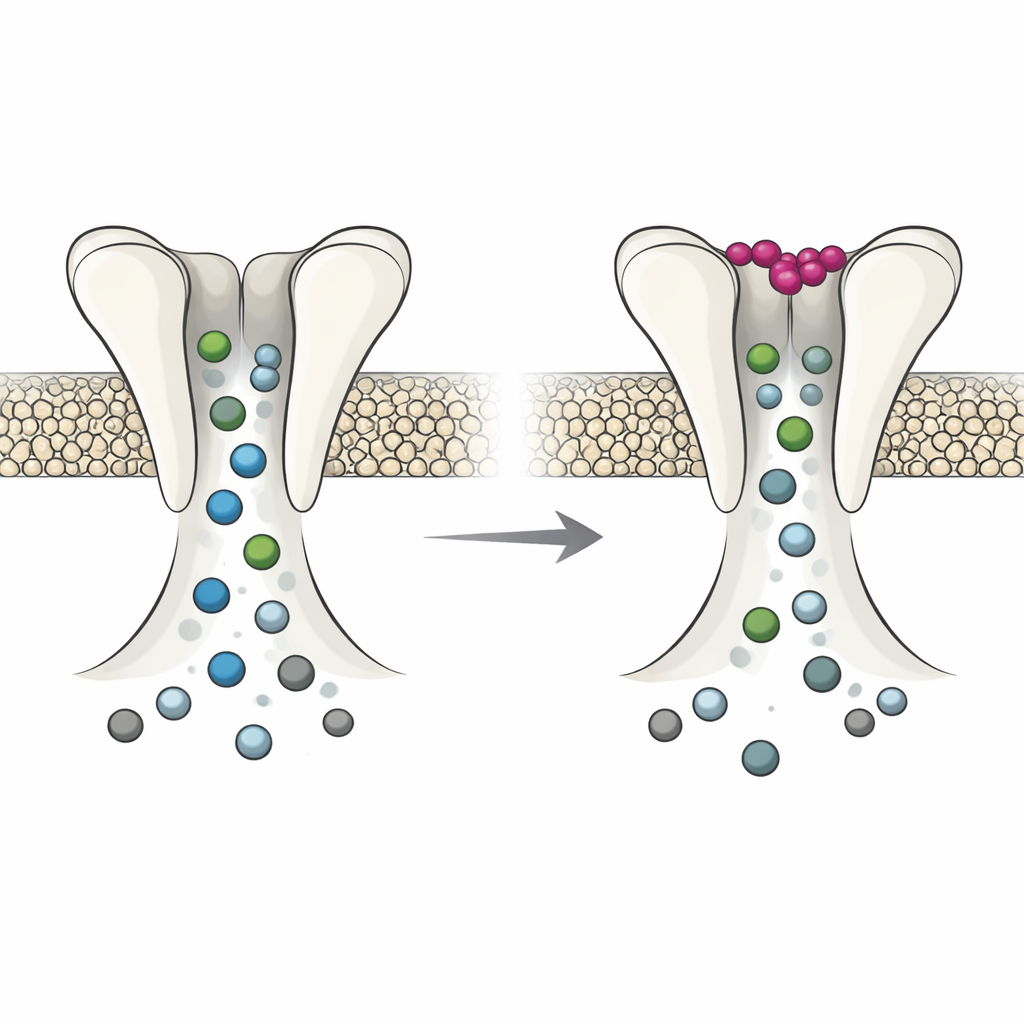
Por que isso importa para a saúde do cérebro
A versão desse canal na mosca é enriquecida em células gliais, as células de suporte que ajudam a manter o balanço de potássio e o pH ao redor dos neurônios. O mecanismo recém-descoberto sugere uma lógica simples: quando o potássio extracelular cai, DmAlka se abre de modo a permitir que mais cloreto entre nas glias e que mais bicarbonato saia, potencialmente ajudando a restaurar tanto os níveis de potássio quanto a acidez no espaço circundante. Em humanos, um comportamento sintonizado por potássio em receptores de glicina semelhantes pode tornar-se relevante em condições extremas, como AVC ou crises epilépticas, quando o potássio extracelular pode disparar muito acima do normal. No geral, este trabalho revela que alguns receptores Cys-loop não são apenas respondedores passivos a neurotransmissores; eles também podem atuar como sensores diretos do ambiente iônico, ligando mudanças no potássio extracelular a alterações na sinalização por cloreto entre espécies.
Citação: Shimomura, T., Kubo, Y., Saitoe, M. et al. Extracellular K+ modulates the pore conformations of Cys-loop receptor anion channels. Nat Commun 17, 3453 (2026). https://doi.org/10.1038/s41467-026-71629-z
Palavras-chave: detecção de potássio extracelular, canais de cloreto, receptores Cys-loop, variantes do receptor de glicina, homeostase iônica glial