Clear Sky Science · fr
Le K+ extracellulaire module les conformations du pore des canaux anioniques de la famille Cys-loop
Comment les cellules « écoutent » le potassium extérieur
Chaque pensée, mouvement et battement de coeur dépend des déplacements de minuscules atomes chargés, ou ions, à travers les membranes cellulaires. Le potassium est l’un des plus importants de ces ions, et sa concentration à l’extérieur des neurones est maintenue dans une fourchette très étroite. Cette étude révèle une façon inattendue dont les cellules cérébrales peuvent détecter directement les variations de potassium extracellulaire et les traduire en modifications du flux de chlorure, un autre ion clé. Les travaux mettent au jour un mécanisme de détection caché au sein d’une famille de récepteurs neuronaux et suggèrent de nouvelles manières dont le cerveau pourrait surveiller et réagir à son propre environnement chimique.
Un nouveau type de capteur de potassium
Jusqu’à présent, la plupart des capteurs connus du potassium chez les animaux étaient des canaux ou des pompes qui utilisent le potassium comme carburant ou cargaison, mais pas comme signal en soi. Les auteurs se sont intéressés à une protéine peu étudiée de la drosophile Drosophila, appelée DmAlka, qui appartient à la famille des récepteurs Cys-loop. Les membres de cette famille forment typiquement des canaux qui s’ouvrent lorsqu’ils lient des neurotransmetteurs, laissant alors passer des ions chlorure à travers la membrane pour atténuer l’excitabilité électrique. De façon surprenante, des travaux antérieurs avaient montré que DmAlka ne répond pas au neurotransmetteur usuel glycine mais s’active dans des conditions alcalines. Ici, les chercheurs montrent que DmAlka est aussi finement accordé à la plage normale des concentrations de potassium extracellulaire, et que cet accord influence fortement la façon dont le chlorure circule dans le canal.
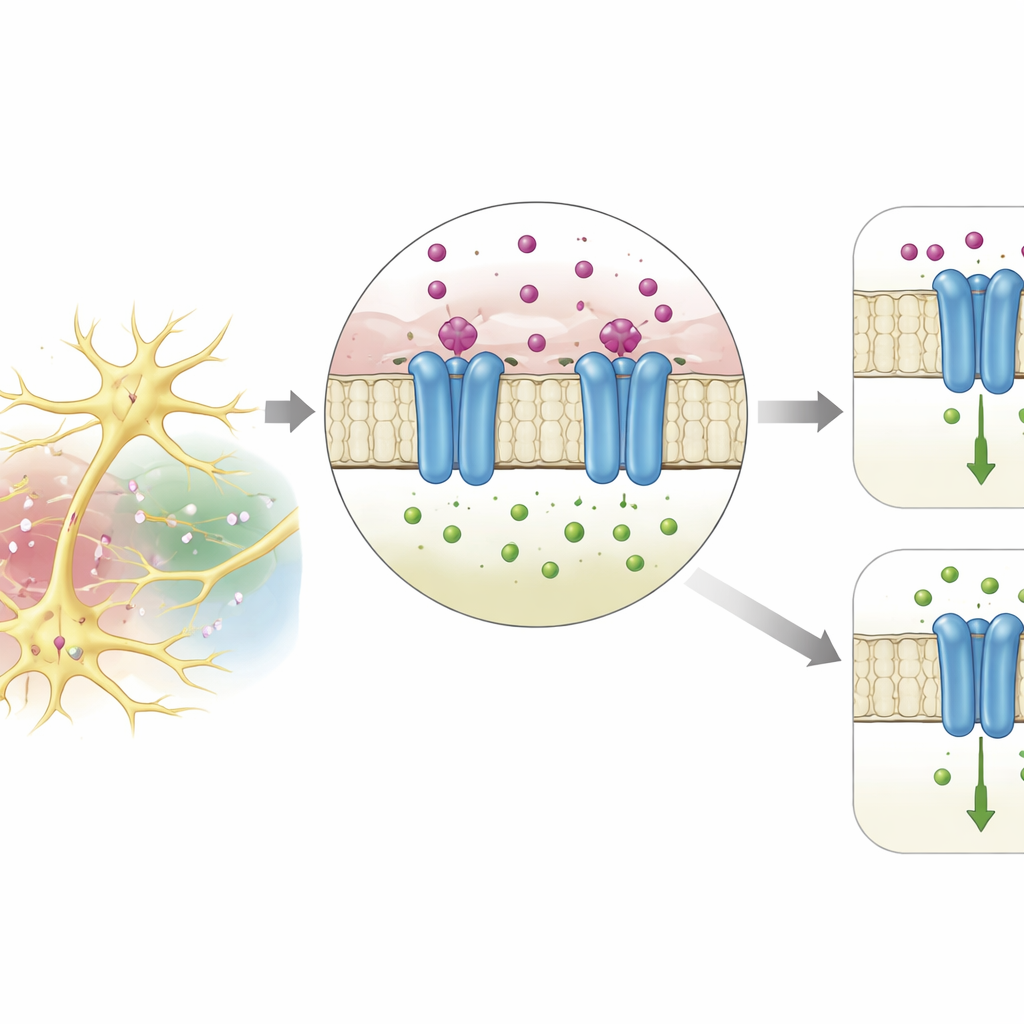
Où le potassium s’accroche
En utilisant un puissant programme de prédiction de structures, l’équipe a modélisé la forme tridimensionnelle de DmAlka. Le modèle a révélé une petite poche à la jonction entre la partie externe détectrice de signaux de la protéine et le pore traversant la membrane qui transporte les ions. Dans cette poche, un ion potassium est soutenu par quatre atomes d’oxygène issus d’acides aminés voisins, dans une configuration qui imite de près la manière dont le potassium est retenu dans les canaux potassiques classiques ou par des molécules d’eau en solution. En modifiant des éléments constitutifs individuels qui contribuent à former cette poche, les chercheurs ont pu affaiblir ou abolir la sensibilité du canal au potassium, confirmant que ce site est le point d’amarrage clé. Des caractéristiques similaires ont été trouvées dans des protéines apparentées chez de nombreux arthropodes, suggérant que cette stratégie de reconnaissance du potassium est largement conservée chez les invertébrés.
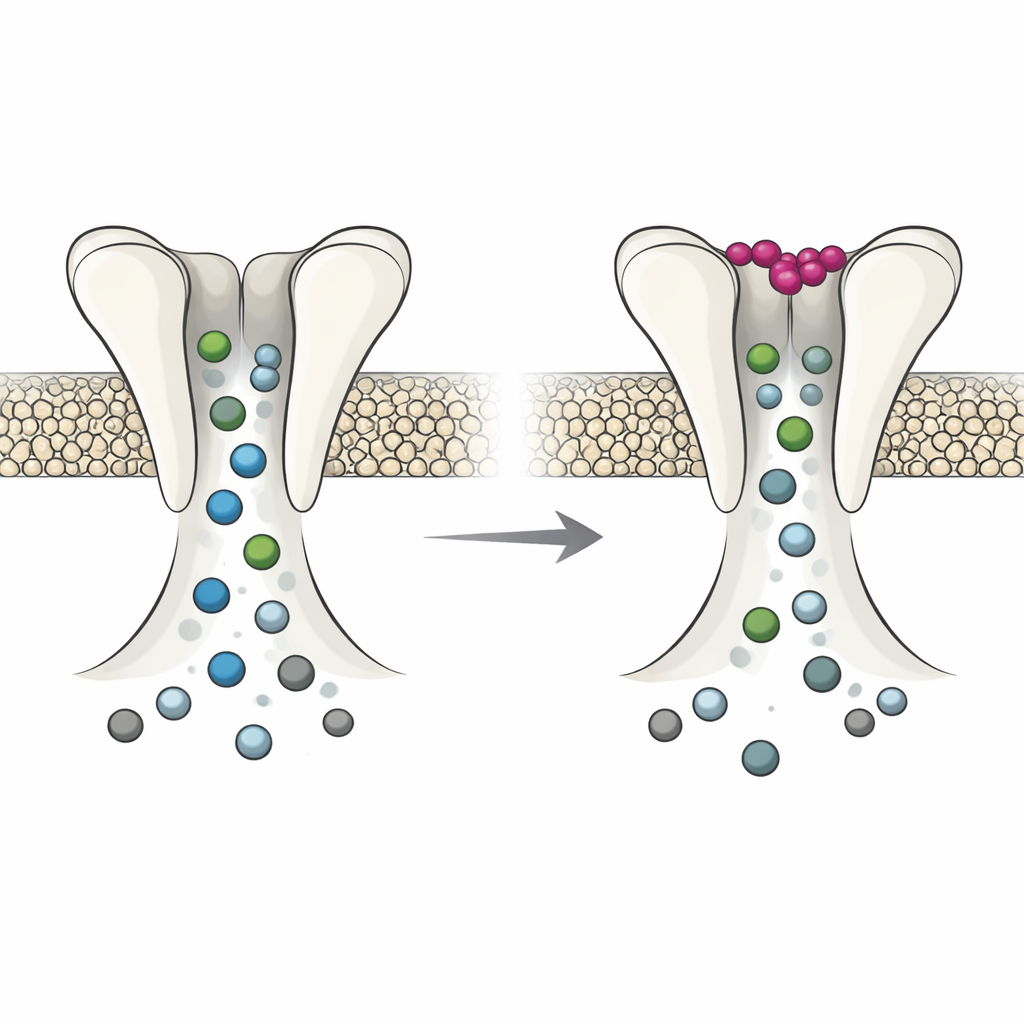
Deux modes, commutés par le potassium
Des expériences d’électrophysiologie réalisées dans des ovocytes de grenouille, qui servent de mini-usines pour produire des canaux, ont révélé que DmAlka se comporte comme un commutateur à deux modes. Lorsque le potassium extracellulaire est bas, le canal a davantage tendance à rester ouvert, réagit différemment aux conditions alcalines et se désensibilise moins avec le temps. Dans ce mode, le pore est relativement lâche : il favorise le chlorure mais permet aussi à d’autres anions, comme le bicarbonate, de passer plus librement, et il devient moins vulnérable au blocage par certains médicaments. Quand le potassium se lie à son site particulier, la protéine entière se réajuste subtilement. Le pore se resserre et devient plus sélectif pour le chlorure, conduit moins bien les autres anions et montre une réponse plus marquée aux molécules bloquant le pore. En somme, le potassium extracellulaire bascule le canal entre un état flexible et largement perméable et un état plus étroit, centré sur le chlorure.
Des répercussions dans le cerveau humain
De manière intrigante, le même mécanisme général semble exister, au moins sous une forme latente, chez l’homme. Un sous-type humain du récepteur de la glycine, GlyR α2, répond normalement au neurotransmetteur glycine et non au potassium. En transplantant les caractéristiques clés de la poche à potassium de DmAlka dans le récepteur humain, les auteurs ont créé un mutant qui a gagné une sensibilité au potassium : un fort potassium extracellulaire augmentait les courants de base même en l’absence de glycine. Ils ont également montré que des variantes humaines naturelles de GlyR α2, certaines associées à des altérations liées à l’épilepsie, peuvent acquérir une réactivité au potassium. Dans ces récepteurs humains, comme dans DmAlka, la liaison du potassium modifie les propriétés du pore, changeant la facilité de passage du chlorure et du bicarbonate et l’efficacité de certains bloqueurs.
Pourquoi c’est important pour la santé cérébrale
La version de ce canal chez la drosophile est enrichie dans les cellules gliales, les cellules de soutien qui aident à maintenir l’équilibre du potassium et le pH autour des neurones. Le mécanisme nouvellement mis au jour suggère une logique simple : quand le potassium extracellulaire diminue, DmAlka s’ouvre d’une manière qui laisse entrer davantage de chlorure dans les glies et laisse sortir plus de bicarbonate, aidant potentiellement à restaurer à la fois les niveaux de potassium et l’acidité de l’espace environnant. Chez l’homme, un comportement similaire accordé au potassium dans les récepteurs de la glycine pourrait devenir important dans des conditions extrêmes, comme un accident vasculaire cérébral ou des crises épileptiques, lorsque le potassium extracellulaire peut monter bien au‑dessus de la normale. Globalement, ces travaux montrent que certains récepteurs Cys-loop ne sont pas seulement des récepteurs passifs de neurotransmetteurs ; ils peuvent aussi jouer le rôle de capteurs directs de l’environnement ionique, reliant les variations de potassium extracellulaire à des changements dans la signalisation par le chlorure entre les espèces.
Citation: Shimomura, T., Kubo, Y., Saitoe, M. et al. Extracellular K+ modulates the pore conformations of Cys-loop receptor anion channels. Nat Commun 17, 3453 (2026). https://doi.org/10.1038/s41467-026-71629-z
Mots-clés: détection du potassium extracellulaire, canaux chlorure, récepteurs Cys-loop, variantes du récepteur de la glycine, homéostasie ionique gliale