Clear Sky Science · sv
Extracellärt K+ påverkar porernas konformationer i Cys-loop-receptorers anjonkanaler
Hur celler ”lyssnar” på kalium utanför
Varje tanke, rörelse och hjärtslag i våra kroppar beror på små laddade atomer, joner, som rör sig över cellmembran. Kalium är en av de viktigaste av dessa joner, och dess nivåer utanför nervceller hålls inom ett mycket snävt intervall. Denna studie visar ett oväntat sätt som hjärnceller direkt kan känna av förändringar i extracellulärt kalium och översätta dem till förändringar i kloridflödet, en annan nyckeljon. Arbetet avslöjar en dold avkänningsmekanism i en familj av nervreceptorer och antyder nya sätt som hjärnan kan övervaka och reagera på sin kemiska omgivning.
En ny sorts kaliumsensor
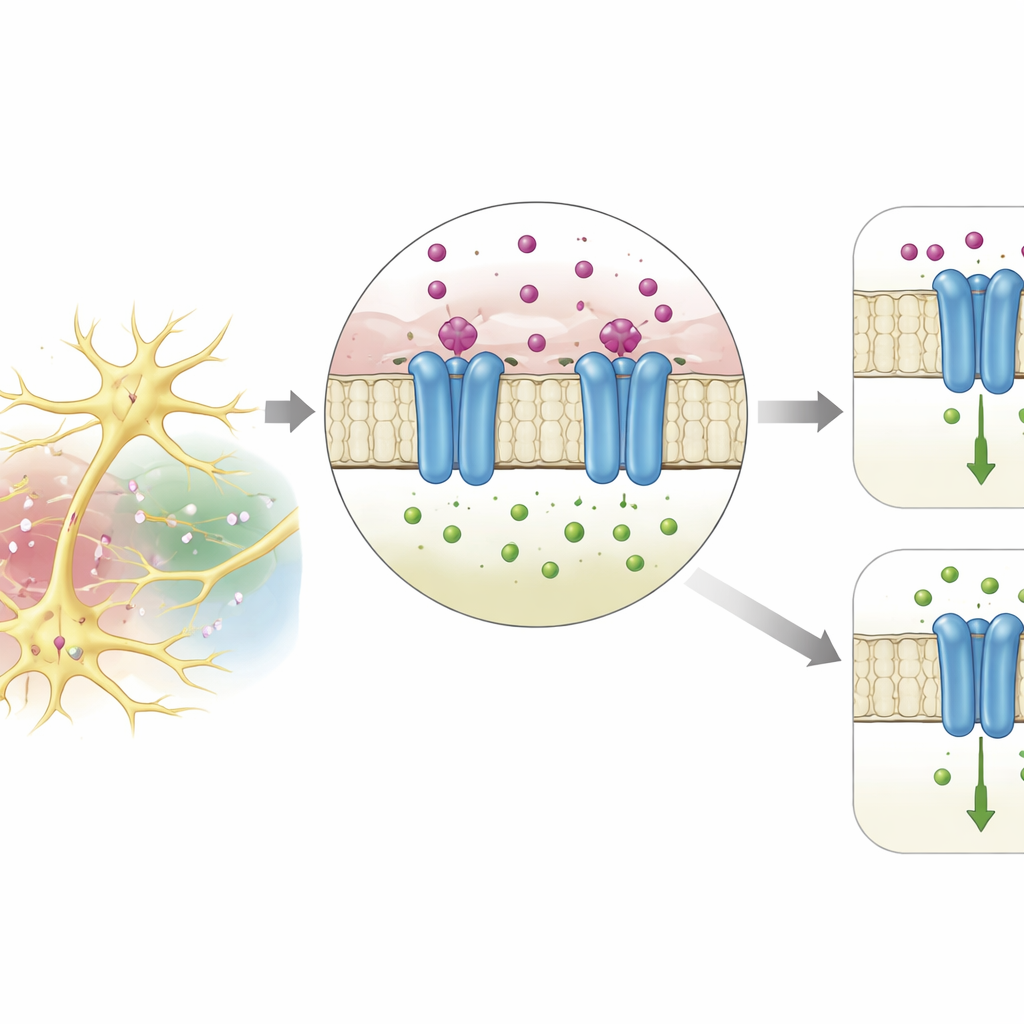
Hittills var de flesta kända kaliumsensorer hos djur kanaler och pumpar som använder kalium som bränsle eller last, inte som en signal i sig. Författarna fokuserade på ett lite studerat protein i fruktflugan Drosophila, kallat DmAlka, som tillhör Cys-loop-receptorfamiljen. Medlemmar i denna familj bildar vanligtvis kanaler som öppnas när de binder neurotransmittorer och sedan tillåter kloridjoner att korsa membranet för att dämpa elektrisk aktivitet. Överraskande nog visade tidigare arbete att DmAlka inte svarar på den vanliga neurotransmittorn glycin utan aktiveras av alkaliska (basiska) förhållanden. Här visar forskarna att DmAlka även är fint inställd på det normala intervallet av kaliumkoncentrationer utanför celler, och att denna inställning starkt formar hur klorid flödar genom kanalen.
Var kaliumet tar tag
Genom att använda ett kraftfullt strukturförutsägelseprogram modellerade teamet DmAlkas tredimensionella form. Modellen avslöjade en liten ficka vid skarven mellan den yttre, signalavkännande delen av proteinet och den membranövergående poren som för joner. I denna ficka vaggar en kaliumjon omgiven av fyra syreatomer från närliggande aminosyror, i en arrangemang som nära efterliknar hur kalium hålls i klassiska kaliumkanaler eller av vattenmolekyler i lösning. Genom att förändra enskilda byggstenar som hjälper till att forma denna ficka kunde forskarna försvaga eller avskaffa kanalens känslighet för kalium, vilket bekräftar att denna plats är den avgörande dockningspunkten. Liknande drag hittades i närbesläktade proteiner över många leddjur, vilket tyder på att denna strategi för kaliumigenkänning är vida bevarad hos ryggradslösa djur.
Två lägen, växlade av kalium
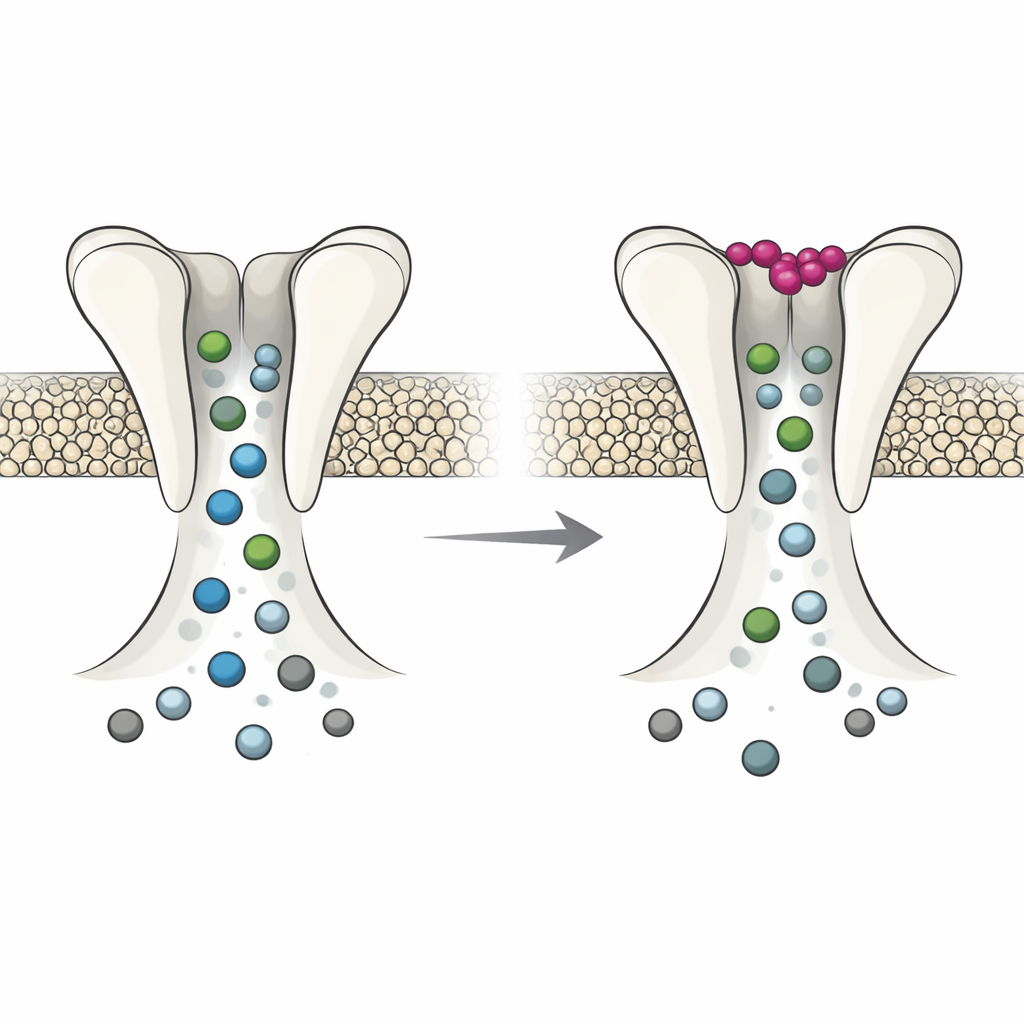
Elektrofysiologiska experiment i grodägg, som kan användas som miniatyrfabriker för att producera kanaler, visade att DmAlka beter sig som en strömbrytare med två lägen. När kalium utanför cellen är lågt är kanalen mer benägen att vara öppen, svarar annorlunda på basiska förhållanden och desensitiseras mindre över tid. I detta läge är poren relativt vid: den favoriserar klorid men tillåter också andra negativa joner, såsom bikarbonat, att passera mer fritt, och den blir mindre sårbar för blockering av vissa läkemedel. När kalium binder vid sin speciella plats skiftar hela proteinet subtilt. Poren smalnar och blir mer selektiv för klorid, leder andra anjoner sämre och visar ett starkare svar på porblockerande molekyler. I praktiken växlar extracellulärt kalium kanalen mellan ett flexibelt, brett permeabelt tillstånd och ett tajtare, mer kloridfokuserat tillstånd.
Ekon i den mänskliga hjärnan
Intressant nog verkar samma övergripande mekanism finnas, åtminstone i latent form, hos människor. En mänsklig glycinreceptorsubtyp, GlyR α2, svarar normalt på neurotransmittorn glycin och inte på kalium. Genom att transplantera nyckelfunktioner från DmAlkas kaliumficka in i den humana receptorn skapade författarna en mutant som fick kaliumkänslighet: hög yttre kalium ökade baslinjeströmmar även utan glycin närvarande. De visade också att naturligt förekommande mänskliga varianter av GlyR α2, några associerade med epilepsi-relaterade förändringar i hjärnan, kan förvärva kaliumrespons. I dessa humana receptorer, liksom i DmAlka, förskjuter kaliumbindning poregenskaperna och ändrar hur lätt klorid och bikarbonat passerar och hur effektiva vissa blockerare är.
Varför det här spelar roll för hjärnhälsa
Fruktflugans version av denna kanal är rikligt förekommande i gliaceller, stödceller som hjälper till att upprätthålla kaliumbalans och pH runt neuroner. Den nyligen avslöjade mekanismen föreslår en enkel logik: när extracellulärt kalium sjunker öppnas DmAlka på ett sätt som släpper in mer klorid i glia och släpper ut mer bikarbonat, vilket potentiellt hjälper till att återställa både kaliumnivåer och surhetsgrad i den omgivande rymden. Hos människor kan liknande kaliuminställda beteenden i glycinreceptorer bli viktiga under extrema förhållanden, såsom stroke eller epileptiska anfall, när kalium utanför neuroner kan skjuta i höjden långt över det normala. Sammantaget visar detta arbete att vissa Cys-loop-receptorer inte bara är passiva mottagare av neurotransmittorer; de kan också fungera som direkta sensorer av den joniska miljön och länka förändringar i extracellulärt kalium till skiften i kloridsignalering över arter.
Citering: Shimomura, T., Kubo, Y., Saitoe, M. et al. Extracellular K+ modulates the pore conformations of Cys-loop receptor anion channels. Nat Commun 17, 3453 (2026). https://doi.org/10.1038/s41467-026-71629-z
Nyckelord: extracellulär kaliumavkänning, kloridkanaler, Cys-loop-receptorer, varianter av glycinreceptorer, glial jonhomeostas