Clear Sky Science · de
Extrazelluläres K+ moduliert die Porenkonformationen von Cys‑Loop‑Rezeptor‑Anionkanälen
Wie Zellen auf Kalium außerhalb hören
Jeder Gedanke, jede Bewegung und jeder Herzschlag in unserem Körper beruht auf winzigen geladenen Atomen, sogenannten Ionen, die über Zellmembranen wandern. Kalium ist eines der wichtigsten dieser Ionen, und seine Konzentration außerhalb von Nervenzellen wird in einem sehr engen Bereich gehalten. Diese Studie zeigt einen unerwarteten Mechanismus, mit dem Gehirnzellen Änderungen des extrazellulären Kaliums direkt wahrnehmen und in Veränderungen des Chloridflusses — eines weiteren Schlüsselsalzes — übersetzen können. Die Arbeit deckt einen verborgenen Sensor in einer Familie von Nervenrezeptoren auf und schlägt neue Möglichkeiten vor, wie das Gehirn seine chemische Umgebung überwachen und darauf reagieren könnte.
Eine neue Art Kalium‑Sensor
Bisher waren die meisten bekannten Kalium‑Sensoren bei Tieren Kanäle und Pumpen, die Kalium als Treibstoff oder Fracht nutzen, nicht als eigenständiges Signal. Die Autoren konzentrierten sich auf ein wenig untersuchtes Protein der Fruchtfliege Drosophila, genannt DmAlka, das zur Familie der Cys‑Loop‑Rezeptoren gehört. Mitglieder dieser Familie bilden typischerweise Kanäle, die sich öffnen, wenn sie Neurotransmitter binden, und dann Chloridionen über die Membran lassen, um die elektrische Aktivität zu dämpfen. Überraschenderweise zeigte frühere Arbeit, dass DmAlka nicht auf den üblichen Neurotransmitter Glycin reagiert, sondern durch alkalische (basische) Bedingungen aktiviert wird. Hier zeigen die Forschenden, dass DmAlka außerdem fein auf den normalen Bereich extrazellulärer Kaliumkonzentrationen abgestimmt ist und dass diese Abstimmung die Chloridströmung durch den Kanal stark beeinflusst.
Wo Kalium griffbereit liegt
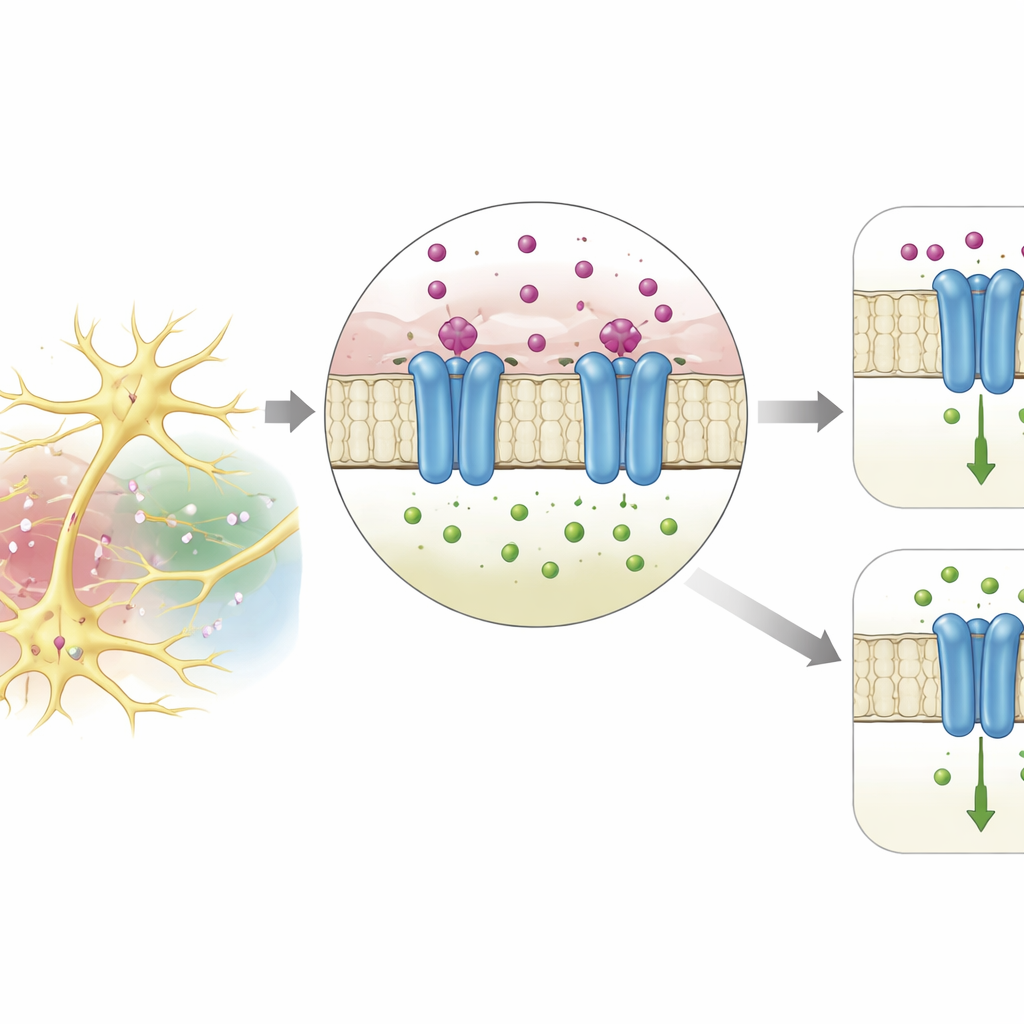
Mithilfe eines leistungsfähigen Strukturvorhersageprogramms modellierte das Team die dreidimensionale Gestalt von DmAlka. Das Modell offenbarte eine kleine Tasche an der Nahtstelle zwischen dem äußeren, Signalsensor‑Teil des Proteins und der membranüberspannenden Pore, die Ionen transportiert. In dieser Tasche ruht ein Kaliumion, gehalten von vier Sauerstoffatomen benachbarter Aminosäuren, in einer Anordnung, die stark der Art ähnelt, wie Kalium in klassischen Kaliumkanälen oder von Wassermolekülen in Lösung gebunden wird. Durch Veränderung einzelner Bausteine, die diese Tasche formen, konnten die Forscher die Kaliumempfindlichkeit des Kanals abschwächen oder beseitigen, was bestätigt, dass dieser Ort die entscheidende Andockstelle ist. Ähnliche Merkmale fanden sich in verwandten Proteinen vieler Arthropodenarten, was darauf hindeutet, dass diese Kalium‑Erkennungsstrategie in Wirbellosen weit verbreitet ist.
Zwei Modi, vom Kalium umgeschaltet
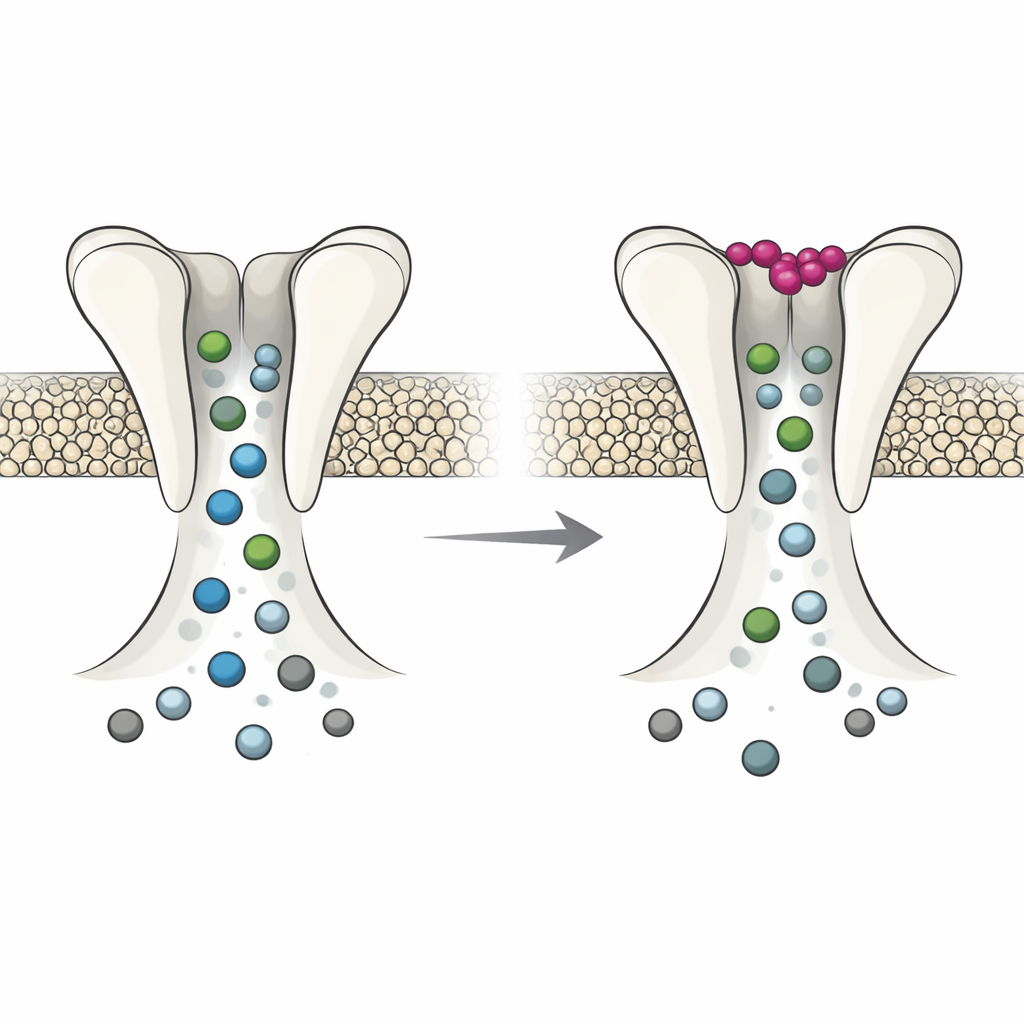
Elektrophysiologische Experimente in Froscheiern, die als Miniaturfabriken zur Herstellung von Kanälen dienen können, zeigten, dass sich DmAlka wie ein Schalter mit zwei Modi verhält. Wenn das extrazelluläre Kalium niedrig ist, bleibt der Kanal wahrscheinlicher offen, reagiert anders auf alkalische Bedingungen und desensibilisiert sich im Zeitverlauf weniger. In diesem Modus ist die Pore relativ weit: Sie bevorzugt Chlorid, lässt aber auch andere negative Ionen wie Bicarbonat freier passieren und wird weniger leicht von bestimmten Medikamenten blockiert. Bindet Kalium an seine spezielle Stelle, verschiebt sich das gesamte Protein subtil. Die Pore verengt sich und wird selektiver für Chlorid, leitet andere Anionen schlechter und zeigt eine stärkere Reaktion auf porenblockierende Moleküle. Effektiv schaltet extrazelluläres Kalium den Kanal zwischen einem flexiblen, breit permeablen Zustand und einem engeren, mehr auf Chlorid fokussierten Zustand um.
Widerhall im menschlichen Gehirn
Interessanterweise scheint derselbe grundlegende Mechanismus zumindest in latenter Form auch beim Menschen vorhanden zu sein. Ein menschlicher Glycinrezeptor‑Subtyp, GlyR α2, reagiert normalerweise auf den Neurotransmitter Glycin und nicht auf Kalium. Indem die Autoren Schlüsselfunktionen der DmAlka‑Kaliumtasche in den menschlichen Rezeptor transplantierten, erzeugten sie ein Mutant, das Kaliumempfindlichkeit erwarb: Hohes externes Kalium verstärkte die Basisströme sogar ohne vorhandenes Glycin. Sie zeigten auch, dass natürlich vorkommende menschliche Varianten von GlyR α2, einige in Verbindung mit epilepsy‑assoziierten Veränderungen im Gehirn, Kaliumantworten annehmen können. In diesen menschlichen Rezeptoren verschiebt Kaliumbindung wie bei DmAlka die Poreneigenschaften, verändert die Leitfähigkeit für Chlorid und Bicarbonat und die Wirksamkeit bestimmter Blocker.
Warum das für die Gehirngesundheit wichtig ist
Die Fruchtfliegen‑Version dieses Kanals ist in Gliazellen angereichert, den Stützzellen, die helfen, Kalium‑Gleichgewicht und pH‑Wert um Neurone herum aufrechtzuerhalten. Der neu entdeckte Mechanismus legt eine einfache Logik nahe: Wenn das extrazelluläre Kalium sinkt, öffnet sich DmAlka so, dass mehr Chlorid in die Glia einströmt und mehr Bicarbonat austritt, was möglicherweise sowohl zum Wiederherstellen der Kaliumwerte als auch der Säurebedingungen im umgebenden Raum beiträgt. Beim Menschen könnte ähnliches kaliumabgestimmtes Verhalten in Glycinrezeptoren unter extremen Bedingungen — etwa Schlaganfall oder epileptischen Anfällen, wenn das extrazelluläre Kalium weit über das Normale ansteigt — bedeutsam werden. Insgesamt zeigt diese Arbeit, dass einige Cys‑Loop‑Rezeptoren nicht nur passive Reagierer auf Neurotransmitter sind; sie können auch direkte Sensoren der ionischen Umgebung sein und Veränderungen des extrazellulären Kaliums mit Verschiebungen der Chlorid‑Signalgebung über Arten hinweg verknüpfen.
Zitation: Shimomura, T., Kubo, Y., Saitoe, M. et al. Extracellular K+ modulates the pore conformations of Cys-loop receptor anion channels. Nat Commun 17, 3453 (2026). https://doi.org/10.1038/s41467-026-71629-z
Schlüsselwörter: extrazelluläre Kaliumwahrnehmung, Chloridkanäle, Cys‑Loop‑Rezeptoren, Glycinrezeptor‑Varianten, gliale Ionenhomöostase