Clear Sky Science · zh
通过非镶嵌性破坏 OTOF 基因生成的绒猴用于模拟人类耳聋
为何小型灵长类对听力研究至关重要
由基因缺陷引起的听力损失很常见,对于一个重要基因 OTOF,针对儿童的基因治疗已开始进入临床探索。然而,科学家仍缺乏一个能够与人类耳朵高度相似的动物模型,用来检验这些疗法的安全性、精确度和持久性。本研究正是为此而来:构建了一系小型绒猴,使其表现出许多儿童所见的同类型耳聋,为从小鼠实验向人类临床试验搭建了一座强有力的桥梁。 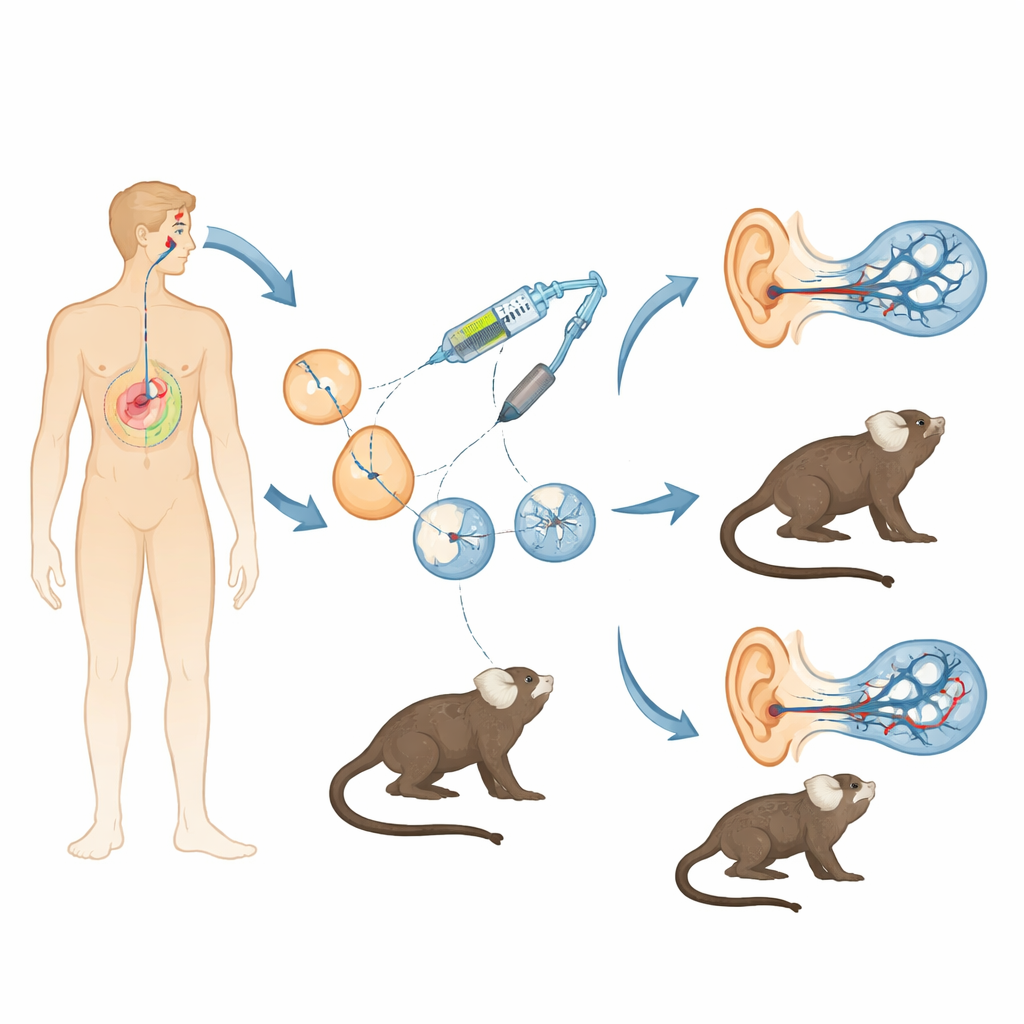
沉默突触构成耳聋的核心
许多与 OTOF 相关的耳聋患者外耳看起来正常,外毛细胞对声音的反应也可能存在。问题出在更深层次:内耳蜗中内毛细胞将声音信息传递给听觉神经的微观突触处。OTOF 基因编码一种名为 otoferlin 的蛋白,这种蛋白对于在突触处释放微小的化学信号颗粒至关重要。当 otoferlin 缺失时,声音信号无法被有效转递,这种情况称为听觉突触病变。由于耳朵的其余结构在多年内可能保持健康,这种类型的耳聋尤其适合一次性基因疗法来恢复缺失的 otoferlin。
构建人类耳聋的灵长类模型
小鼠在听力研究中非常有价值,但在基因、发育和听力发作时间上与人类存在关键差异。相比之下,绒猴是体型小的非人灵长类,与人类共享更多 DNA,胎内已开始听觉,并拥有丰富的社交声带交流。研究人员将体外受精与 CRISPR/Cas9 基因编辑系统结合,破坏了绒猴 OTOF 基因的关键外显子。通过在早期胚胎中注入精心优化的 CRISPR 组分混合物,他们力求在两个等位基因上删除该片段,同时避免灵长类编辑中的一大难题:镶嵌性——即同一动物不同细胞带有不同突变。在经过多轮卵母细胞采集、受精和将胚胎移植到代孕母体后,他们获得了两只存活的、具有双等位基因且非镶嵌性的 OTOF 破坏绒猴——即每个细胞都带有预期的敲除突变。
检测听力、脑电信号与行为
为确定这些基因改造的绒猴是否真正模拟人类病情,研究团队从六个月大开始对其听力进行测试。来自脑干的电生理记录——通常在声音到达听觉通路时显示清晰波形——在敲除动物中即便在极高声压下也呈现平坦波形。与此同时,外毛细胞产生的耳声发射测试(微小回声)在敲除体与正常体之间都很强且相似。这种脑响应缺失但耳蜗力学功能保留的组合,恰与人类 OTOF 相关的听觉突触病变高度吻合。对一只动物内耳的显微检查证实,内毛细胞存在但缺少 otoferlin 蛋白,而整体耳蜗结构保持完整。 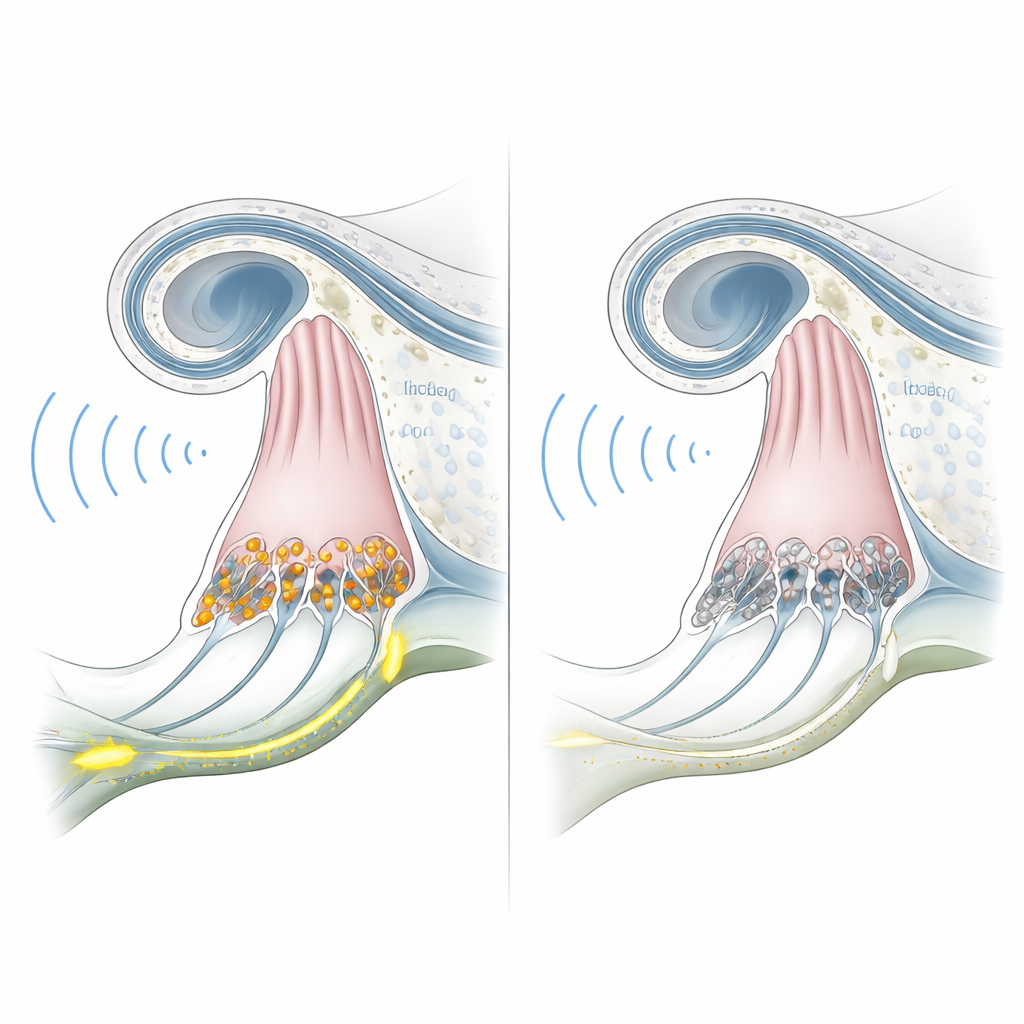
有声却无法听见
由于绒猴以话多著称,研究者还考察了耳聋如何影响早期发声发育。当婴猴短暂与家人分开录音时,正常与敲除个体都发出了数千次呼叫,包含健康婴猴通常产生的所有主要呼叫类型。呼叫频率在两组间相似,这表明发声的基本驱动力和曲目在早期大体是先天形成的,并不完全依赖听力。然而,进一步的细致分析显示,敲除个体中最长的呼叫类型随年龄增长的延长幅度不及有听力的个体,提示听觉反馈仍会随时间塑造发声成熟的细微方面。这些微妙差异使该模型不仅对听力研究有价值,也有助于理解声音经验如何雕塑交流行为。
通向更好听力治疗的新路径
通过产生具有清晰非镶嵌性 OTOF 基因敲除的绒猴,这项工作提供了一个与人类遗传性耳聋高度一致的灵长类模型。动物表现出听觉突触病变的标志性特征:外耳力学正常、内毛细胞缺失 otoferlin、以及无法将声音信息传递到大脑。该模型将使研究人员能够微调基因治疗策略——测试不同的病毒载体、剂量与给药时机,并将长期听力结局与耳内 otoferlin 恢复的精确测量相联系。尽管构建此类灵长类模型过程缓慢、费用高昂且在伦理上要求严格,作者认为,为患有遗传性耳聋的儿童改进改变生活的疗法的潜力,使这种经过严谨控制的方法在科学和医学上都具有重要价值。
引用: Kahland, T., Lindenwald, D.L., Jeschke, M. et al. Generation of marmoset monkeys with a non-mosaic disruption of the OTOF gene as a model of human deafness. Nat Commun 17, 3033 (2026). https://doi.org/10.1038/s41467-026-71047-1
关键词: 遗传性耳聋, 绒猴模型, 基因疗法, 听觉突触病变, CRISPR 编辑