Clear Sky Science · it
Generazione di marmoset con una disruzione non-mosaica del gene OTOF come modello della sordità umana
Perché i piccoli primati sono importanti per la perdita dell'udito
La perdita dell'udito dovuta a geni difettosi è comune, e per un gene importante chiamato OTOF la terapia genica nei bambini è già cominciata. Tuttavia agli scienziati manca ancora un modello animale che rispecchi da vicino l'orecchio umano per valutare quanto siano sicuri, precisi e duraturi tali trattamenti. Questo studio crea proprio questo: una linea di piccoli marmoset ingegnerizzati per manifestare lo stesso tipo di sordità osservata in molti bambini, offrendo un ponte potente tra gli esperimenti nei topi e le sperimentazioni cliniche umane. 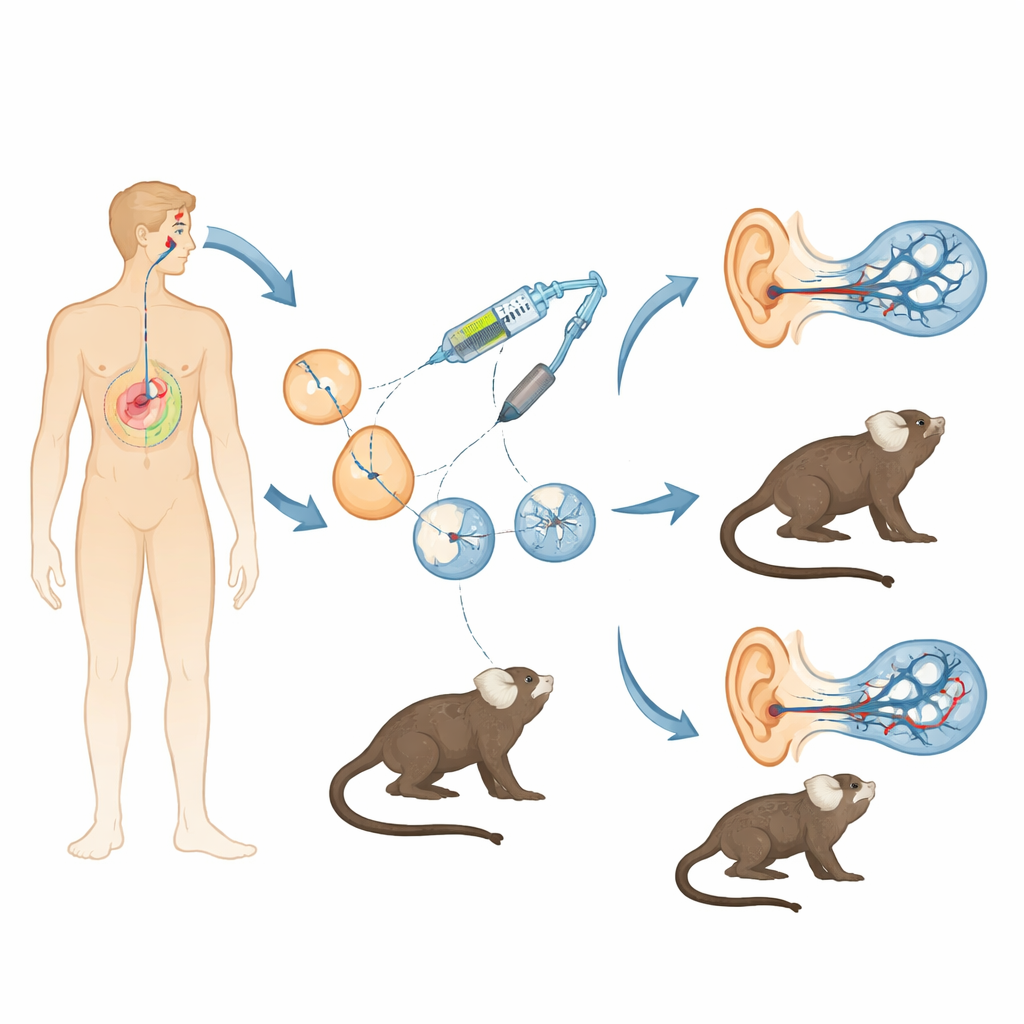
Una sinapsi silenziosa al centro della sordità
Molte persone con sordità legata a OTOF hanno orecchie dall'aspetto normale e persino cellule dell'orecchio esterno che rispondono ancora ai suoni. Il problema è più profondo, nelle giunzioni microscopiche in cui le cellule ciliate interne della coclea trasmettono l'informazione sonora al nervo dell'udito. Il gene OTOF fornisce il progetto per una proteina chiamata otoferlin, cruciale per il rilascio di minuscoli pacchetti di segnali chimici a queste sinapsi. Quando l'otoferlin manca, il segnale sonoro semplicemente non viene trasmesso, una condizione nota come sinaptopatia uditiva. Poiché il resto dell'orecchio può rimanere strutturalmente sano per anni, questa forma di sordità è particolarmente promettente per terapie geniche una tantum volte a ripristinare l'otoferlin mancante.
Progettare un modello primate della sordità umana
I topi sono stati preziosi per comprendere l'udito, ma i loro geni, lo sviluppo e l'inizio dell'udito differiscono in modi chiave rispetto ai nostri. I marmoset, al contrario, sono piccoli primati non umani che condividono più del nostro DNA, iniziano a sentire prima della nascita e possiedono una ricca comunicazione vocale sociale. I ricercatori hanno combinato la fecondazione in vitro con il sistema di editing genico CRISPR/Cas9 per interrompere un esone cruciale del gene OTOF del marmoset. Iniettando miscele attentamente ottimizzate dei componenti CRISPR negli embrioni precoci, hanno cercato di eliminare questo segmento in entrambe le copie del gene evitando un insidioso problema nell'editing dei primati: il mosaicismo, in cui cellule diverse dello stesso animale presentano mutazioni differenti. Dopo molteplici cicli di raccolta di ovociti, fecondazione e trasferimento embrionale in madri surrogate, hanno ottenuto due scimmiette sopravvissute con disruzioni bialleliche e non-mosaiche di OTOF—ovvero ogni cellula presentava l'annullamento voluto.
Verificare l'udito, i segnali cerebrali e il comportamento
Per capire se questi marmoset ingegnerizzati rispecchiassero veramente la condizione umana, il team ha testato il loro udito a partire dai sei mesi di età. Le registrazioni elettriche dal tronco encefalico, che normalmente mostrano onde chiare quando il suono raggiunge la via uditiva, erano piatte anche a livelli sonori molto intensi negli animali knockout. Allo stesso tempo, i test delle emissioni otoacustiche—piccoli echi generati dalle cellule ciliate esterne—erano robusti e simili a quelli dei marmoset normali. Questa combinazione di risposte cerebrali assenti ma meccanica cocleare preservata corrisponde da vicino alla sinaptopatia uditiva umana legata a OTOF. L'esame microscopico dell'orecchio interno di un animale ha confermato che le cellule ciliate interne erano presenti ma prive della proteina otoferlin, mentre la struttura cocleare complessiva restava intatta. 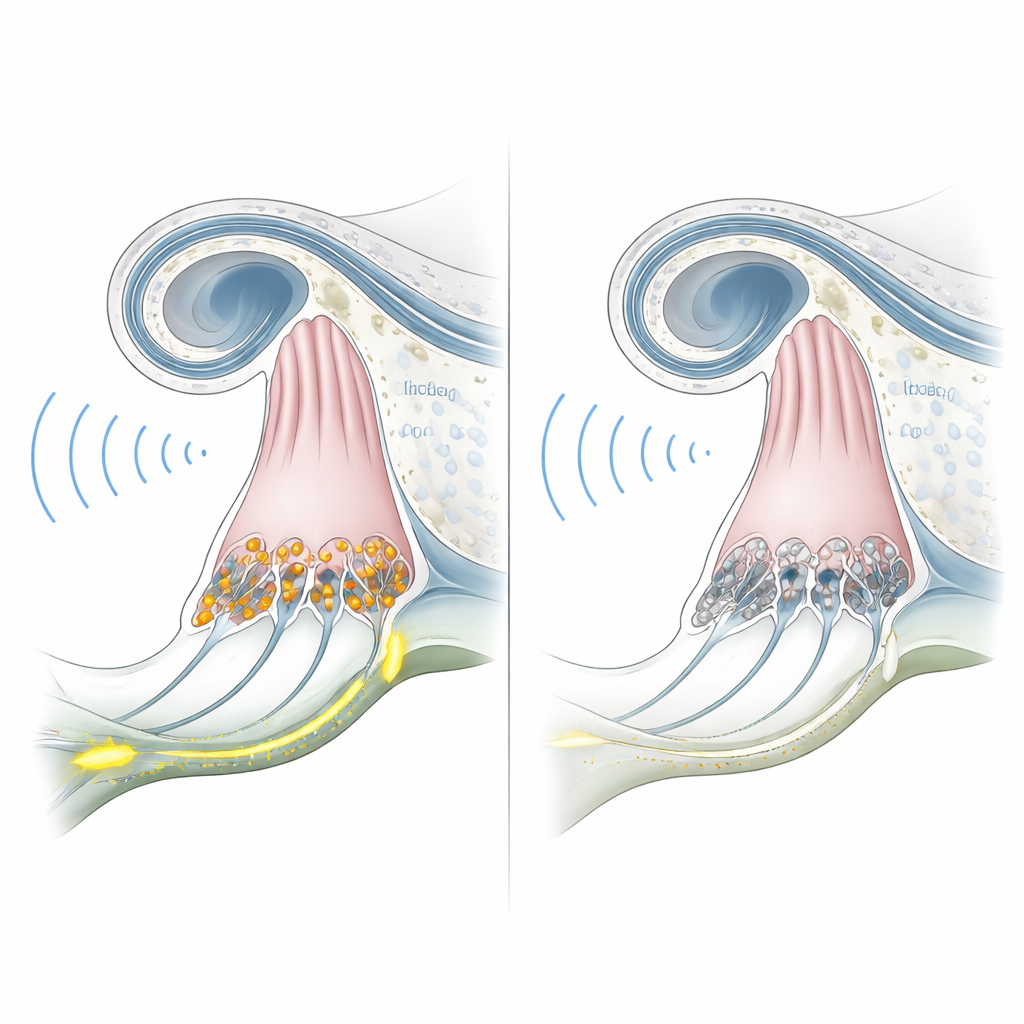
Voci senza udito
Poiché i marmoset sono famosi per la loro loquacità, gli scienziati hanno anche indagato come la sordità influenzi lo sviluppo vocale precoce. Quando i cuccioli sono stati brevemente registrati lontano dalla famiglia, sia i marmoset normali sia quelli knockout hanno prodotto migliaia di richiami, includendo tutti i principali tipi di vocalizzazione che i cuccioli sani emettono di solito. I tassi di emissione erano simili tra i gruppi, suggerendo che l'impulso di base e il repertorio delle vocalizzazioni sono in gran parte innati e non richiedono l'udito, almeno nelle prime fasi di vita. Tuttavia, un'analisi più dettagliata ha rivelato che i tipi di richiami più lunghi non si allungavano con l'età altrettanto nei soggetti sordi quanto in quelli udenti, suggerendo che il feedback uditivo modella comunque aspetti più fini della maturazione vocale nel tempo. Queste differenze sottili rendono il modello prezioso non solo per la ricerca sull'udito ma anche per comprendere come l'esperienza sonora plasmi la comunicazione.
Nuove strade verso trattamenti migliori per l'udito
Producendo marmoset con un knockout pulito e non-mosaico del gene OTOF, questo lavoro fornisce un modello primate che rispecchia da vicino una forma umana di sordità ereditaria. Gli animali mostrano le caratteristiche distintive della sinaptopatia uditiva: meccanica dell'orecchio esterno normale, assenza di otoferlin nelle cellule ciliate interne e incapacità di trasmettere le informazioni sonore al cervello. Questo modello permetterà ai ricercatori di affinare le strategie di terapia genica—testando diversi sistemi virali di veicolazione, dosi e tempistiche, e collegando gli esiti uditivi a lungo termine a misurazioni precise del ripristino di otoferlin nell'orecchio interno. Sebbene creare tali modelli primati sia lento, costoso e eticamente impegnativo, gli autori sostengono che il potenziale di migliorare terapie che cambiano la vita per i bambini con sordità genetica rende questo approccio attentamente controllato sia scientificamente che medicamente valido.
Citazione: Kahland, T., Lindenwald, D.L., Jeschke, M. et al. Generation of marmoset monkeys with a non-mosaic disruption of the OTOF gene as a model of human deafness. Nat Commun 17, 3033 (2026). https://doi.org/10.1038/s41467-026-71047-1
Parole chiave: sordità genetica, modello marmoset, terapia genica, sinaptopatia uditiva, editing CRISPR