Clear Sky Science · pl
Generowanie makaków karłowatych z niemozajkowym zaburzeniem genu OTOF jako model głuchoty u ludzi
Dlaczego małe małpki mają znaczenie dla badań nad utratą słuchu
Utrata słuchu wywołana wadliwymi genami jest powszechna, a dla jednego z istotnych genów o nazwie OTOF terapie genowe u dzieci już się rozpoczynają. Naukowcom nadal jednak brakuje modelu zwierzęcego, który wiernie odzwierciedlałby ludzki ustrój słuchowy, by testować, jak bezpieczne, precyzyjne i trwałe są takie terapie. To badanie tworzy właśnie taki model: linię małych małpek koczkodanów karłowatych zmodyfikowanych tak, by miały ten sam typ głuchoty spotykany u wielu dzieci, stanowiąc potężne ogniwo łączące eksperymenty na myszach z badaniami klinicznymi u ludzi. 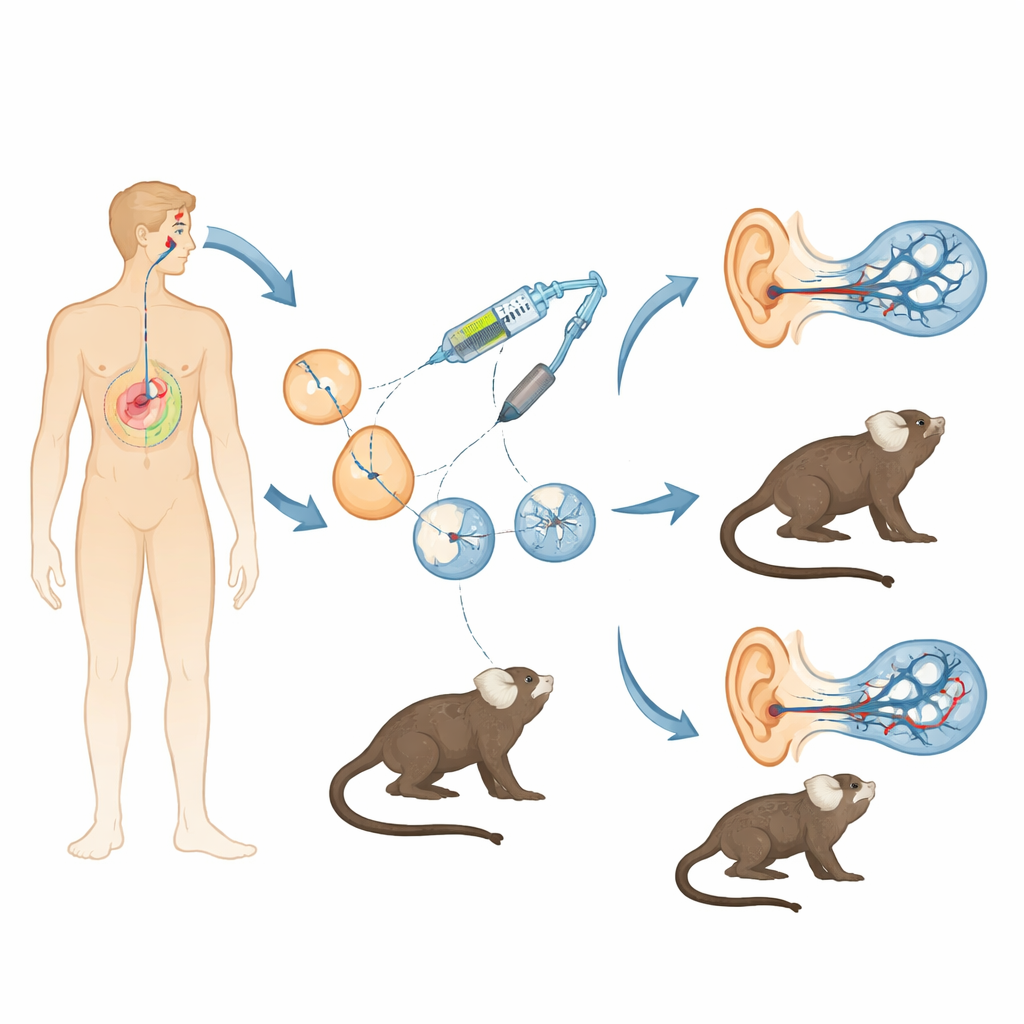
Ciche synapsy w sercu głuchoty
Wiele osób z głuchotą związaną z OTOF ma ucho o wyglądzie zewnętrznym prawidłowym, a nawet komórki zewnętrzne ucha, które nadal reagują na dźwięk. Problem leży głębiej, w mikroskopijnych połączeniach, gdzie komórki zmysłowe wewnętrzne w ślimaku przekazują informacje dźwiękowe do nerwu słuchowego. Gen OTOF zawiera instrukcję dla białka zwanego otoferliną, które jest kluczowe dla uwalniania maleńkich pęcherzyków z mediatorami na tych synapsach. Gdy otoferliny brakuje, sygnał dźwiękowy po prostu nie jest przekazywany — stan znany jako synaptopatia słuchowa. Ponieważ reszta ucha może przez lata pozostawać strukturalnie zdrowa, ta forma głuchoty jest szczególnie obiecująca dla jednorazowych terapii genowych mających na celu przywrócenie brakującej otoferliny.
Inżynieria modelu prymata odzwierciedlającego ludzką głuchotę
Myszy były nieocenione dla zrozumienia słuchu, lecz ich geny, rozwój i moment pojawienia się słyszenia różnią się w istotny sposób od naszych. Koczkodany karłowate, w przeciwieństwie do nich, to małe naczelne, które dzielą z nami więcej DNA, zaczynają słyszeć przed narodzinami i mają bogatą społeczną komunikację wokalną. Badacze połączyli zapłodnienie in vitro z systemem edycji genów CRISPR/Cas9, aby zaburzyć istotny egzON w genie OTOF marmoseta. Poprzez wstrzyknięcie starannie zoptymalizowanych mieszanek składników CRISPR do wczesnych embrionów, dążyli do usunięcia tego fragmentu w obu kopiach genu, jednocześnie unikając poważnego problemu przy edycji prymatów: mozaicyzmu, czyli sytuacji, w której różne komórki tego samego zwierzęcia niosą różne mutacje. Po wielu cyklach pobierania oocytów, zapłodnień i przesadzeń embrionów do matek zastępczych uzyskali dwoje przeżyłych małp z biallelicznymi, niemozajkowymi uszkodzeniami OTOF — co znaczy, że każda komórka nosiła zamierzony knockout.
Sprawdzanie słuchu, sygnałów mózgowych i zachowania
Aby ustalić, czy te zmodyfikowane małpy rzeczywiście odzwierciedlają ludzki stan, zespół badał ich słuch zaczynając od sześciu miesięcy życia. Rejestracje elektryczne ze wzgórka mózgu, które normalnie ukazują wyraźne fale, gdy dźwięk dociera do drogi słuchowej, były płaskie nawet przy bardzo głośnych poziomach dźwięku u zwierząt z knockoutem. Jednocześnie badania emisji otoakustycznych — maleńkich echo generowanych przez komórki zewnętrzne ślimaka — były silne i podobne do obserwowanych u normalnych małp. To połączenie nieobecnych odpowiedzi mózgowych przy zachowanej mechanice ślimaka ściśle odpowiada ludzkiej synaptopatii związanej z OTOF. Badanie mikroskopowe ucha wewnętrznego jednego osobnika potwierdziło, że komórki zmysłowe wewnętrzne były obecne, ale pozbawione białka otoferliny, podczas gdy ogólna struktura ślimaka pozostała nienaruszona. 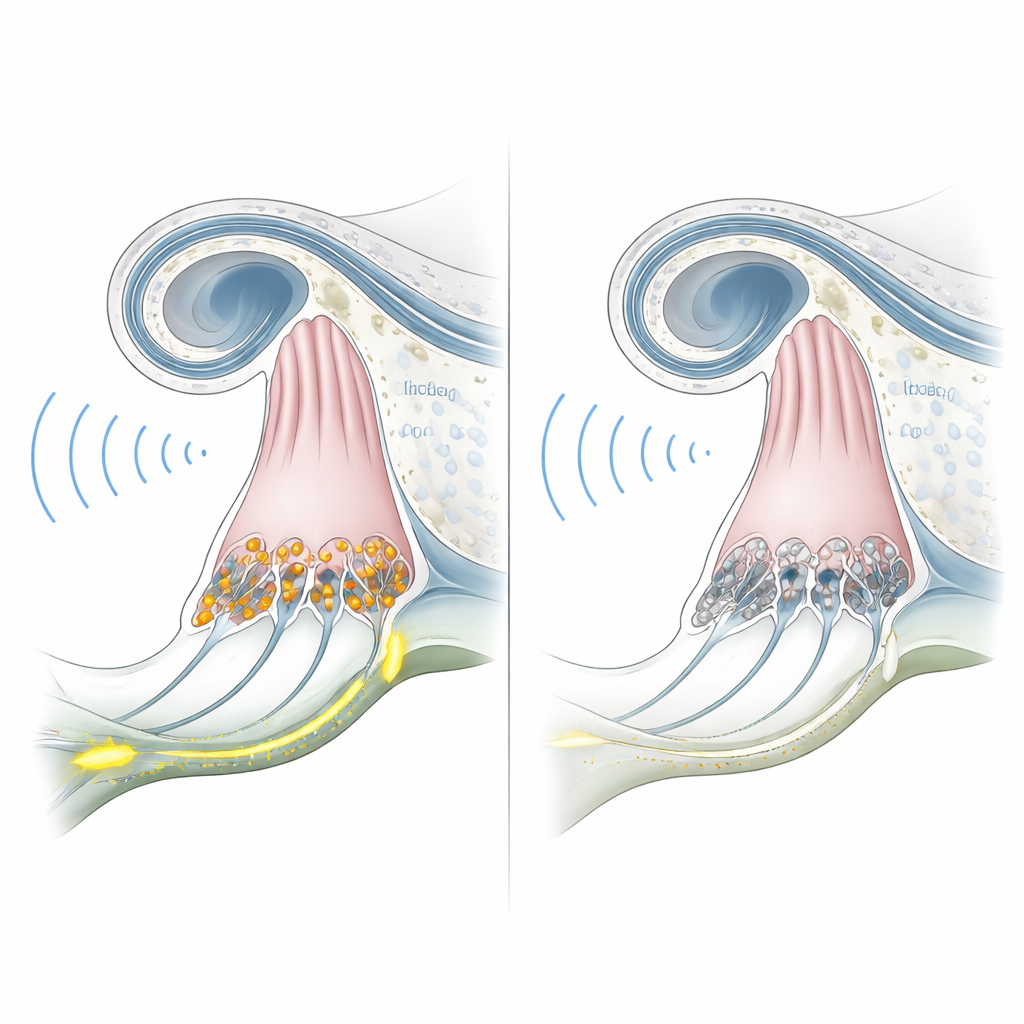
Głosy bez słyszenia
Ponieważ koczkodany karłowate słyną z gadatliwości, naukowcy zapytali także, jak głuchota wpływa na wczesny rozwój wokalny. Gdy nagrywano niemowlęta krótko oddzielone od rodzin, zarówno normalne, jak i knockoutowe małpy wydawały tysiące odgłosów, obejmujących wszystkie główne typy wołań, które zdrowe młode zwykle emitują. Częstotliwość wołań była podobna w obu grupach, co sugeruje, że podstawowy napęd i repertuar wokalizacji są w dużej mierze wrodzone i przynajmniej we wczesnym życiu nie wymagają słyszenia. Jednak bardziej szczegółowa analiza wykazała, że najdłuższe typy wołań u zwierząt głuchych nie wydłużały się z wiekiem tak bardzo jak u słyszących, co sugeruje, że sprzężenie zwrotne słuchowe wpływa na drobniejsze aspekty dojrzewania wokalnego w czasie. Te subtelne różnice czynią model cennym nie tylko dla badań nad słuchem, lecz również dla zrozumienia, jak doświadczenie dźwiękowe kształtuje komunikację.
Nowe drogi ku lepszym terapiom słuchu
Poprzez wytworzenie marmosetów z czystym, niemozajkowym knockoutem genu OTOF, ta praca dostarcza model prymata, który ściśle odwzorowuje jedną z form dziedzicznej głuchoty u ludzi. Zwierzęta wykazują charakterystyczne cechy synaptopatii słuchowej: prawidłową mechanikę ucha zewnętrznego, brak otoferliny w komórkach wewnętrznych oraz niezdolność do przekazywania informacji dźwiękowej do mózgu. Model pozwoli badaczom dopracować strategie terapii genowej — testując różne systemy dostarczania wirusowego, dawki i czas podania oraz wiążąc długoterminowe wyniki słuchowe z precyzyjnymi pomiarami odbudowy otoferliny w uchu wewnętrznym. Chociaż tworzenie takich modeli prymatów jest powolne, kosztowne i stawia wysokie wymagania etyczne, autorzy argumentują, że potencjał poprawy terapii zmieniających życie dzieci z genetyczną głuchotą sprawia, iż to ostrożnie kontrolowane podejście jest zarówno naukowo, jak i medycznie uzasadnione.
Cytowanie: Kahland, T., Lindenwald, D.L., Jeschke, M. et al. Generation of marmoset monkeys with a non-mosaic disruption of the OTOF gene as a model of human deafness. Nat Commun 17, 3033 (2026). https://doi.org/10.1038/s41467-026-71047-1
Słowa kluczowe: genetyczna głuchota, model koczkodanów karłowatych, terapia genowa, synaptopatia słuchowa, edytowanie CRISPR