Clear Sky Science · fr
Génération de singes marmosets avec une perturbation non mosaïque du gène OTOF comme modèle de la surdité humaine
Pourquoi les petits singes comptent pour la perte auditive
La perte auditive d’origine génétique est fréquente, et pour un gène important appelé OTOF, des essais de thérapie génique chez l’enfant ont déjà commencé. Pourtant, les chercheurs manquent encore d’un modèle animal qui reflète fidèlement l’oreille humaine pour tester la sécurité, la précision et la durabilité de ces traitements. Cette étude crée précisément un tel modèle : une lignée de petits marmosets génétiquement modifiés pour présenter le même type de surdité observé chez de nombreux enfants, offrant un lien puissant entre les expériences sur souris et les essais cliniques humains. 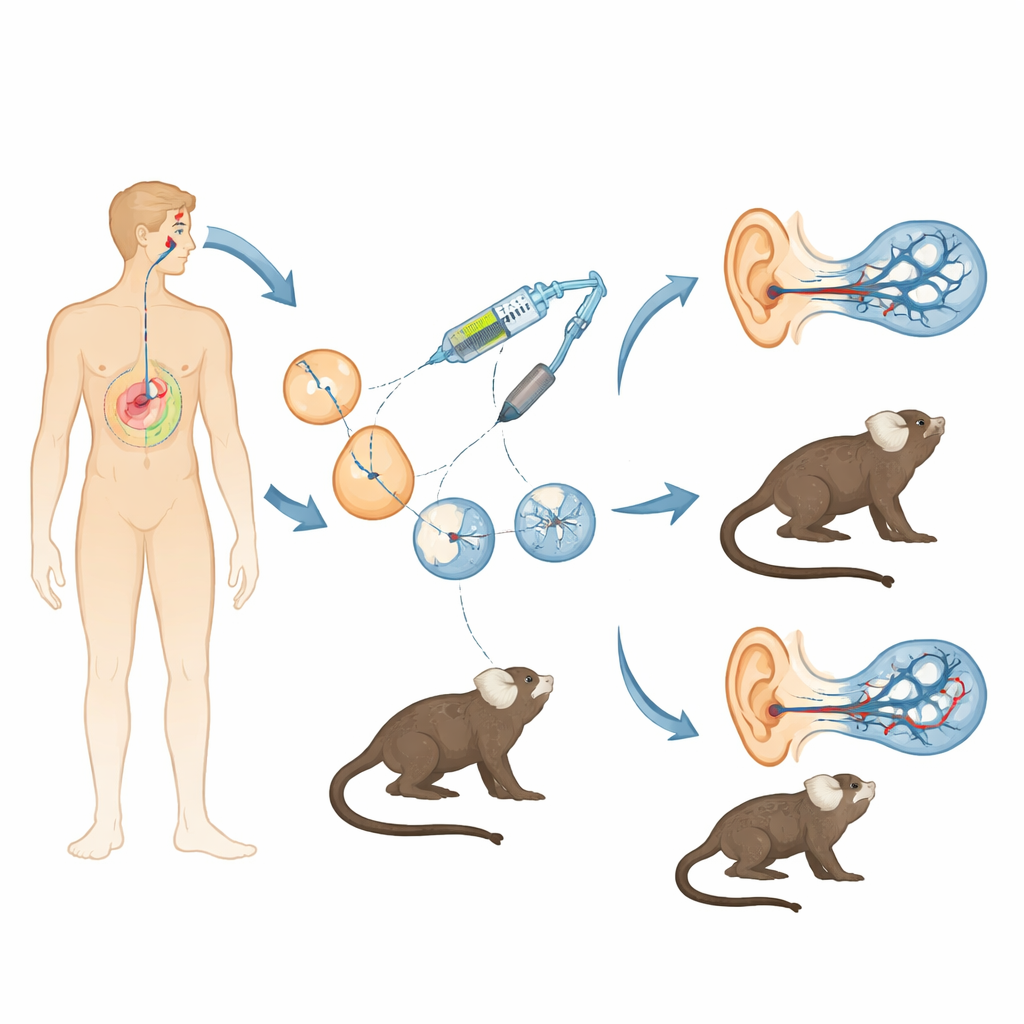
Une synapse silencieuse au cœur de la surdité
Beaucoup de personnes atteintes d’une surdité liée à OTOF ont des oreilles d’apparence normale et même des cellules de l’oreille externe qui répondent encore au son. Le problème se situe plus profondément, aux jonctions microscopiques où les cellules ciliées internes de la cochlée transmettent l’information sonore au nerf auditif. Le gène OTOF code pour une protéine appelée otoferline, essentielle à la libération de petites vésicules de neurotransmetteurs à ces synapses. En l’absence d’otoferline, le signal sonore n’est tout simplement pas relayé, une condition appelée synaptopathie auditive. Comme le reste de l’oreille peut rester structurellement sain pendant des années, cette forme de surdité est particulièrement prometteuse pour des thérapies géniques en une seule administration visant à restaurer l’otoferline manquante.
Concevoir un modèle primate de la surdité humaine
Les souris ont été précieuses pour comprendre l’audition, mais leurs gènes, leur développement et le moment d’apparition de l’audition diffèrent de façon importante des nôtres. Les marmosets, en revanche, sont de petits primates non humains qui partagent davantage notre ADN, entendent avant la naissance et disposent d’une communication vocale sociale riche. Les chercheurs ont combiné la fécondation in vitro avec le système d’édition génomique CRISPR/Cas9 pour perturber un exon crucial du gène OTOF du marmoset. En injectant des mélanges optimisés de composants CRISPR dans des embryons précoces, ils ont cherché à supprimer ce segment sur les deux copies du gène tout en évitant un écueil majeur de l’édition chez les primates : le mosaïcisme, où différentes cellules du même animal portent des mutations différentes. Après de nombreux cycles de collecte d’ovocytes, de fécondation et de transfert d’embryons chez des mères porteuses, ils ont obtenu deux singes survivants présentant des perturbations bialléliques et non mosaïques d’OTOF — c’est‑à‑dire que chaque cellule portait l’inactivation voulue.
Vérifier l’audition, les signaux cérébraux et le comportement
Pour savoir si ces singes modifiés reproduisaient vraiment l’affection humaine, l’équipe a testé leur audition à partir de six mois. Les enregistrements électriques du tronc cérébral, qui montrent normalement des ondes claires lorsque le son atteint la voie auditive, étaient plats même à des niveaux sonores très élevés chez les animaux knockouts. Parallèlement, les tests d’émissions otoacoustiques — de minuscules échos générés par les cellules ciliées externes — étaient robustes et similaires à ceux des singes normaux. Cette combinaison d’absence de réponses cérébrales mais de mécanique cochléaire préservée correspond étroitement à la synaptopathie auditive liée à OTOF chez l’humain. L’examen microscopique des oreilles internes d’un animal a confirmé que les cellules ciliées internes étaient présentes mais dépourvues de la protéine otoferline, tandis que la structure cochléaire globale restait intacte. 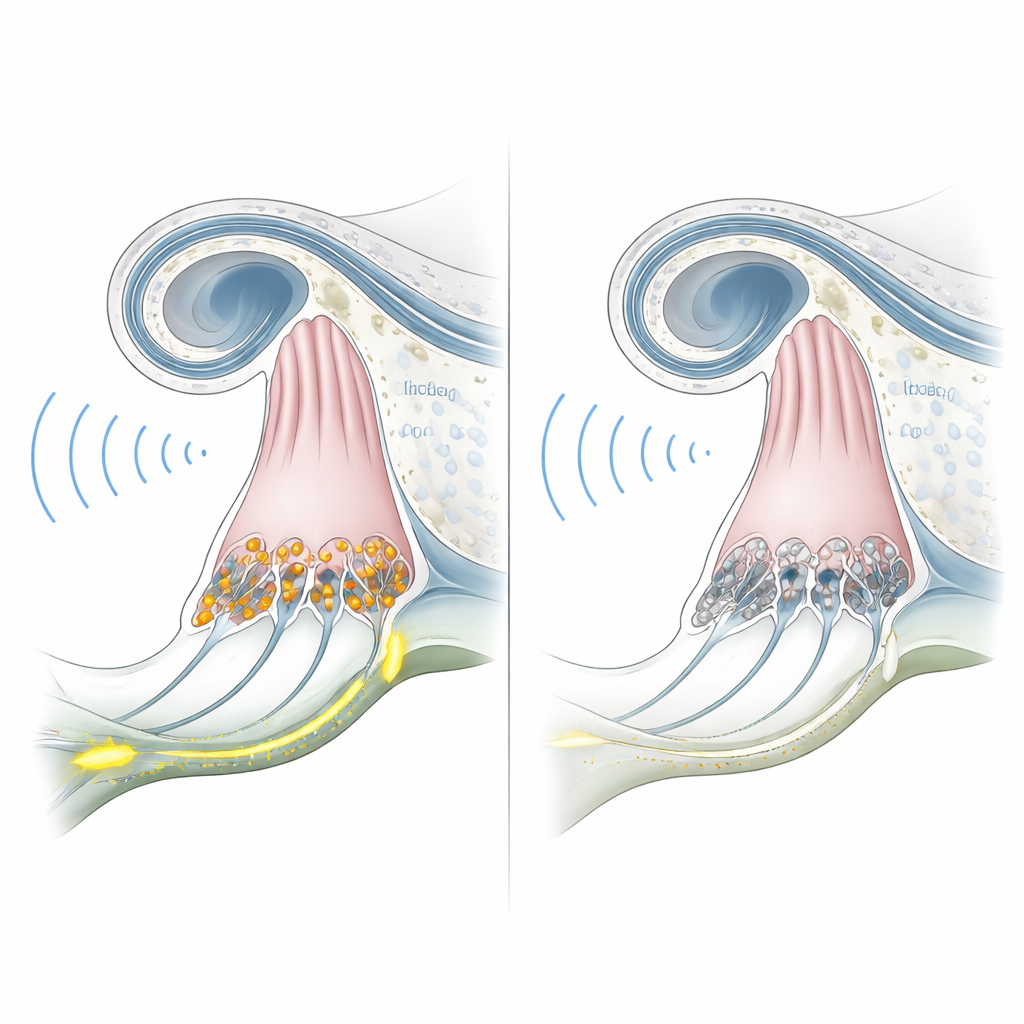
Des voix sans audition
Puisque les marmosets sont réputés pour leur loquacité, les scientifiques ont également étudié l’impact de la surdité sur le développement précoce des vocalisations. Lors d’enregistrements brefs loin de leur famille, aussi bien les singes normaux que les knockouts ont produit des milliers d’appels, incluant tous les types d’appels majeurs que les jeunes sains émettent habituellement. Les taux d’appels étaient similaires entre les groupes, ce qui suggère que la poussée et le répertoire de base des vocalisations sont largement innés et ne nécessitent pas l’audition, du moins au début de la vie. Toutefois, une analyse plus fine a révélé que les types d’appels les plus longs ne s’allongeaient pas autant avec l’âge chez les animaux sourds que chez les entendants, laissant entendre que le retour auditif module quand même des aspects plus subtils de la maturation vocale au fil du temps. Ces différences subtiles rendent le modèle utile non seulement pour la recherche sur l’audition, mais aussi pour comprendre comment l’expérience sonore façonne la communication.
Nouvelles voies vers de meilleurs traitements auditifs
En produisant des marmosets avec une inactivation propre et non mosaïque du gène OTOF, ce travail fournit un modèle primate qui reproduit fidèlement une forme humaine de surdité héréditaire. Les animaux présentent les caractéristiques emblématiques de la synaptopathie auditive : mécanique normale de l’oreille externe, absence d’otoferline dans les cellules ciliées internes et incapacité à transmettre l’information sonore au cerveau. Ce modèle permettra aux chercheurs d’affiner les stratégies de thérapie génique — tester différents vecteurs viraux, doses et fenêtres temporelles — et de relier les résultats auditifs à long terme à des mesures précises de restauration d’otoferline dans l’oreille interne. Bien que la création de tels modèles primates soit lente, coûteuse et exige des considérations éthiques strictes, les auteurs soutiennent que le potentiel d’améliorer des thérapies qui changent la vie des enfants atteints de surdité génétique rend cette approche soigneusement contrôlée à la fois scientifiquement et médicalement justifiée.
Citation: Kahland, T., Lindenwald, D.L., Jeschke, M. et al. Generation of marmoset monkeys with a non-mosaic disruption of the OTOF gene as a model of human deafness. Nat Commun 17, 3033 (2026). https://doi.org/10.1038/s41467-026-71047-1
Mots-clés: surdité génétique, modèle marmoset, thérapie génique, synaptopathie auditive, édition CRISPR