Clear Sky Science · ar
توليد قرود المارسوت الصغيرة مع تعطيل غير فسيفسائي لجين OTOF كنموذج للصمم البشري
لماذا تهم القرود الصغيرة في دراسة فقدان السمع
الصمم الناتج عن جينات معطوبة شائع، ولمجموعة جينية مهمة تُدعى OTOF، بدأ بالفعل تطبيق العلاج الجيني لدى الأطفال. ومع ذلك يفتقر العلماء إلى نموذج حيواني يحاكي أذن الإنسان عن قرب لاختبار مدى أمان ودقة وطول أثر هذه العلاجات. تقوم هذه الدراسة بملء هذه الفجوة: فقد أنشأ الباحثون سلالة من قرود المارسوت الصغيرة المهندَسة بحيث تحمل نفس نوع الصمم الذي يُرى لدى العديد من الأطفال، مما يوفر جسرًا قويًا بين تجارب الفئران والتجارب السريرية البشرية. 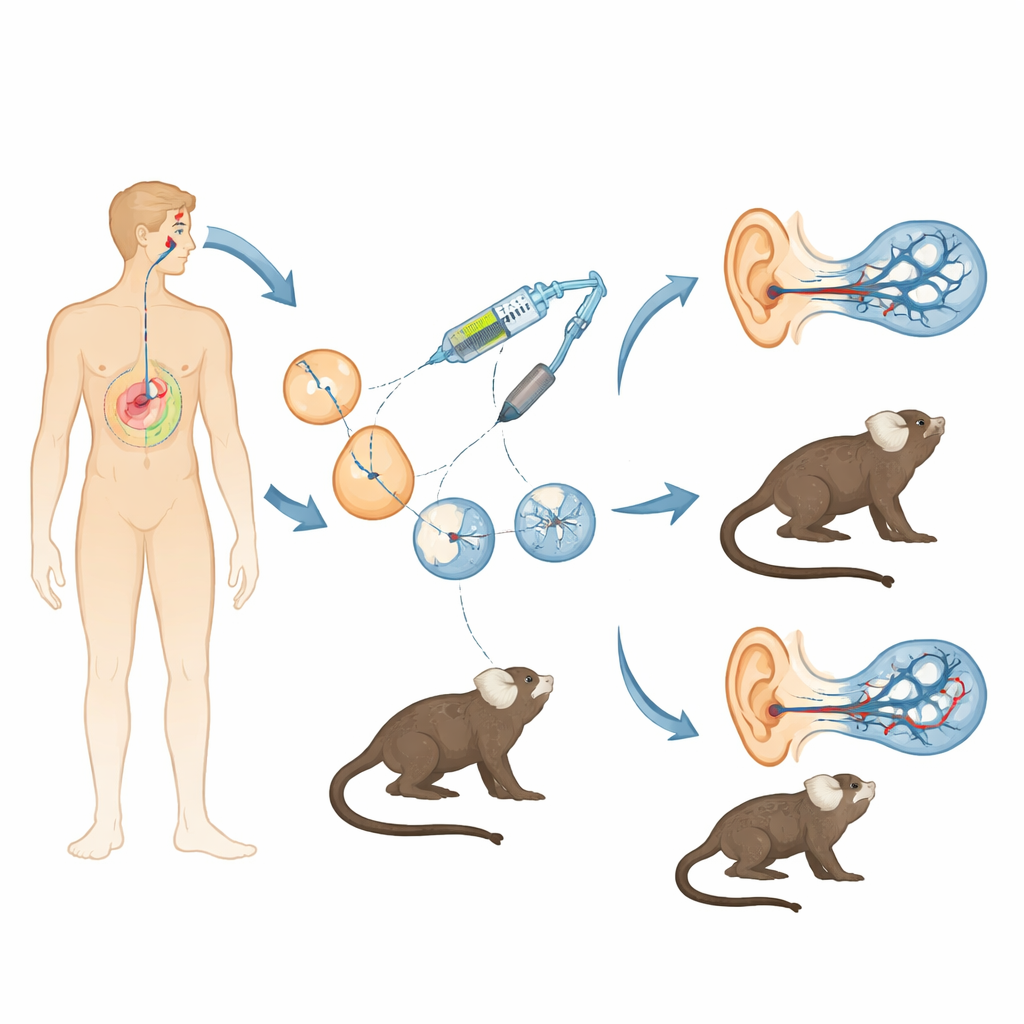
المشبك الصامت في صميم الصمم
يعاني كثير من الأشخاص المصابين بصمم مرتبط بـ OTOF من آذان تبدو طبيعية وحتى خلايا الأذن الخارجية التي لا تزال تستجيب للصوت. المشكلة تكمن أبعد في الوصلات المجهرية حيث تنقل خلايا الشعر الداخلية في القوقعة معلومات الصوت إلى العصب السمعي. يوفر جين OTOF الشفرة لبروتين يُدعى أوتوفرلين، وهو ضروري لإطلاق حزم صغيرة من الإشارات الكيميائية عند هذه المشابك. عندما يغيب الأوتوفرلين، لا يتم توصيل إشارة الصوت ببساطة، وهي حالة تُعرف بالاعتلال المشبكي السمعي. وبما أن بقية أجزاء الأذن قد تظل سليمة بنيويًا لسنوات، فإن هذا الشكل من الصمم يعتبر واعدًا على نحو خاص للعلاجات الجينية لمرة واحدة التي تهدف إلى استعادة الأوتوفرلين المفقود.
هندسة نموذج أولي للقرد الشمسي لصمم الإنسان
كانت الفئران قيمة لفهم السمع، لكن جيناتها وتطورها ووقت بدء السمع تختلف عنا بطرق مهمة. بالمقابل، قرود المارسوت الصغيرة هي قرود غير بشرية تشترك معنا في جزء أكبر من الحمض النووي، وتبدأ في السمع قبل الولادة، ولديها تواصل صوتي اجتماعي ثري. جمع الباحثون بين التلقيح الاصطناعي ونظام التحرير الجيني CRISPR/Cas9 لتعطيل إكسون حاسم في جين OTOF لدى المارسوت. عن طريق حقن خلطات محسنة بعناية من مكونات CRISPR في الأجنّة المبكرة، سعوا إلى حذف هذا الجزء في النسختين الجينيتين مع تجنب عقبة رئيسية في تحرير الرئيسيات: الفسيفساءية، حيث تحمل خلايا مختلفة في نفس الحيوان طفرات مختلفة. بعد دورات عديدة من جمع البويضات والتخصيب ونقل الأجنة إلى أمهات بديلات، حصلوا على قردتين نجتا مع تعطيل ثنائي الالحاق وغير فسيفسائي في OTOF — بمعنى أن كل خلية حملت الطفرة المطلوبة.
فحص السمع وإشارات الدماغ والسلوك
لاكتشاف ما إذا كانت هذه القرود المهندَسة تمثل بالفعل الحالة البشرية، اختبر الفريق سمعها بدءًا من عمر ستة أشهر. كانت التسجيلات الكهربائية من جذع الدماغ، التي تُظهر عادة موجات واضحة عندما يصل الصوت إلى المسار السمعي، مسطحة حتى عند مستويات صوتية عالية جدًا في الحيوانات المطوية الجين. في الوقت نفسه، كانت اختبارات الانبعاثات الأذينية الصوتية — الصدى الصغير الناتج عن خلايا الشعر الخارجية — قوية ومشابهة لتلك لدى القرود الطبيعية. يتطابق هذا الجمع بين غياب استجابات الدماغ وبقاء ميكانيكا القوقعة مع الاعتلال المشبكي السمعي المرتبط بـ OTOF لدى البشر. وأكد الفحص المجهري لأذن داخلية لحيوان واحد وجود خلايا الشعر الداخلية لكن دون بروتين الأوتوفرلين، في حين ظلت البنية العامة للقوقعة سليمة. 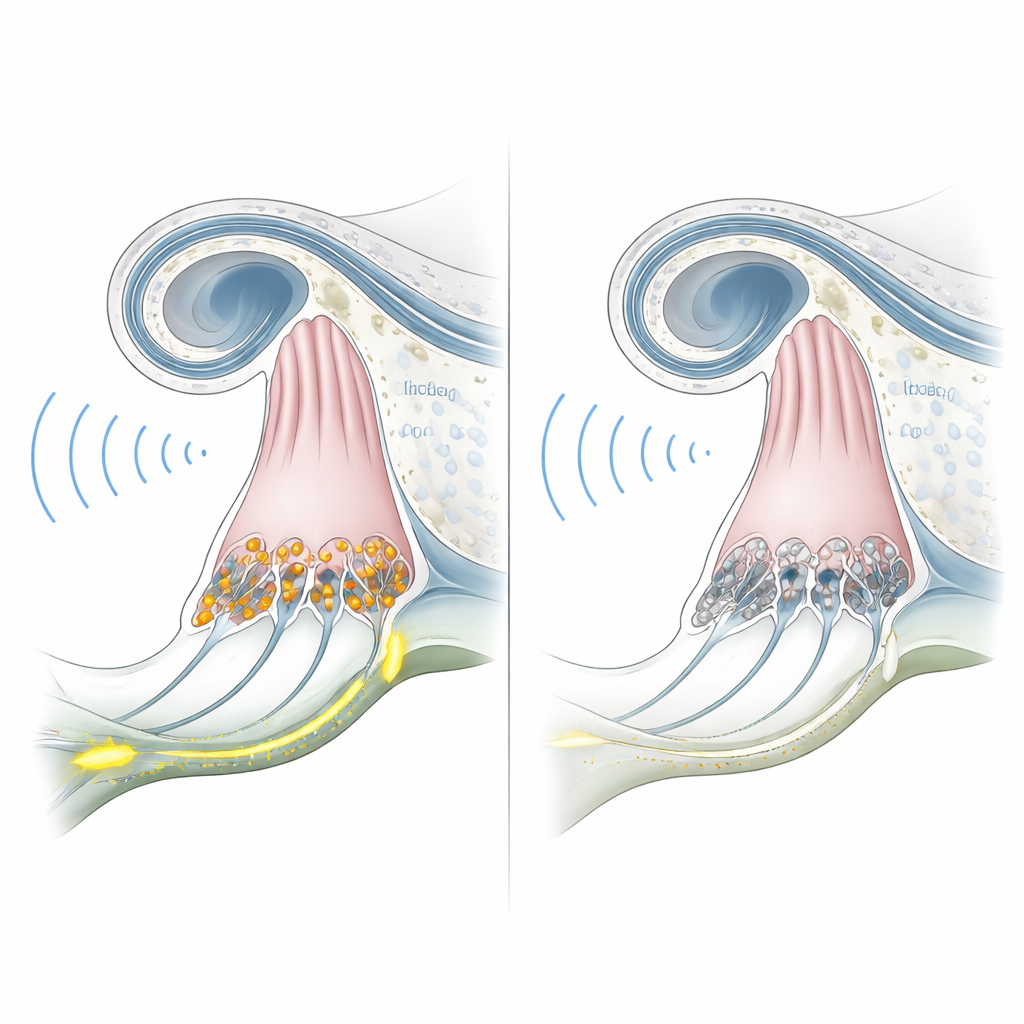
أصوات بلا سمع
بما أن المارسوت معروفة بثرثرتها الصوتية، سأل العلماء أيضًا كيف يؤثر الصمم على تطور الصوت المبكر. عندما سُجلت الصغار لفترات قصيرة بعيدًا عن عائلاتهم، أنتجت كل من القرود الطبيعية والمطعونة آلاف النداءات، بما في ذلك جميع أنواع النداءات الرئيسية التي تصدر عادةً من الصغار الأصحاء. كانت معدلات النداء متشابهة بين المجموعتين، ما يشير إلى أن الدافع الأساسي ومجموعة الأصوات الفطرية موجودة وليست معتمدة على السمع، على الأقل في المراحل المبكرة من الحياة. ومع ذلك، كشفت تحليلات أكثر تفصيلاً أن أطول أنواع النداءات لم تطلِ مثلما يحدث مع تقدم العمر في الحيوانات الصمّة مقارنة بالحيوانات السامعة، مما يلمّح إلى أن التغذية الراجعة السمعية لا تزال تشكل جوانب أدق من نضج الصوت بمرور الوقت. تحدث هذه الاختلافات الطفيفة قيمة النموذج ليس فقط لأبحاث السمع ولكن أيضًا لفهم كيف يشكّل الخبرة السمعية التواصل.
طرق جديدة نحو علاجات سمعية أفضل
من خلال إنتاج مارسوت مع تعطيل نظيف وغير فسيفسائي لجين OTOF، يقدم هذا العمل نموذجًا للرئيسيات يتتبع عن قرب شكلًا بشريًا من الصمم الوراثي. تظهر الحيوانات السمات المميزة للاعتلال المشبكي السمعي: ميكانيكا طبيعية للأذن الخارجية، غياب الأوتوفرلين في خلايا الشعر الداخلية، وفشل في نقل معلومات الصوت إلى الدماغ. سيسمح هذا النموذج للباحثين بضبط استراتيجيات العلاج الجيني — اختبار أنظمة توصيل فيروسية مختلفة، والجرعات، والتوقيت، وربط نتائج السمع طويلة المدى بقياسات دقيقة لاستعادة الأوتوفرلين في الأذن الداخلية. وعلى الرغم من أن إنشاء مثل هذه النماذج في الرئيسيات بطيء ومكلف ومُكلّف أخلاقيًا، يجادل المؤلفون بأن القدرة على تحسين علاجات مغيرة للحياة للأطفال المصابين بالصمم الوراثي تجعل هذا النهج المسيطر عليه بعناية ذا قيمة علمية وطبية.
الاستشهاد: Kahland, T., Lindenwald, D.L., Jeschke, M. et al. Generation of marmoset monkeys with a non-mosaic disruption of the OTOF gene as a model of human deafness. Nat Commun 17, 3033 (2026). https://doi.org/10.1038/s41467-026-71047-1
الكلمات المفتاحية: الصمم الوراثي, نموذج المارسوت, العلاج الجيني, الاعتلال المشبكي السمعي, تحرير CRISPR