Clear Sky Science · pt
Geração de saguis marmoset com uma descontinuidade não-mosaica do gene OTOF como modelo da surdez humana
Por que macacos pequenos importam para a perda auditiva
A perda auditiva causada por genes defeituosos é comum e, para um gene importante chamado OTOF, a terapia genética em crianças já está começando. Ainda assim, faltava aos cientistas um modelo animal que espelhasse de perto o ouvido humano para testar quão seguras, precisas e duradouras essas intervenções realmente são. Este estudo cria exatamente isso: uma linhagem de pequenos marmosets geneticamente modificados para apresentar o mesmo tipo de surdez observado em muitas crianças, oferecendo uma ponte poderosa entre experimentos em camundongos e ensaios clínicos humanos. 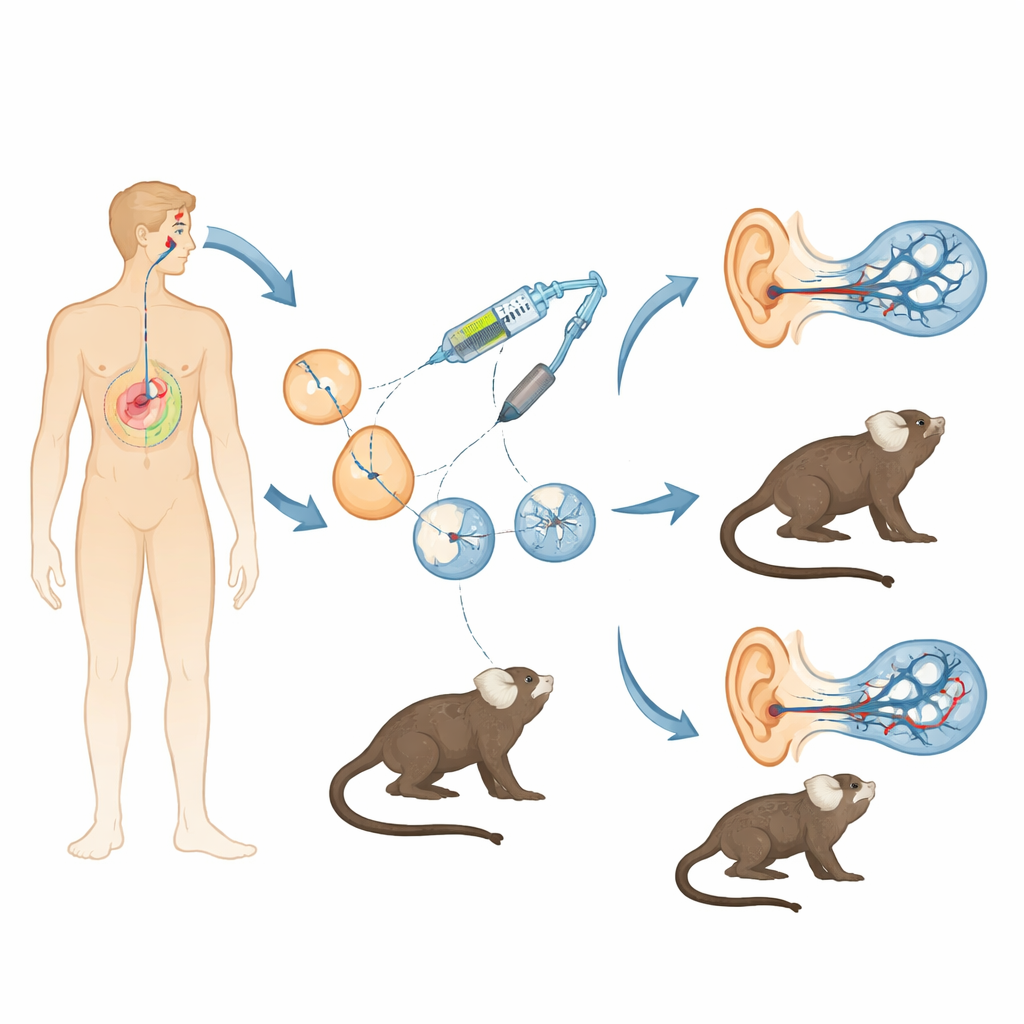
Uma sinapse silenciosa no cerne da surdez
Muitas pessoas com surdez relacionada ao OTOF têm ouvidos que parecem normais e até células da orelha externa que ainda respondem ao som. O problema está mais profundo, nas junções microscópicas onde as células ciliadas internas da cóclea transmitem a informação sonora para o nervo auditivo. O gene OTOF codifica a proteína otoferlina, essencial para liberar minúsculos pacotes de sinais químicos nessas sinapses. Quando a otoferlina está ausente, o sinal sonoro simplesmente não é transmitido, uma condição conhecida como sinaptopatia auditiva. Como o restante do ouvido pode permanecer estruturalmente saudável por anos, essa forma de surdez é especialmente promissora para terapias genéticas de dose única que visam restaurar a otoferlina ausente.
Engenharia de um modelo primata da surdez humana
Camundongos têm sido inestimáveis para entender a audição, mas seus genes, desenvolvimento e início da audição diferem em aspectos fundamentais dos nossos. Os marmosets, em contrapartida, são pequenos primatas não humanos que compartilham mais do nosso DNA, começam a ouvir antes do nascimento e possuem comunicação vocal social rica. Os pesquisadores combinaram fertilização in vitro com o sistema de edição genética CRISPR/Cas9 para interromper um éxon crucial do gene OTOF do marmoset. Ao injetar misturas cuidadosamente otimizadas dos componentes CRISPR em embriões precoces, buscaram deletar esse segmento em ambas as cópias do gene enquanto evitavam uma armadilha maior da edição em primatas: o mosaicismo, quando células diferentes no mesmo animal apresentam mutações distintas. Após muitas rodadas de coleta de oócitos, fertilização e transferência de embriões para mães de aluguel, obtiveram dois macacos sobreviventes com descontinuidades bialélicas e não-mosaicas no OTOF — isto é, todas as células carregavam a interrupção pretendida.
Avaliando audição, sinais cerebrais e comportamento
Para verificar se esses macacos realmente modelavam a condição humana, a equipe testou a audição a partir dos seis meses de idade. Registros elétricos do tronco encefálico, que normalmente mostram ondas claras quando o som alcança a via auditiva, estavam planos mesmo em níveis sonoros muito altos nos animais com knockout. Ao mesmo tempo, testes de emissões otoacústicas — pequenos ecos gerados pelas células ciliadas externas — foram robustos e semelhantes aos de macacos normais. Essa combinação de respostas cerebrais ausentes mas mecânica coclear preservada corresponde de perto à sinaptopatia auditiva humana relacionada ao OTOF. Exame microscópico do ouvido interno de um animal confirmou que as células ciliadas internas estavam presentes mas sem a proteína otoferlina, enquanto a estrutura coclear geral permanecia intacta. 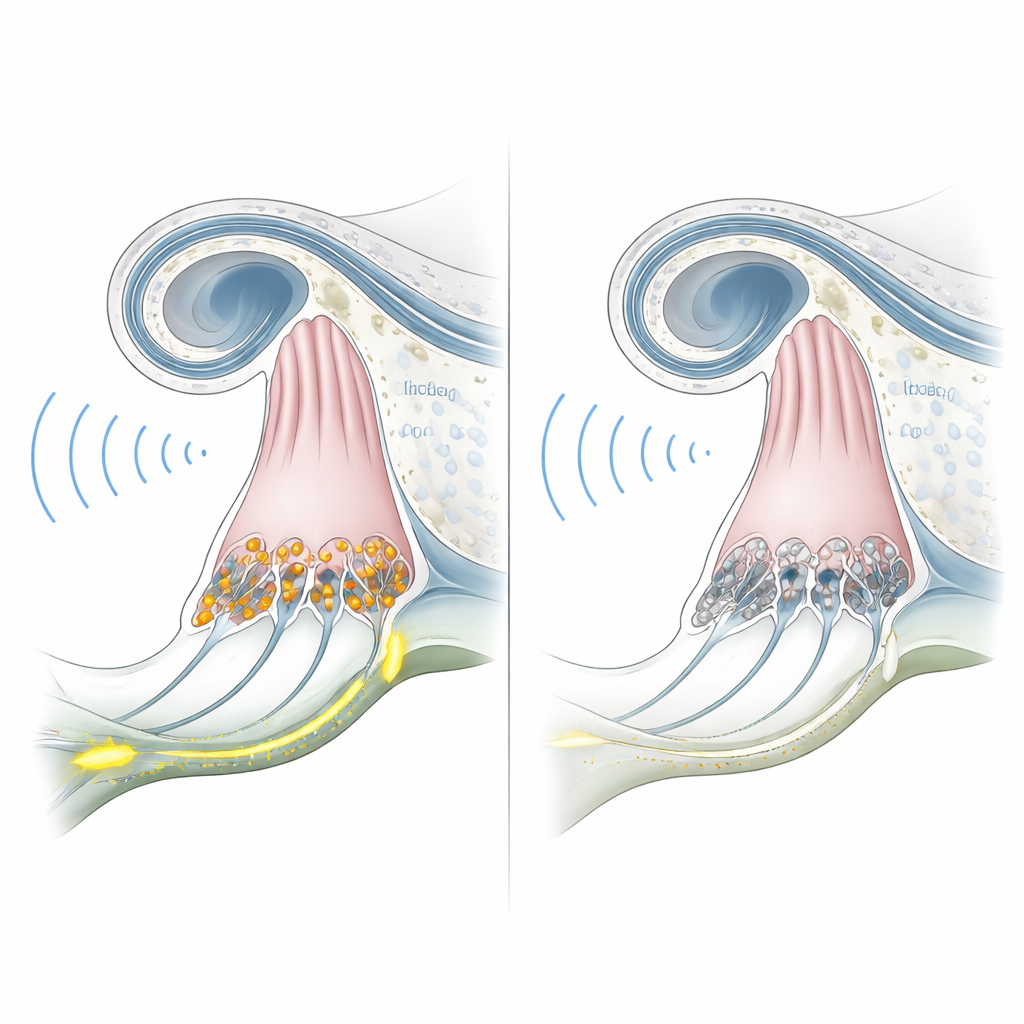
Vozes sem audição
Como os marmosets são notoriamente vocais, os cientistas também investigaram como a surdez afetava o desenvolvimento vocal precoce. Quando filhotes foram brevemente gravados longe das suas famílias, tanto macacos normais quanto com knockout produziram milhares de vocalizações, incluindo todos os principais tipos de chamada que filhotes saudáveis geralmente emitem. As taxas de vocalização foram semelhantes entre os grupos, sugerindo que o impulso básico e o repertório para vocalizações são em grande parte inatos e não exigem audição, ao menos no início da vida. No entanto, análises mais detalhadas revelaram que os tipos de chamada mais longos não se alongaram com a idade tanto nos animais surdos quanto nos ouvintes, indicando que o feedback auditivo ainda molda aspectos mais sutis da maturação vocal ao longo do tempo. Essas diferenças sutis tornam o modelo valioso não apenas para pesquisa auditiva, mas também para entender como a experiência sonora esculpe a comunicação.
Novos caminhos para tratamentos auditivos melhores
Ao produzir marmosets com um knockout limpo e não-mosaico do gene OTOF, este trabalho entrega um modelo primata que acompanha de perto uma forma humana de surdez hereditária. Os animais exibem as características marcantes da sinaptopatia auditiva: mecânica normal da orelha externa, ausência de otoferlina nas células ciliadas internas e falha em transmitir a informação sonora ao cérebro. Esse modelo permitirá aos pesquisadores ajustar estratégias de terapia genética — testando diferentes sistemas virais de entrega, doses e tempos, e vinculando resultados auditivos de longo prazo a medições precisas da restauração da otoferlina no ouvido interno. Embora a criação de modelos primatas seja lenta, cara e eticamente exigente, os autores argumentam que o potencial de melhorar terapias que mudam a vida de crianças com surdez genética torna essa abordagem cuidadosamente controlada tanto cientificamente quanto medicamente justificável.
Citação: Kahland, T., Lindenwald, D.L., Jeschke, M. et al. Generation of marmoset monkeys with a non-mosaic disruption of the OTOF gene as a model of human deafness. Nat Commun 17, 3033 (2026). https://doi.org/10.1038/s41467-026-71047-1
Palavras-chave: surdez genética, modelo em marmoset, terapia genética, sinaptopatia auditiva, edição CRISPR