Clear Sky Science · de
Erzeugung von Marmosett-Affen mit einer nicht-mosaikartigen Störung des OTOF-Gens als Modell für menschliche Taubheit
Warum kleine Affen für das Hörvermögen wichtig sind
Gehörverlust durch fehlerhafte Gene ist weit verbreitet, und für ein besonders wichtiges Gen namens OTOF beginnen Gentherapien bereits bei Kindern. Dennoch fehlt der Forschung bislang ein Tiermodell, das das menschliche Ohr eng genug nachbildet, um Sicherheit, Präzision und Dauerhaftigkeit solcher Behandlungen zuverlässig zu prüfen. Diese Studie schafft genau das: eine Linie kleiner Marmosett-Affen, die so gezüchtet wurden, dass sie die bei vielen Kindern beobachtete Form der Taubheit aufweisen und damit eine starke Brücke zwischen Mausexperimenten und klinischen Studien am Menschen bilden. 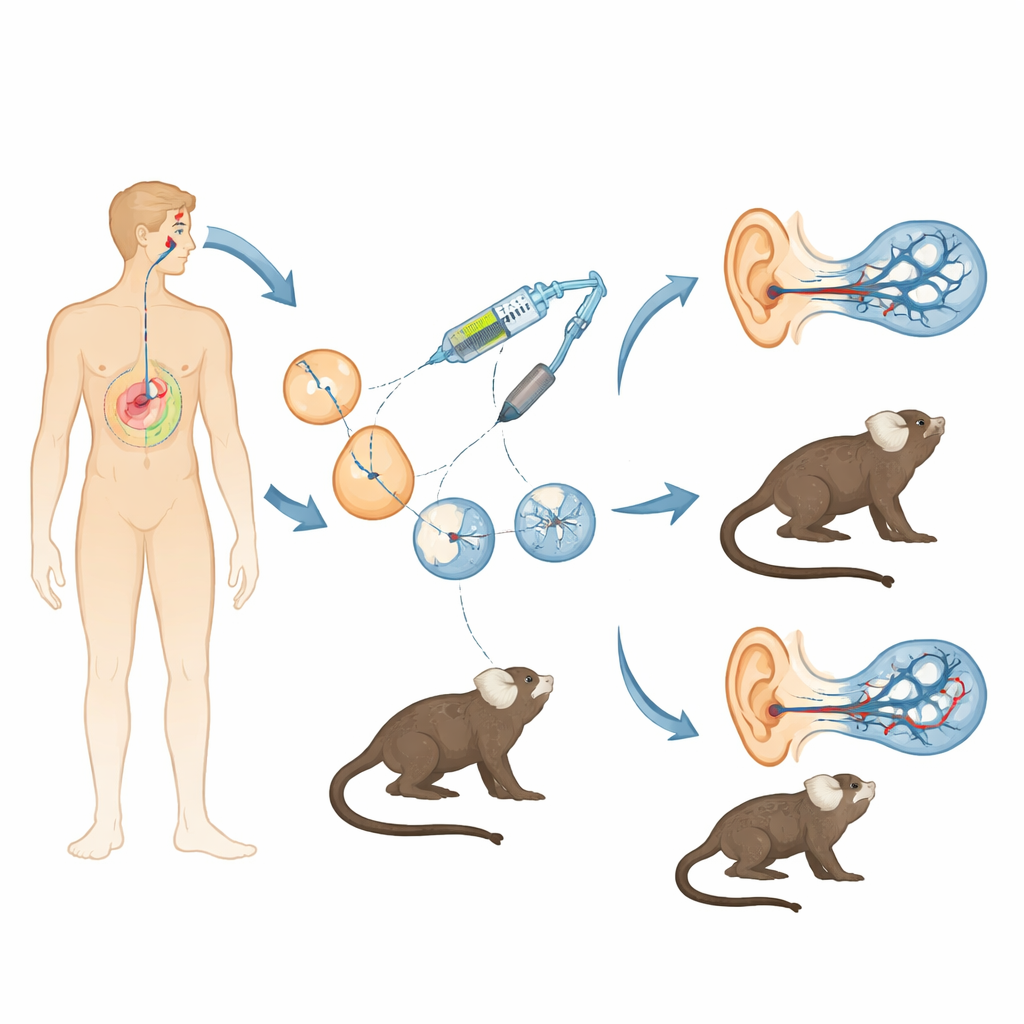
Eine stumme Synapse im Kern der Taubheit
Viele Menschen mit OTOF-bedingter Taubheit haben Ohren, die äußerlich normal erscheinen, und selbst äußere Haarzellen, die noch auf Geräusche reagieren. Das Problem liegt tiefer, an den mikroskopischen Verbindungsstellen, an denen innere Haarzellen der Cochlea Schallinformationen an den Hörnerv weitergeben. Das OTOF-Gen liefert den Bauplan für ein Protein namens Otoferlin, das für die Freisetzung winziger chemischer Signalpakete an diesen Synapsen entscheidend ist. Fehlt Otoferlin, wird das Tonsignal schlichtweg nicht weitergeleitet — ein Zustand, der als auditorische Synaptopathie bezeichnet wird. Da der Rest des Ohrs über Jahre strukturell intakt bleiben kann, eröffnet diese Form der Taubheit besonders gute Chancen für einmalige Gentherapien, die darauf abzielen, das fehlende Otoferlin wiederherzustellen.
Ein Primatenmodell menschlicher Taubheit konstruieren
Mäuse waren und sind unschätzbar für das Verständnis des Hörens, doch in wichtigen Punkten unterscheiden sich ihre Gene, Entwicklung und der Beginn des Hörvermögens von denen des Menschen. Marmosette hingegen sind kleine Nichtmenschen-Primaten, die uns genetisch näherstehen, bereits vor der Geburt mit dem Hören beginnen und eine reiche soziale vokale Kommunikation zeigen. Die Forschenden kombinierten In-vitro-Fertilisation mit dem CRISPR/Cas9-Geneditierungssystem, um ein entscheidendes Exon im marmosettischen OTOF-Gen zu stören. Durch das Injizieren sorgfältig optimierter Mischungen aus CRISPR-Komponenten in frühe Embryonen versuchten sie, dieses Segment in beiden Genkopien zu löschen und gleichzeitig eine große Fallstricke der Primaten-Editierung zu vermeiden: Mosaizität, bei der verschiedene Zellen desselben Tieres unterschiedliche Mutationen tragen. Nach vielen Zyklen der Eizellgewinnung, Befruchtung und Embryotransfer in Leihmütter erhielten sie zwei überlebende Affen mit biallelischen, nicht-mosaikartigen OTOF-Störungen — das heißt, jede Zelle trug den beabsichtigten Knockout.
Hören, Hirnsignale und Verhalten prüfen
Um zu prüfen, ob diese genetisch veränderten Affen das menschliche Krankheitsbild wirklich abbilden, testete das Team ihr Hörvermögen ab einem Alter von sechs Monaten. Elektrische Aufzeichnungen vom Hirnstamm, die normalerweise klare Wellen zeigen, wenn Schall den auditorischen Weg erreicht, blieben selbst bei sehr lauten Schallpegeln bei den Knockout-Tieren aus. Gleichzeitig waren Tests der otoakustischen Emissionen — winzige Echo-Signale, die von äußeren Haarzellen erzeugt werden — robust und denen normaler Affen ähnlich. Diese Kombination aus fehlenden hirnvermittelten Reaktionen bei gleichzeitig erhaltenen cochleären Mechaniken entspricht genau der menschlichen OTOF-bedingten auditorischen Synaptopathie. Die mikroskopische Untersuchung des Innenohrs eines Tieres bestätigte, dass die inneren Haarzellen vorhanden, jedoch ohne Otoferlin waren, während die Gesamtstruktur der Cochlea intakt blieb. 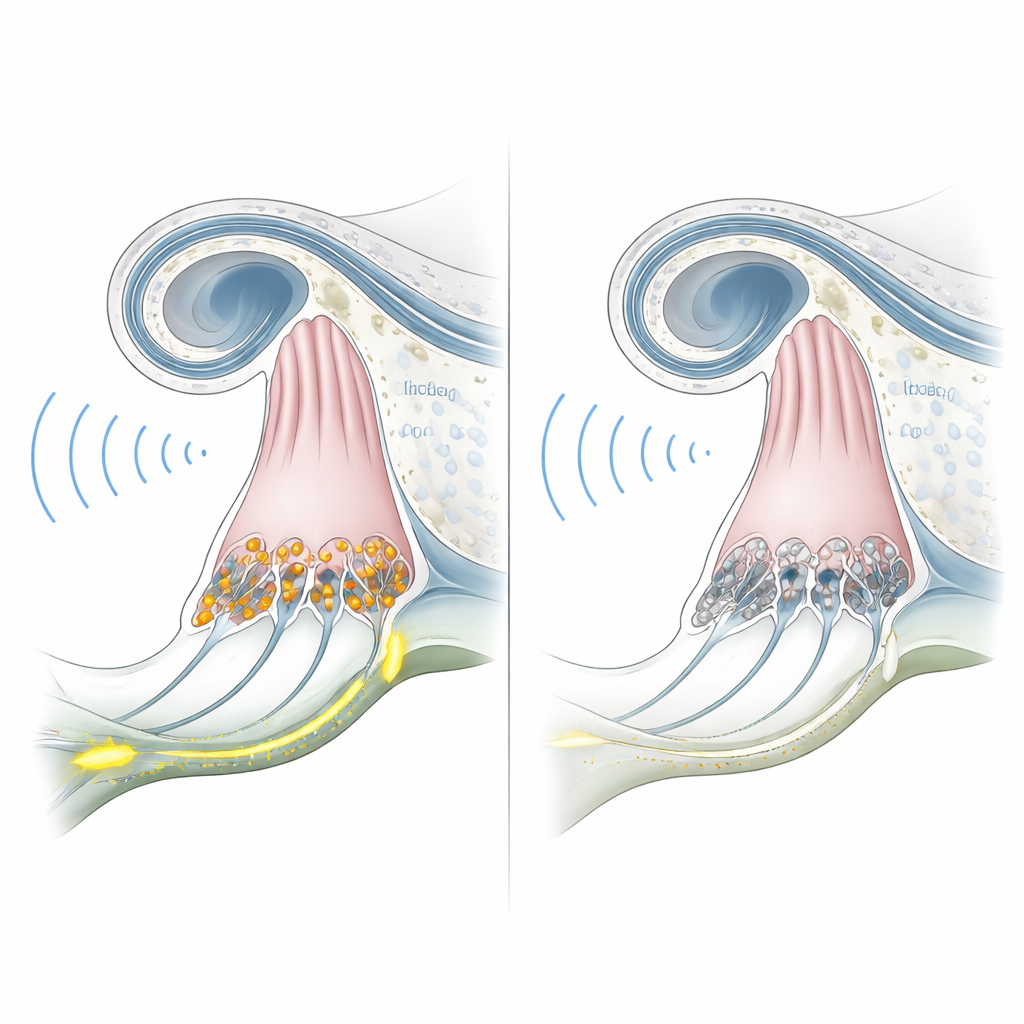
Stimmen ohne Hören
Da Marmosette für ihren Gesprächsreichtum bekannt sind, fragten die Wissenschaftlerinnen und Wissenschaftler auch, wie sich Taubheit auf die frühe vokale Entwicklung auswirkt. Als die Jungtiere kurzzeitig getrennt von ihren Familien aufgenommen wurden, produzierten sowohl normale als auch Knockout-Affen Tausende von Lauten, einschließlich aller wichtigen Lauttypen, die gesunde Jungtiere normalerweise zeigen. Die Rufraten waren in beiden Gruppen ähnlich, was darauf hindeutet, dass der grundlegende Antrieb und das Repertoire für Lautäußerungen weitgehend angeboren sind und zumindest in den frühen Lebensphasen kein Hören erfordern. Eine detailliertere Analyse zeigte jedoch, dass sich die längsten Lauttypen bei tauben Tieren mit dem Alter nicht so stark verlängerten wie bei hörenden Tieren, was darauf hindeutet, dass auditives Feedback feinere Aspekte der vokalen Reifung über die Zeit hinweg formt. Diese subtilen Unterschiede machen das Modell nicht nur für die Hörforschung wertvoll, sondern auch für das Verständnis, wie Hörerfahrungen Kommunikation prägen.
Neue Wege zu besseren Hörbehandlungen
Indem sie Marmosette mit einem sauberen, nicht-mosaikartigen Knockout des OTOF-Gens erzeugten, liefern die Autoren ein Primatenmodell, das eine menschliche Form erblich bedingter Taubheit genau widerspiegelt. Die Tiere zeigen die Kennzeichen einer auditorischen Synaptopathie: normale Mechanik der äußeren Cochlea, fehlendes Otoferlin in den inneren Haarzellen und ein Ausfallen der Weiterleitung von Schallinformationen zum Gehirn. Dieses Modell ermöglicht es Forschenden, Gentherapie-Strategien zu verfeinern — verschiedene virale Transportsysteme, Dosen und Zeitpunkte zu testen und langfristige Hörergebnisse mit präzisen Messungen der Otoferlin-Wiederherstellung im Innenohr zu verknüpfen. Obwohl die Erzeugung solcher Primatenmodelle langsam, kostspielig und ethisch anspruchsvoll ist, argumentieren die Autoren, dass das Potenzial, lebensverändernde Therapien für Kinder mit genetischer Taubheit zu verbessern, diesen sorgfältig kontrollierten Ansatz sowohl wissenschaftlich als auch medizinisch lohnenswert macht.
Zitation: Kahland, T., Lindenwald, D.L., Jeschke, M. et al. Generation of marmoset monkeys with a non-mosaic disruption of the OTOF gene as a model of human deafness. Nat Commun 17, 3033 (2026). https://doi.org/10.1038/s41467-026-71047-1
Schlüsselwörter: genetische Taubheit, Marmosett-Modell, Gentherapie, auditorische Synaptopathie, CRISPR-Bearbeitung