Clear Sky Science · he
יצירת קופי מרמוסטים עם ניתוק לא-מוזאיקי של גן OTOF כמודל לחירשות אנושית
למה קופים קטנים חשובים למחלת שמיעה
חירשות הנגרמת על־ידי גנים לקויים נפוצה, ועבור גן חשוב אחד בשם OTOF כבר מתחילים ניסויים בתרפיה גנטית בילדים. עם זאת, למדענים עדיין חסר מודל חייתי שמשקף באופן דוק את האוזן האנושית כדי לבדוק עד כמה טיפולים אלה בטוחים, מדויקים ומתמשכים. המחקר הזה יוצר בדיוק את זה: שושלת של קופי מרמוסטים קטנים שהונדסו כך שיפתחו את אותו סוג חירשות שנצפה אצל ילדים רבים, ומספקת גשר עוצמתי בין ניסויים בעכברים לניסויים קליניים בבני אדם. 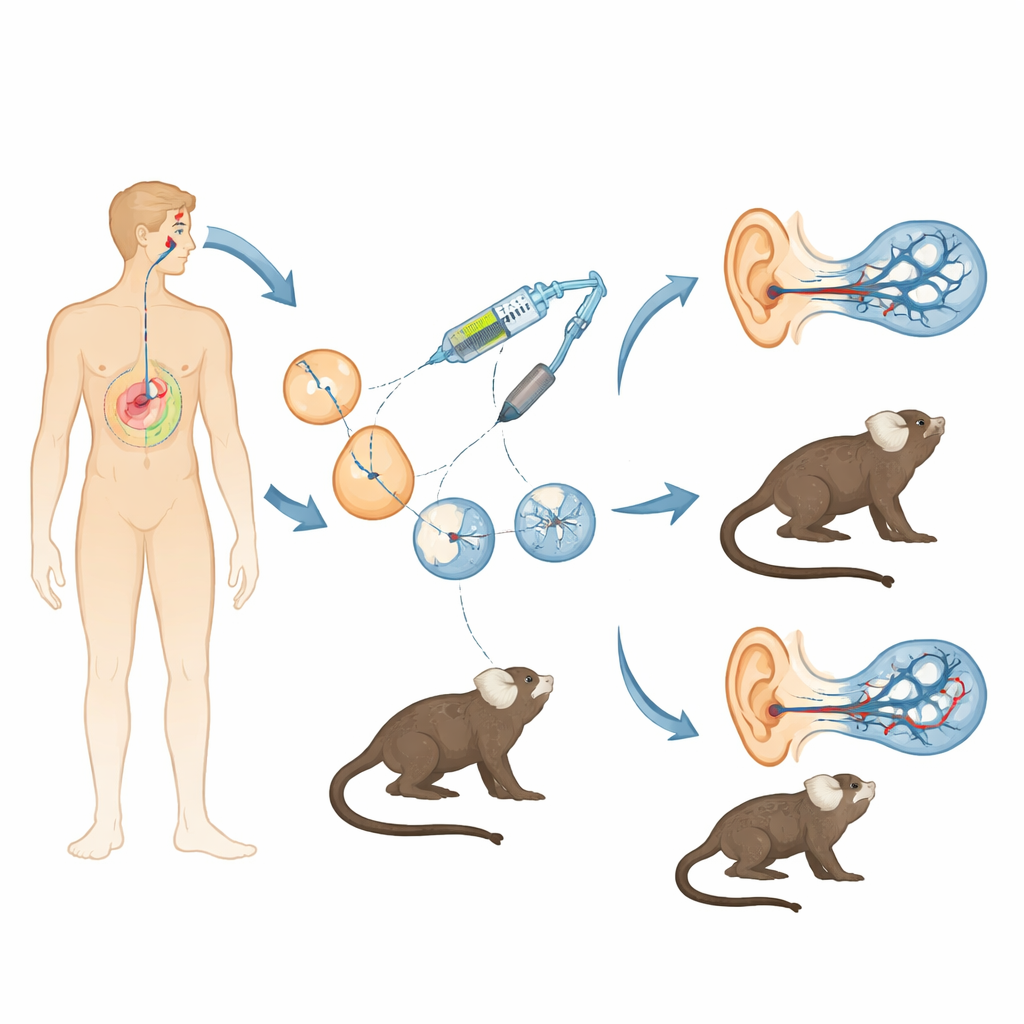
סינפסה אילמת בלב החירשות
הרבה אנשים עם חירשות הקשורה ל־OTOF נראים כאילו אוזניהם תקינות ואפילו תאי האוזן החיצוניים עדיין מגיבים לקול. הבעיה נמצאת עמוק יותר, במפרקי הגוף המיקרוסקופיים שבהם תאי השיער הפנימיים בבסיס השבלול מעבירים מידע שמיעתי לעצב השמיעה. גן OTOF מכיל את התבנית לחלבון בשם אוטופרלין, החשוב לשחרור מנות זעירות של אותות כימיים בסינפסות אלה. כשהאוטופרלין חסר, אות הקול פשוט לא מועבר — מצב הידוע כסינפטופתיה שמיעתית. כיוון ששאר המבנה של האוזן יכול להישאר בריא למשך שנים, צורה זו של חירשות מבטיחה במיוחד טיפולי גן חד־פעמיים שמטרתם לשחזר את האוטופרלין החסר.
הנדסה של מודל פרימאטי לחירשות אנושית
עכברים היו בעלי ערך רב להבנת השמיעה, אך הגנים שלהם, ההתפתחות ותזמון תחילת השמיעה שונים במובנים מהותיים משלנו. לעומת זאת, קופי מרמוסט הם פרימטים קטנים שאנו חולקים איתם יותר דנ"א, הם מתחילים לשמוע עוד לפני הלידה ומפגינים תקשורת קולית חברתית עשירה. החוקרים שילבו הפריה חוץ־גופית עם מערכת עריכת הגנים CRISPR/Cas9 כדי לשבש אקסון חיוני בגן OTOF של המרמוסט. על־ידי הזרקת תערובות ממוטבות בקפידה של רכיבי CRISPR לעוברים מוקדמים, הם ניסו למחוק מקטע זה בשתי העותקים של הגן תוך הימנעות ממכשול עיקרי בעריכת פרימטים: מוזאיקה, שבה תאים שונים באותו בעל־החיים נושאים מוטציות שונות. לאחר סיבובים רבים של איסוף ביציות, הפריה והעברת עוברים לנקבות פונדקאיות, הם קיבלו שני קופים ששרדו עם הפרעות OTOF בילאיליות ולא־מוזאיקיות — כלומר כל תא נשא את הכיבוי הרצוי.
בדיקת שמיעה, אותות מוח והתנהגות
כדי לבדוק האם הקופים המהונדסים אכן מהווים מודל למצב האנושי, הצוות בחן את שמיעתם החל מגיל שישה חודשים. הקלטות חשמליות מהגזע המוחי, שבדרך כלל מראות גלים ברורים כאשר קול מגיע לנתיב השמיעה, היו שטוחות אפילו בעוצמות קול גבוהות מאוד אצל בעלי הכיבוי. בו בזמן, בדיקות של פליטת קול אוטואקוסטית — הדהודים זעירים שמייצרים תאי השיער החיצוניים — היו חזקים ודומים לאלה של קופים תקינים. השילוב הזה של תגובות מוחיות נעדרות אך מכניקת שבלול שמורה תואם מקרוב את הסינפטופתיה השמיעתית האנושית הקשורה ל־OTOF. בדיקה מיקרוסקופית של האוזניים הפנימיות של אחד החיות אישרה כי תאי השיער הפנימיים קיימים אך חסר בהם חלבון האוטופרלין, בעוד שמבנה השבלול הכולל נותר שלם. 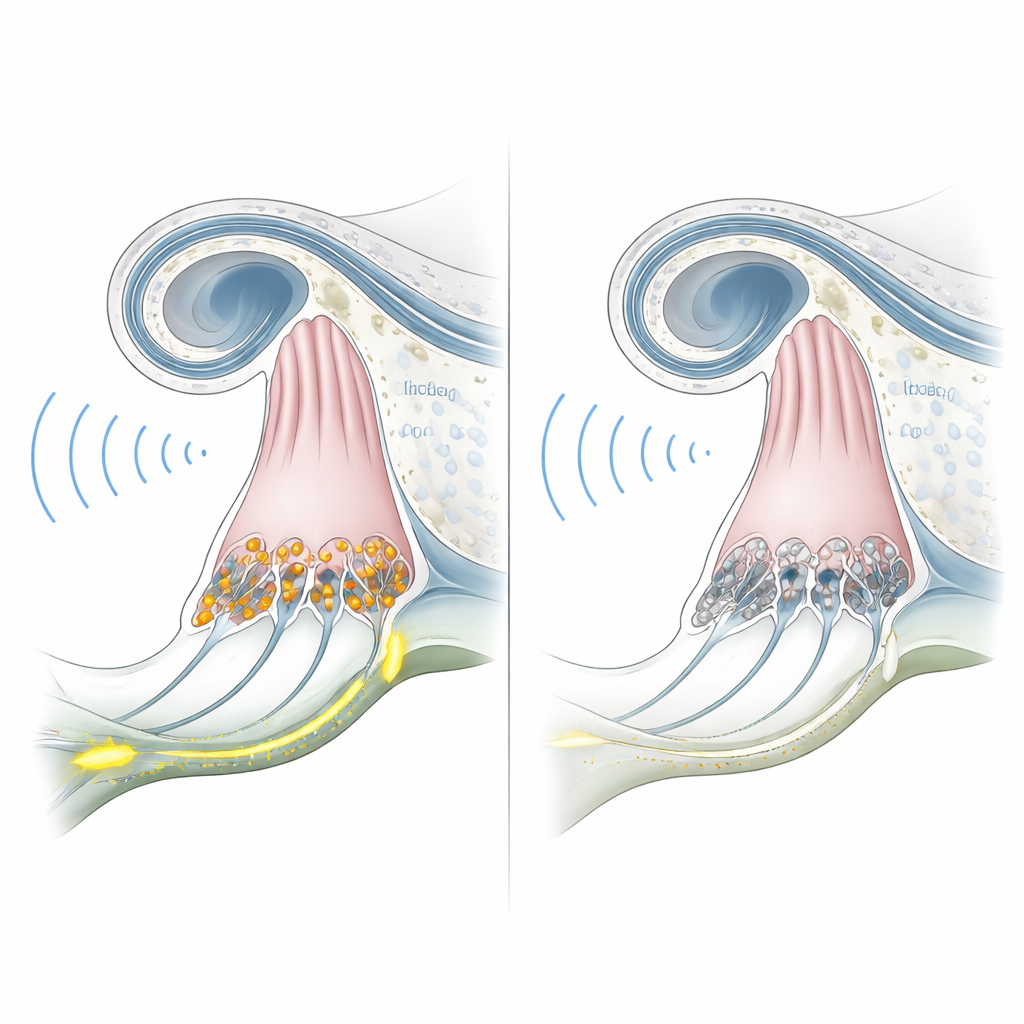
קולות בלי שמיעה
מכיוון שמרמוסט ידועים כפרטנוניים ברובם עם נטייה רבה להשמיע קולות, החוקרים גם בדקו כיצד החירשות משפיעה על התפתחות הווקליזציה המוקדמת. כאשר תיעדו לתקופות קצרות גורים הרחק ממשפחותיהם, גם הקופים התקינים וגם אלה עם הכיבוי הפיקו אלפי קריאות, כולל כל סוגי הקריאות העיקריים שילודים בריאים מבצעים בדרך כלל. קצב הקריאות היה דומה בין הקבוצות, מה שמרמז שהתמריץ הבסיסי והמגוון של הווקליזציות בנויים במידה רבה מראש ואינם דורשים שמיעה, לפחות בשלבים המוקדמים של החיים. עם זאת, ניתוח מפורט יותר הראה שהסוגים הארוכים ביותר של קריאות לא התארכו עם הגיל באותה מידה אצל החיות החירשות כפי שהיה אצל החיות השומעות, דבר שמרמז שמשוב שמיעתי מעצב עדיין היבטים עדינים של הבשלת הווקליזציה לאורך זמן. הבדלים עדינים אלה הופכים את המודל בעל ערך לא רק למחקר שמיעה אלא גם להבנת האופן שבו חוויית הצליל מעצבת תקשורת.
דרכים חדשות לטיפולים שמיעתיים טובים יותר
על־ידי יצירת מרמוסטים עם כיבוי נקי ולא־מוזאיקי של גן OTOF, עבודה זו מספקת מודל פרימאטי שעוקב בצמוד צורה אנושית של חירשות תורשתית. החיות מציגות תכונות מייצגות של סינפטופתיה שמיעתית: מכניקת אוזן חיצונית תקינה, היעדר אוטופרלין בתאי השיער הפנימיים וכישלון בהעברת מידע שמיעתי למוח. מודל זה יאפשר לחוקרים לכוונן אסטרטגיות תרפיה גנטית — לבדוק מערכות וקטוריות שונות, מינונים ותזמונים, ולקשר תוצאות שמיעה ארוכות טווח למדידות מדויקות של שחזור אוטופרלין באוזן הפנימית. למרות שיצירת מודלים פרימטיים כאלה איטית, יקרה וטעונה מבחינה אתית, המחברים טוענים שהפוטנציאל לשפר טיפולים שמשני חיים לילדים עם חירשות גנטית עושה את הגישה המבוקרת הזאת ראויה הן מבחינה מדעית והן מבחינה רפואית.
ציטוט: Kahland, T., Lindenwald, D.L., Jeschke, M. et al. Generation of marmoset monkeys with a non-mosaic disruption of the OTOF gene as a model of human deafness. Nat Commun 17, 3033 (2026). https://doi.org/10.1038/s41467-026-71047-1
מילות מפתח: חירשות גנטית, מודל מרמוסט, תרפיה גנטית, סינפטופתיה שמיעתית, עריכת CRISPR