Clear Sky Science · nl
Generatie makakenmarmosets met een niet-mosaicale verstoring van het OTOF-gen als model voor menselijke doofheid
Waarom kleine apen belangrijk zijn voor gehoorverlies
Doofheid als gevolg van defecte genen komt veel voor, en voor één belangrijk gen, OTOF, begint gentherapie bij kinderen al. Toch ontbreekt het wetenschappers nog aan een diermodel dat het menselijk oor nauwkeurig nabootst om te testen hoe veilig, precies en langdurig zulke behandelingen werkelijk zijn. Deze studie creëert precies dat: een lijn van kleine marmoset-apen die zodanig zijn gefabriceerd dat zij hetzelfde type doofheid vertonen als veel kinderen, en daarmee een krachtig brug vormen tussen muisexperimenten en humane klinische proeven. 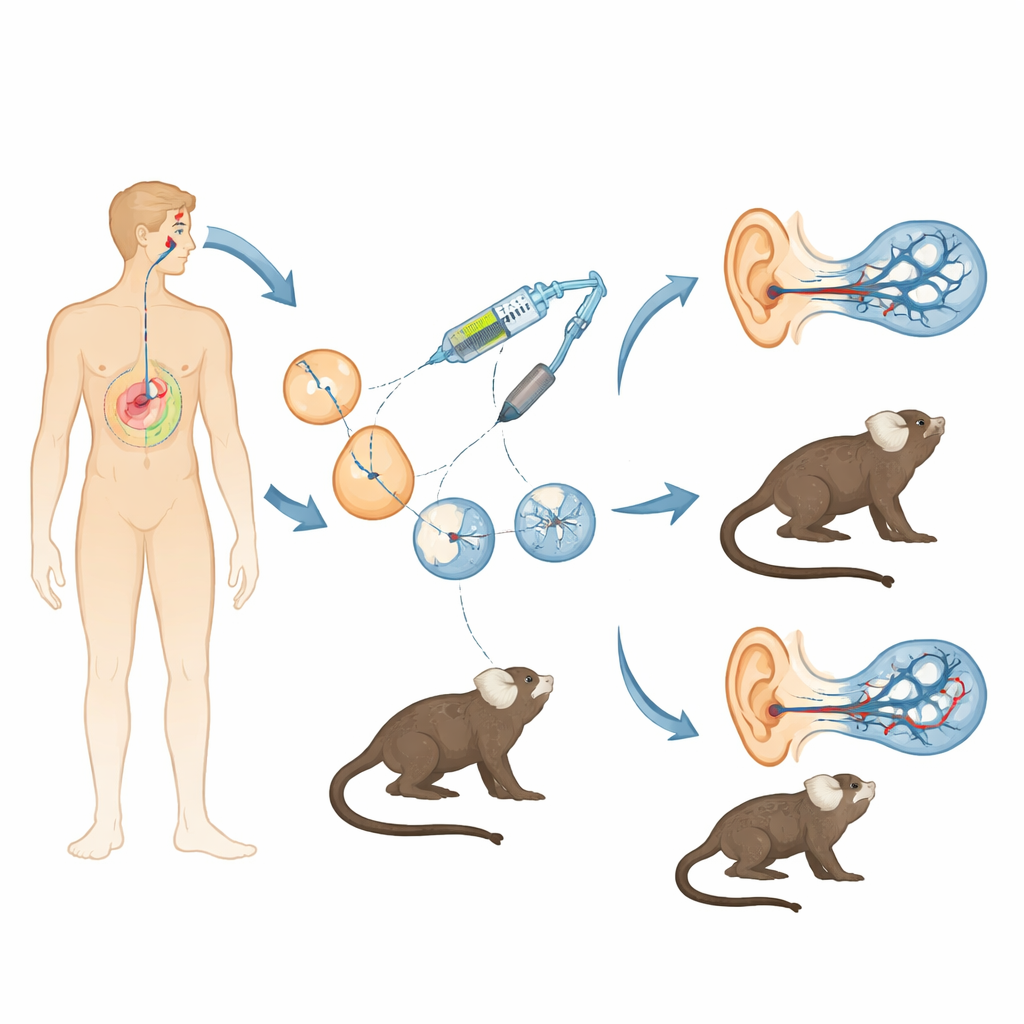
Een stille synaps in het hart van de doofheid
Veel mensen met OTOF-gerelateerde doofheid hebben oren die er normaal uitzien en zelfs buitenste haarcellen die nog op geluid reageren. Het probleem zit dieper, bij de microscopische verbindingen waarbinnen de binnenste haarcellen in het slakkenhuis geluidsinformatie doorgeven aan de gehoorzenuw. Het OTOF-gen bevat de blauwdruk voor een eiwit dat otoferline heet en essentieel is voor het vrijgeven van kleine pakketjes chemische boodschappers bij deze synapsen. Als otoferline ontbreekt, wordt het geluidssignaal simpelweg niet doorgegeven — een aandoening die bekendstaat als auditieve synaptopathie. Omdat de rest van het oor jarenlang structureel gezond kan blijven, is deze vorm van doofheid bijzonder veelbelovend voor eenmalige gentherapieën die tot doel hebben ontbrekende otoferline te herstellen.
Een primatenmodel van menselijke doofheid ontwikkelen
Muizen zijn van onschatbare waarde geweest voor het begrijpen van gehoor, maar hun genen, ontwikkeling en het begin van het gehoor verschillen op belangrijke punten van die van mensen. Marmosets daarentegen zijn kleine niet-menselijke primaten die meer van ons DNA delen, vóór de geboorte al kunnen horen en een rijke sociale vocale communicatie hebben. De onderzoekers combineerden in-vitrofertilisatie met het CRISPR/Cas9-genbewerkingssysteem om een cruciale exon in het marmoset-OTOF-gen te verstoren. Door zorgvuldig geoptimaliseerde mengsels van CRISPR-componenten in vroege embryo’s te injecteren, probeerden ze dit segment in beide genkopieën te verwijderen en tegelijk een grote valkuil van primatenbewerking te vermijden: mosaicisme, waarbij verschillende cellen in hetzelfde dier verschillende mutaties dragen. Na vele rondes van eicelverzameling, bevruchting en embryo-overdracht naar draagmoeders kregen ze twee overlevende apen met biallelische, niet-mosaicale OTOF-verstoringen — wat betekent dat elke cel de bedoelde knockout droeg.
Gehoor, hersensignalen en gedrag controleren
Om te achterhalen of deze gemodificeerde apen werkelijk het menselijke beeld nabootsten, testte het team hun gehoor vanaf zes maanden leeftijd. Elektrische opnames van de hersenstam, die normaal gesproken duidelijke golven laten zien wanneer geluid het auditieve pad bereikt, waren vlak zelfs bij zeer luide geluidsniveaus in de knockout-dieren. Tegelijkertijd waren testen van otoakoestische emissies — kleine echo’s die door buitenste haarcellen worden gegenereerd — sterk en vergelijkbaar met die van normale apen. Deze combinatie van afwezige hersenreacties maar behouden cochleaire mechanica komt nauwkeurig overeen met menselijke OTOF-gerelateerde auditieve synaptopathie. Microscopisch onderzoek van het binnenoor van één dier bevestigde dat binnenste haarcellen aanwezig waren maar geen otoferline-eiwit bevatten, terwijl de algehele cochleaire structuur intact bleef. 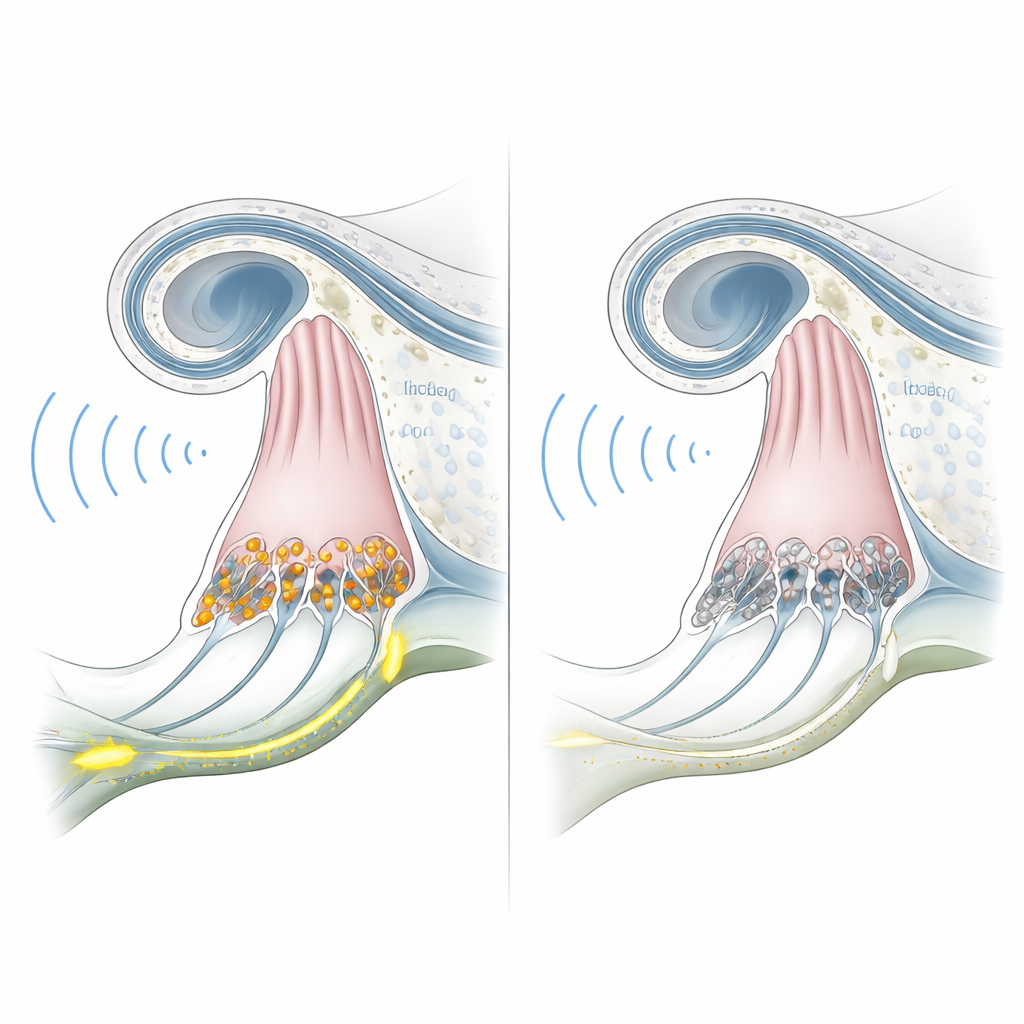
Stemmen zonder gehoor
Aangezien marmosets berucht vocaal zijn, onderzochten de wetenschappers ook hoe doofheid de vroege vocale ontwikkeling beïnvloedde. Toen zuigelingen kort werden opgenomen zonder hun families, produceerden zowel normale als knockout-apen duizenden roepen, inclusief alle belangrijke roepsoorten die gezonde zuigelingen gewoonlijk maken. Roepfrequenties waren vergelijkbaar tussen de groepen, wat suggereert dat de basisdrang en het repertoire voor vocalisaties grotendeels ingebouwd zijn en niet noodzakelijkerwijs gehoor vereisen, althans vroeg in het leven. Meer gedetailleerde analyse toonde echter dat de langste roepsoorten met de leeftijd minder toenamen bij dove dieren dan bij horende dieren, wat erop wijst dat auditieve feedback nog steeds fijnere aspecten van vocale rijping in de loop van de tijd vormt. Deze subtiele verschillen maken het model waardevol, niet alleen voor gehooronderzoek maar ook voor het begrijpen hoe geluidservaring communicatie vormt.
Nieuwe wegen naar betere gehoorbescherming en behandelingen
Door marmosets te produceren met een zuivere, niet-mosaicale knockout van het OTOF-gen levert dit werk een primatenmodel dat nauw aansluit bij een menselijke vorm van erfelijke doofheid. De dieren tonen de kenmerkende eigenschappen van auditieve synaptopathie: normale buitenste orenmechanica, ontbrekende otoferline in binnenste haarcellen en een falen om geluidsinformatie naar de hersenen te sturen. Dit model stelt onderzoekers in staat gentherapiestrategieën te verfijnen — verschillende virale afleveringssystemen, doses en timing te testen en langdurige gehooruitkomsten te koppelen aan precieze metingen van otoferline-herstel in het binnenoor. Hoewel het creëren van dergelijke primatenmodellen langzaam, kostbaar en ethisch belastend is, betogen de auteurs dat de potentie om levensveranderende therapieën voor kinderen met genetische doofheid te verbeteren deze zorgvuldig gecontroleerde aanpak zowel wetenschappelijk als medisch de moeite waard maakt.
Bronvermelding: Kahland, T., Lindenwald, D.L., Jeschke, M. et al. Generation of marmoset monkeys with a non-mosaic disruption of the OTOF gene as a model of human deafness. Nat Commun 17, 3033 (2026). https://doi.org/10.1038/s41467-026-71047-1
Trefwoorden: genetische doofheid, marmosetmodel, gentherapie, auditieve synaptopathie, CRISPR-bewerking