Clear Sky Science · zh
噬菌体外显子核酸内切酶放大抗防御基因以规避细菌免疫
病毒如何智胜细菌防御
细菌与感染它们的病毒(称为噬菌体)处于微观的军备竞赛中。细菌不断进化出新的方式来检测并阻止入侵的噬菌体,而噬菌体则进化出对策以绕过这些防御。该研究揭示了一种出人意料的病毒伎俩:某些噬菌体能够迅速复制并放大自身基因组中的特定片段,这些片段有助于击败不同的细菌免疫系统,从而在最需要时放大它们的抗防御工具的“音量”。
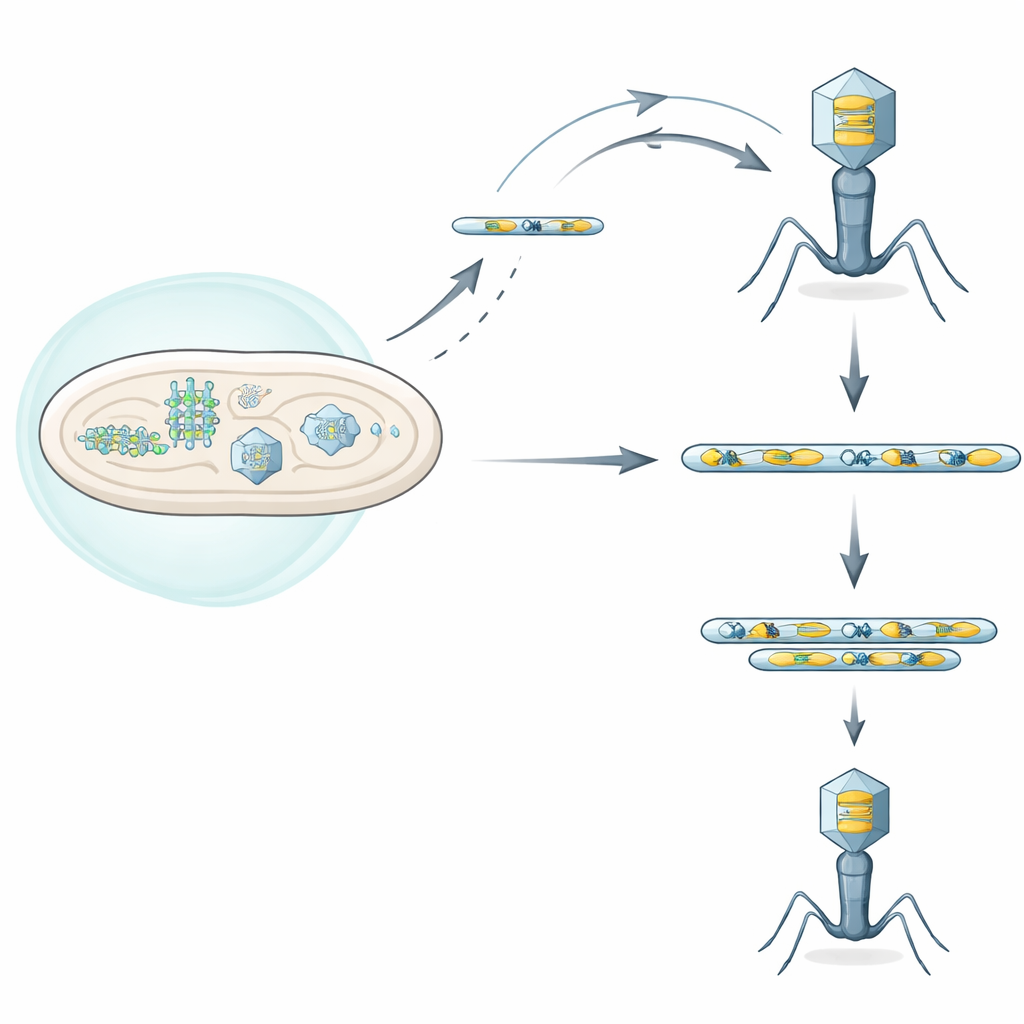
细菌防护与病毒攻击之间的对决
细菌携带多种防御系统,能够感知病毒感染并将其阻断,有时甚至会杀死被感染的细胞以保护更广泛的群体。作者关注了一种名为 Septu 的防御系统,该系统存在于一个临床分离株的Escherichia coli中。Septu 攻击一种小而关键的分子——用于将遗传密码翻译为蛋白质的转移 RNA(tRNA)。通过切割这种 tRNATyr,Septu 剥夺了细胞和入侵噬菌体进行蛋白质合成所需的关键成分,从而停止病毒复制。然而一些噬菌体仍能在 Septu 存在下繁殖,这表明它们已进化出巧妙的逃逸路线。
作为病毒备用供应的额外 tRNA 副本
研究人员以一种被称为 T6 的 T-系列噬菌体为对象,分离出能够在 Septu 存在下复制的罕见“逃逸”突变体。当他们对这些病毒基因组进行测序时,并未发现所有逃逸体都有一个共同的整齐突变。相反,他们发现每个逃逸噬菌体都大幅放大了一个包含两个特征的短 DNA 片段:完整的 tRNATyr 基因和邻近的一个名为 segB 的基因,该基因编码一种外显子核酸内切酶(一种切割 DNA 的蛋白质)。这些被放大的片段形成串联重复,就像同一段落被连续粘贴多次。额外的副本提升了 tRNATyr 的产生,提供了足够的 tRNA 来抵消 Septu 的切割活性,从而使病毒复制得以恢复。
驱动基因组扩展的 DNA 切割酶
团队随后探究 SegB 是否仅仅是该放大区域中的“乘客”,抑或是真正驱动这一过程的因素。通过让噬菌体在缺失 SegB 或携带失活版本的情况下进化,他们证明只有具有正常功能 SegB 的噬菌体才能在免疫压力下构建这些 DNA 重复。生化测试证实,SegB 会切割噬菌体基因组中的特定位点,通常靠近 tRNA 基因。在 SegB 引入断裂之后,病毒的重组机制可以以意外的方式重新连接 DNA,从而复制附近的片段。当存在 Septu 时,恰巧获得更多 tRNATyr 副本的变体具有强烈的生存优势并迅速在噬菌体群体中占据主导。一旦防御压力消失,这些额外副本往往会回落,表明这些扩增是动态且可逆的。
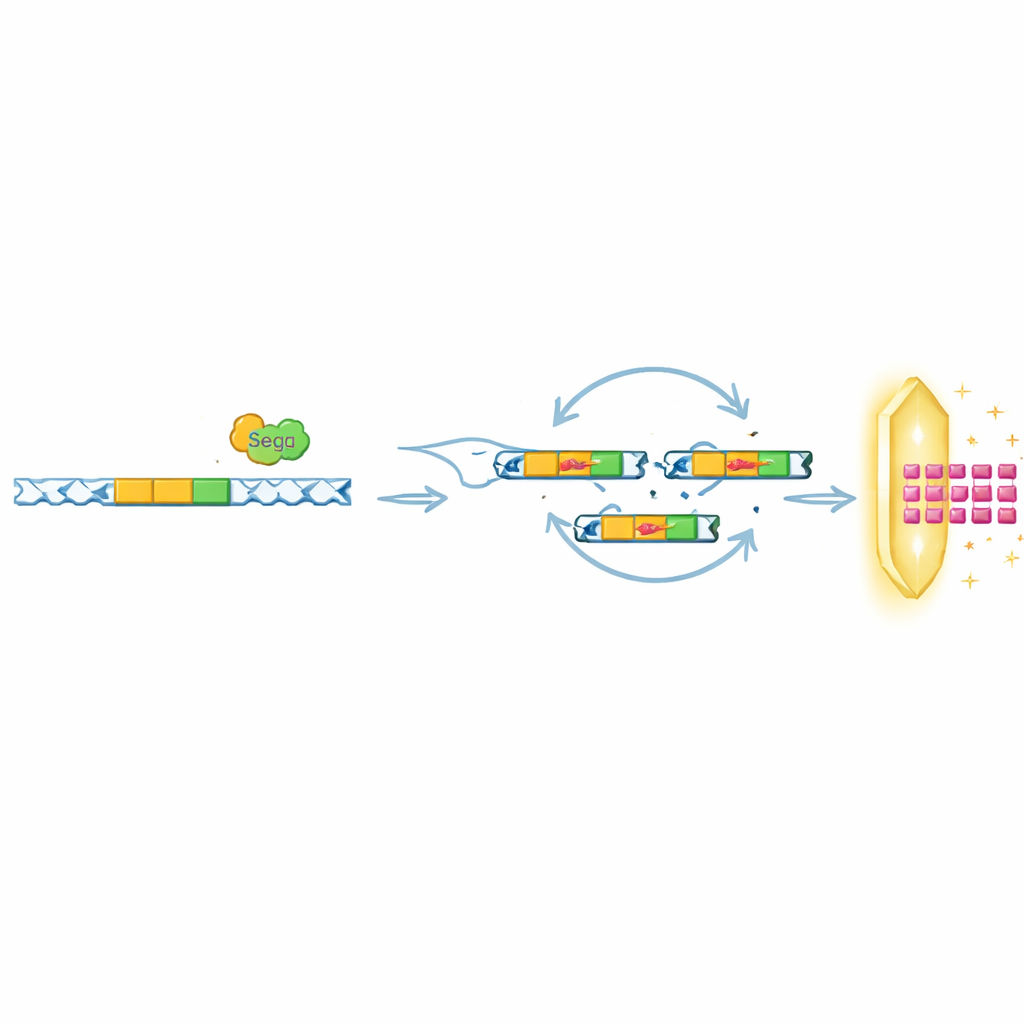
对不同防御重复使用同一伎俩
有趣的是,研究人员发现 SegB 的作用不仅限于帮助 T6 绕过 Septu。在其他实验中,他们让噬菌体面对不同的细菌系统,包括 OLD 和 ToxIN,这些系统也以截然不同的方式阻止感染。在 OLD 压力下,SegB 驱动了远端 DNA 区域的放大,该区域编码一个小型病毒蛋白 Gp49.2,能与 OLD 防御蛋白结合并抑制其功能。在相关噬菌体面临 ToxIN 压力时,SegB 则被证明对于放大另一种抗防御基因 tifA 所必需。在公共数据库中的许多噬菌体基因组中,类似 SegB 的基因常常位于 tRNA 群附近,这表明将 DNA 切割与局部或远程基因放大耦合的策略在自然界中可能广泛存在。
这对病毒—细菌军备竞赛意味着什么
对非专业读者而言,关键信息是:一些病毒并不只是等待缓慢的单字母突变来适应。相反,它们可以像手风琴一样快速“拉长”基因组的部分区域,在受到攻击时复制有用基因的多个副本,并在不再需要这些副本时再收缩。在本例中,一种称为 SegB 的 DNA 切割酶触发了基因组重排,放大了 tRNA 基因和其他抗防御因子,使噬菌体能够克服若干不同的细菌免疫系统。这揭示了一种灵活且快速反应的策略,帮助病毒在与细菌的对抗中始终保持一步领先。
引用: Chihara, K., Azam, A.H., Egorov, A.A. et al. Phage homing endonuclease amplifies anti-defense genes to evade bacterial immunity. Nat Commun 17, 3468 (2026). https://doi.org/10.1038/s41467-026-71036-4
关键词: 噬菌体免疫, 细菌抗病毒防御, 基因组扩增, 外显子核酸内切酶, 噬菌体–细菌军备竞赛