Clear Sky Science · es
La endonucleasa de homing de fagos amplifica genes anti‑defensa para eludir la inmunidad bacteriana
Cómo los virus superan las defensas bacterianas
Las bacterias y los virus que las infectan, llamados fagos, están inmersos en una carrera armamentística microscópica. Las bacterias desarrollan nuevas formas de detectar y bloquear fagos invasores, mientras que los fagos evolucionan contramedidas para burlar esas defensas. Este estudio desvela una táctica viral sorprendente: algunos fagos pueden copiar y amplificar rápidamente segmentos concretos de su propio ADN que les ayudan a vencer distintos sistemas inmunitarios bacterianos, aumentando efectivamente la dosis de sus herramientas anti‑defensa justo cuando más las necesitan.
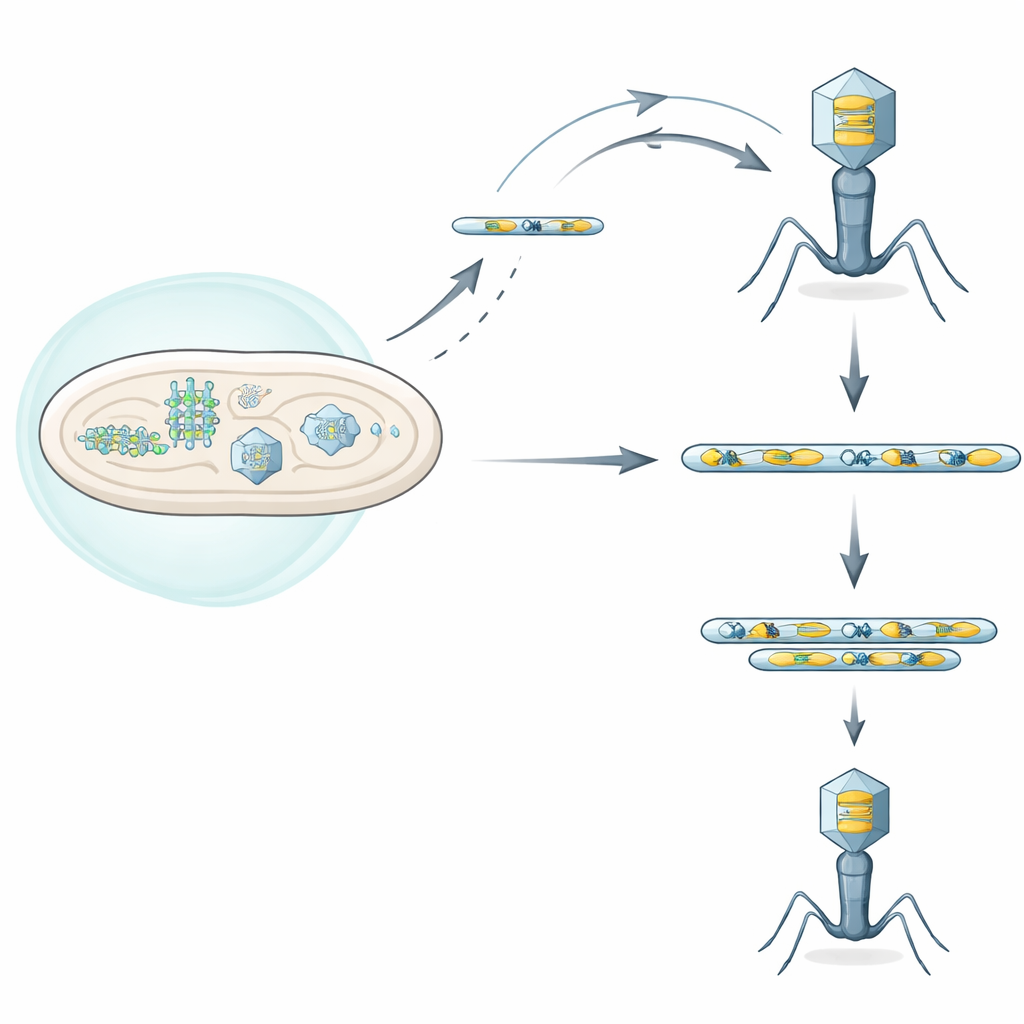
Un duelo entre escudos bacterianos y atacantes virales
Las bacterias poseen numerosos sistemas de defensa que detectan la infección viral y la interrumpen, a veces incluso matando la célula infectada para proteger a la población en conjunto. Los autores se centraron en uno de esos sistemas, llamado Septu, presente en una cepa clínica de Escherichia coli. Septu ataca una molécula pequeña pero vital, un ARN de transferencia (ARNt) necesario para traducir el código genético en proteínas. Al cortar este tRNATyr, Septu priva tanto a la célula como al fago invasor de un ingrediente clave para la síntesis proteica, deteniendo la replicación viral. Aun así, algunos fagos consiguen crecer pese a Septu, lo que sugiere que han desarrollado vías de escape ingeniosas.
Copias adicionales de ARNt como suministro de respaldo viral
Trabajando con un fago tipo T conocido como T6, los investigadores aislaron raros mutantes “de escape” capaces de replicarse en presencia de Septu. Al secuenciar estos genomas virales, no encontraron una única mutación común a todos los escapistas. En su lugar, descubrieron que cada fago de escape había amplificado masivamente un segmento corto de ADN que contenía dos elementos: el gen completo de tRNATyr y un gen cercano llamado segB, que codifica una endonucleasa de homing, una proteína que corta ADN. Estos segmentos amplificados formaban repeticiones en tándem, como un mismo párrafo pegado muchas veces seguidas. Las copias adicionales aumentaron la producción de tRNATyr, proporcionando suficiente ARNt para compensar la actividad cortante de Septu y permitiendo que la replicación viral se reanudara.
Una enzima cortadora de ADN que impulsa la expansión del genoma
El equipo se preguntó entonces si SegB era simplemente un pasajero en esta región amplificada o el impulsor del proceso. Al evolucionar fagos carentes de SegB, o que portaban una versión inactiva de la proteína, mostraron que solo los fagos con SegB funcional podían construir estas repeticiones de ADN bajo presión inmune. Pruebas bioquímicas confirmaron que SegB corta en sitios específicos del genoma del fago, con frecuencia cerca de genes de ARNt. Tras las roturas introducidas por SegB, la maquinaria de recombinación viral puede volver a unir el ADN de formas que accidentalmente duplican segmentos cercanos. Cuando Septu está presente, las variantes que por casualidad ganan más copias de tRNATyr obtienen una fuerte ventaja de supervivencia y rápidamente dominan la población fagica. Una vez que la presión defensiva desaparece, estas copias adicionales tienden a colapsar, lo que muestra que las amplificaciones son dinámicas y reversibles.
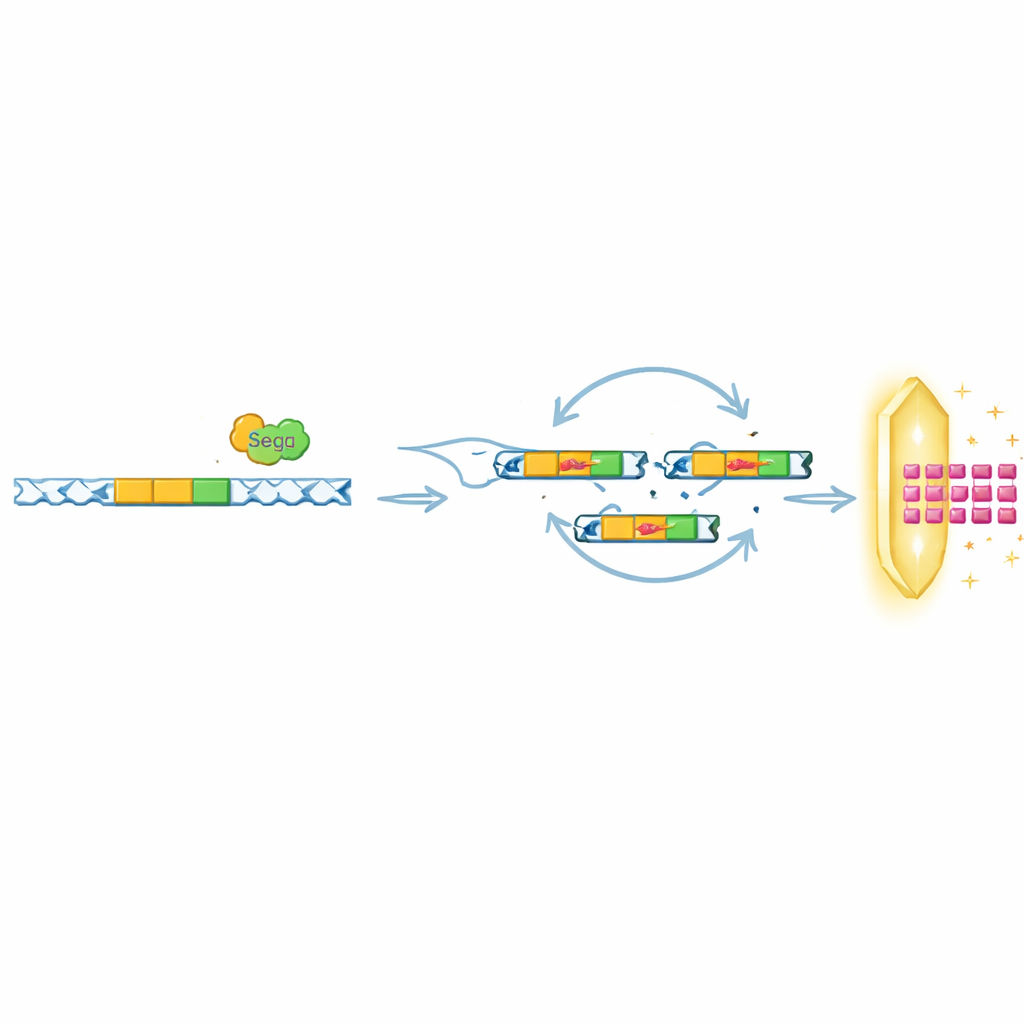
Reutilizar la misma táctica contra diferentes defensas
De forma intrigante, los investigadores comprobaron que el papel de SegB va más allá de ayudar a T6 a eludir a Septu. En otros experimentos, sometieron a los fagos a distintos sistemas bacterianos, incluidos OLD y ToxIN, que también bloquean la infección pero por mecanismos muy diferentes. Bajo la presión de OLD, SegB impulsó la amplificación de una región distante del ADN que codifica una pequeña proteína viral, Gp49.2, que se une físicamente e inhibe la proteína defensiva OLD. Bajo la presión de ToxIN en un fago relacionado, SegB fue necesario para amplificar otro gen anti‑defensa, tifA. En muchos genomas de fagos disponibles en bases de datos públicas, genes como SegB se encontraron con frecuencia próximos a cúmulos de ARNt, lo que sugiere que esta estrategia de acoplar el corte de ADN con amplificaciones locales o a larga distancia puede ser común en la naturaleza.
Qué significa esto para la carrera armamentística virus–bacteria
Para un público no especializado, el mensaje clave es que algunos virus no se limitan a esperar lentas mutaciones de una sola letra en su ADN para adaptarse. En lugar de eso, pueden “estirar” rápidamente partes de su genoma como un acordeón, creando múltiples copias adicionales de genes útiles cuando están bajo ataque y reduciéndolas cuando ya no hacen falta. En este caso, una enzima cortadora de ADN llamada SegB desencadena reorganizaciones del genoma que amplifican genes de ARNt y otros factores anti‑defensa, permitiendo a los fagos superar varios sistemas inmunitarios bacterianos. Esto revela una estrategia flexible y de respuesta rápida que ayuda a los virus a mantenerse un paso por delante en su batalla con las bacterias.
Cita: Chihara, K., Azam, A.H., Egorov, A.A. et al. Phage homing endonuclease amplifies anti-defense genes to evade bacterial immunity. Nat Commun 17, 3468 (2026). https://doi.org/10.1038/s41467-026-71036-4
Palabras clave: inmunidad de bacteriófagos, defensa antiviral bacteriana, amplificación del genoma, endonucleasa de homing, carrera armamentística fago–bacteria