Clear Sky Science · sv
Faghoming-endonukleas förstärker anti-försvarsgener för att undkomma bakteriellt immunförsvar
Hur virus överlistar bakteriella försvar
Bakterier och de virus som infekterar dem, så kallade fager, är inbegripna i ett mikroskopiskt vapenlopp. Bakterier utvecklar nya sätt att upptäcka och blockera invaderande fager, medan fager utvecklar motdrag för att slingra sig förbi dessa försvar. Denna studie avslöjar ett överraskande viralt knep: vissa fager kan snabbt kopiera och förstärka specifika delar av sitt eget DNA som hjälper dem att slå olika bakterieimmunsystem, vilket i praktiken höjer volymen på deras anti-försvarsverktyg just när de behöver dem som mest.
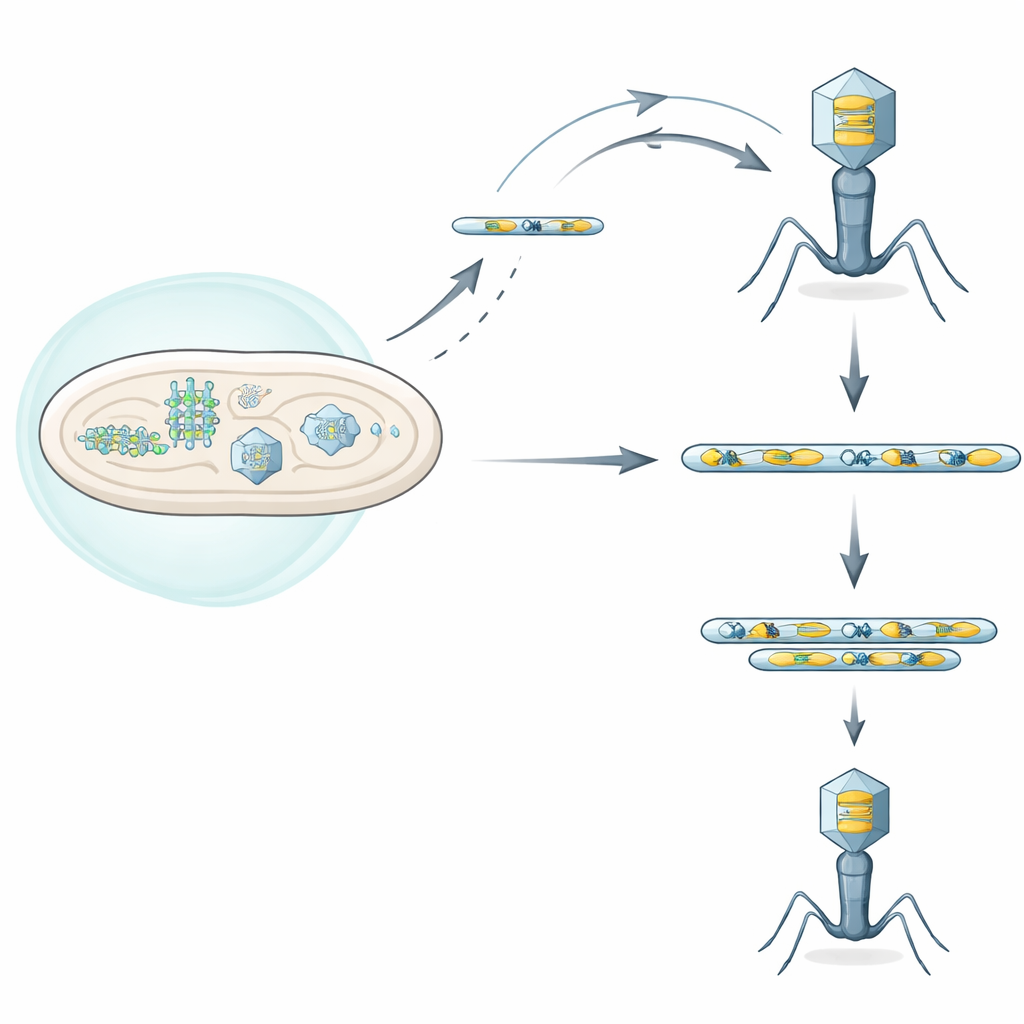
En duell mellan bakteriella sköldar och virala angripare
Bakterier bär på många försvarssystem som känner igen virusinfektioner och slår ner dem, ibland genom att döda den infekterade cellen för att skydda populationen i stort. Författarna fokuserade på ett sådant system, kallat Septu, som hittas i en klinisk stam av Escherichia coli. Septu angriper en liten men livsviktig molekyl, en transfer-RNA (tRNA) som behövs för att översätta den genetiska koden till proteiner. Genom att klippa detta tRNATyr svälter Septu både cellen och den invaderande fagen på en nyckelingrediens för proteinsyntes, vilket stoppar viral replikation. Ändå lyckas vissa fager fortfarande växa trots Septu, vilket antyder att de har utvecklat smarta flyktvägar.
Extra tRNA-kopior som viral reserv
Genom att arbeta med en T-even-fag känd som T6 isolerade forskarna sällsynta ”flykt”mutanter som kunde replikera i närvaro av Septu. När de sekvenserade dessa virala genom hittade de ingen enstaka, tydlig mutation som delades av alla flyktmutanter. Istället upptäckte de att varje flyktfag hade massivt förstärkt ett kort DNA-segment som innehöll två element: hela tRNATyr-genen och en närliggande gen kallad segB, som kodar för ett homing-endonukleas, ett DNA-klippande protein. Dessa förstärkta segment bildade tandemrepetitioner, som samma stycke inklistrat många gånger i följd. De extra kopiorna ökade tRNATyr-produktionen, vilket gav tillräckligt med tRNA för att övervinna Septus klyvningsaktivitet och gjorde det möjligt för viral replikation att återupptas.
En DNA-klippande enzym som driver genomexpansion
Teamet undrade sedan om SegB bara var en passagerare i detta amplifierade område eller drivkraften bakom processen. Genom att evolvera fager som saknade SegB, eller som bar en inaktiverad version av proteinet, visade de att endast fager med en fungerande SegB kunde bygga dessa DNA-repetitioner under immunsystemets tryck. Biokemiska tester bekräftade att SegB klipper specifika platser i faggenomet, ofta nära tRNA-gener. Efter att SegB inför brott kan den virala rekombinationsmaskineriet återfoga DNA på sätt som oavsiktligt duplicerar närliggande segment. När Septu är närvarande har varianter som råkar få fler tRNATyr-kopior en stark överlevnadsfördel och tar snabbt över fagpopulationen. När försvarstrycket tas bort tenderar dessa extra kopior att kollapsa igen, vilket visar att förstärkningarna är dynamiska och reversibla.
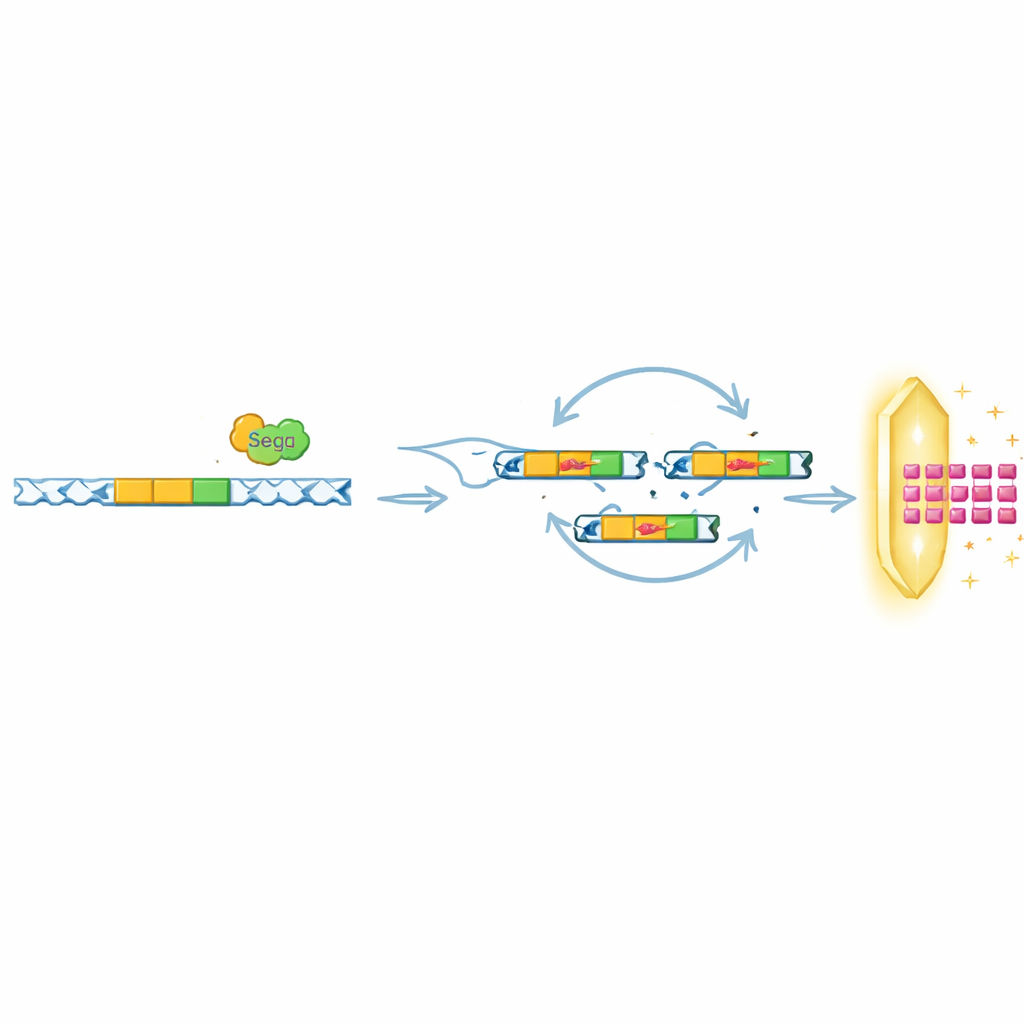
Återanvändning av samma trick mot olika försvar
Intressant nog fann forskarna att SegB:s roll sträcker sig bortom att hjälpa T6 att överlista Septu. I andra experiment utsatte de fager för olika bakteriella system, inklusive OLD och ToxIN, som också blockerar infektion men på mycket olika sätt. Under OLD-tryck drev SegB förstärkning av en avlägsen DNA-region som kodar för ett litet viralt protein, Gp49.2, som fysiskt binder till och hämmar OLD-försvarsproteinet. Under ToxIN-tryck i en närbesläktad fag krävdes SegB för att förstärka ännu en anti-försvarsgen, tifA. I många faggenom i offentliga databaser hittades gener som SegB ofta nära tRNA-kluster, vilket tyder på att denna strategi att koppla DNA-klippning till lokal eller långdistans genförstärkning kan vara utbredd i naturen.
Vad detta betyder för virus–bakterie vapenlopp
För en icke-specialist är huvudbudskapet att vissa virus inte bara väntar på långsamma, enstaka bokstavsmutationer i sitt DNA för att anpassa sig. Istället kan de snabbt ”sträcka” delar av sitt genom som ett dragspel, skapa flera extra kopior av hjälpsamma gener under angrepp och krympa tillbaka när kopiorna inte längre behövs. I detta fall utlöser ett DNA-klippande enzym kallat SegB genomomarrangemang som förstärker tRNA-gener och andra anti-försvarsfaktorer, vilket låter fager övermanna flera olika bakteriella immunsystem. Detta avslöjar en flexibel, snabbresponstrategi som hjälper virus att ligga ett steg före i sin kamp med bakterier.
Citering: Chihara, K., Azam, A.H., Egorov, A.A. et al. Phage homing endonuclease amplifies anti-defense genes to evade bacterial immunity. Nat Commun 17, 3468 (2026). https://doi.org/10.1038/s41467-026-71036-4
Nyckelord: bakteriofag-immunitet, bakteriellt antiviralt försvar, genomförstärkning, homing-endonukleas, fag–bakterie vapenlopp