Clear Sky Science · pl
Endonukleaza homingowa fagów amplifikuje geny antyobronne, by unikać odporności bakterii
Jak wirusy przechytrzają obronę bakterii
Bakterie i wirusy, które je infekują — zwane fagami — toczą mikroskopijny wyścig zbrojeń. Bakterie rozwijają nowe sposoby wykrywania i blokowania napadających fagów, podczas gdy fagi ewoluują kontrruchy, by wymknąć się tym mechanizmom. W tym badaniu odkryto zaskakujący chwyt wirusowy: niektóre fagi potrafią szybko kopiować i amplifikować określone fragmenty własnego DNA, które pomagają im pokonać różne systemy odpornościowe bakterii, efektywnie zwiększając „głośność” swoich narzędzi antyobronnych właśnie wtedy, gdy są najbardziej potrzebne.
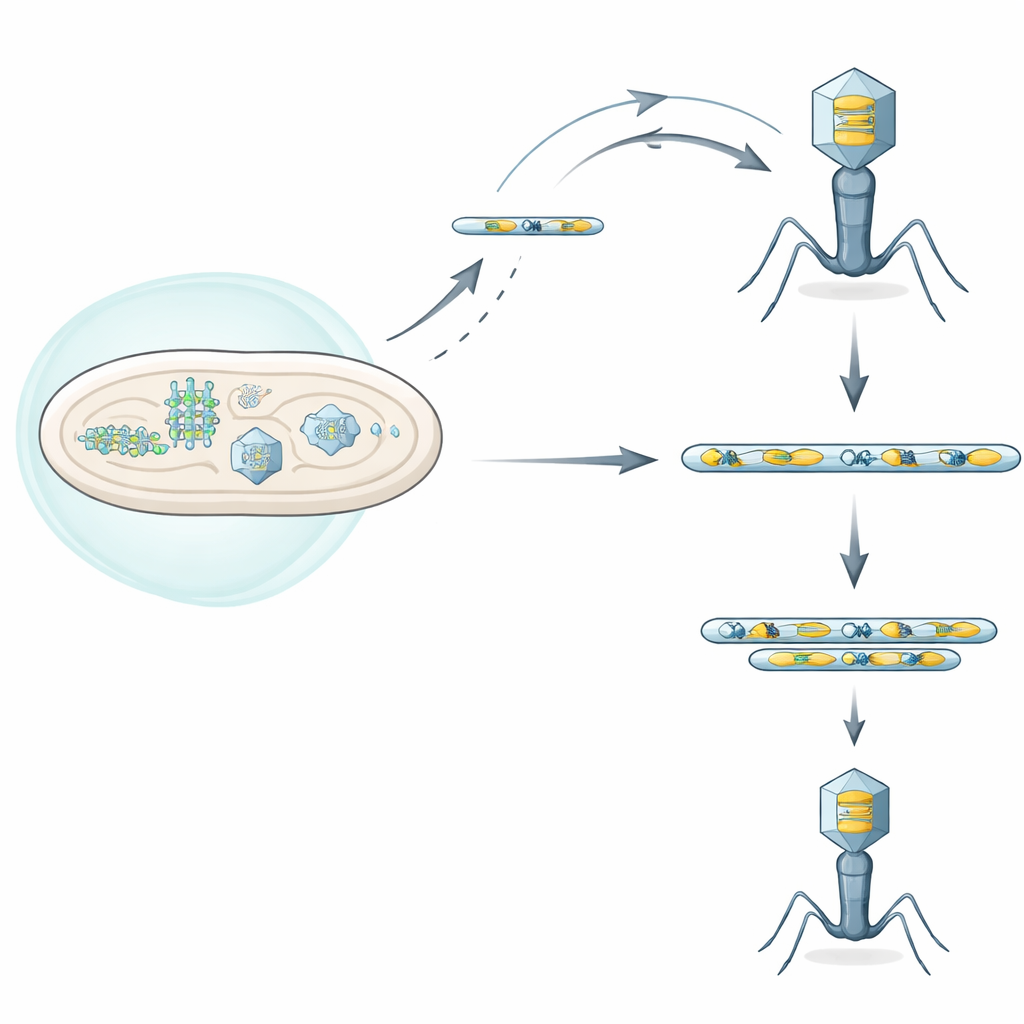
Pojedynek między bakteryjnymi tarczami a wirusowymi najeźdźcami
Bakterie posiadają liczne systemy obronne, które wykrywają infekcję wirusową i ją zatrzymują, czasem nawet zabijając zakażoną komórkę, by chronić populację. Autorzy skupili się na jednym takim systemie, nazwanym Septu, występującym w klinicznym szczepie Escherichia coli. Septu atakuje małą, lecz kluczową cząsteczkę — tRNA (tRNA) potrzebne do tłumaczenia kodu genetycznego na białka. Poprzez cięcie tego tRNATyr, Septu pozbawia zarówno komórkę, jak i napadający faga, niezbędnego składnika syntezy białek, zatrzymując replikację wirusa. A jednak niektórym fagom udaje się rosnąć pomimo działania Septu, co sugeruje, że wykształciły sprytne drogi ucieczki.
Dodatkowe kopie tRNA jako zapas wirusowy
Pracując z fagiem z grupy T-even znanym jako T6, badacze wyizolowali rzadkie „ucieczkowe” mutanty, które potrafiły replikować się w obecności Septu. Sekwencjonując te genomy wirusowe, nie znaleźli pojedynczej, wspólnej mutacji we wszystkich uciekinierach. Zamiast tego odkryli, że każdy fag-uciekinier masywnie amplifikował krótki odcinek DNA zawierający dwie cechy: pełny gen tRNATyr oraz pobliski gen nazwany segB, kodujący endonukleazę homingową — białko tnące DNA. Te amplifikowane segmenty tworzyły tandemowe powtórzenia, niczym ten sam akapit wklejony wiele razy z rzędu. Dodatkowe kopie zwiększały produkcję tRNATyr, dostarczając wystarczającej ilości tRNA, by przezwyciężyć cięcie przez Septu i umożliwić wznówienie replikacji wirusa.
Enzym tnący DNA napędzający ekspansję genomu
Zespół zadał następnie pytanie, czy SegB jest jedynie pasażerem w tej amplifikowanej strefie, czy też głównym sprawcą procesu. Ewoluując fagi pozbawione SegB lub niosące inaktywną wersję białka, wykazali, że tylko fagi z funkcjonalnym SegB potrafiły tworzyć te powtórzenia DNA pod presją odporności. Testy biochemiczne potwierdziły, że SegB tnie w określonych miejscach genomu faga, często w pobliżu genów tRNA. Po wprowadzeniu przez SegB przerw, wirusowy aparat rekombinacyjny może łączyć DNA w sposób, który przypadkowo duplikuje pobliskie fragmenty. Gdy obecny jest Septu, warianty, które przypadkowo zyskują więcej kopii tRNATyr, mają dużą przewagę przeżyciową i szybko dominują populację fagów. Po ustaniu presji obronnej te dodatkowe kopie zwykle się redukują, pokazując, że amplifikacje są dynamiczne i odwracalne.
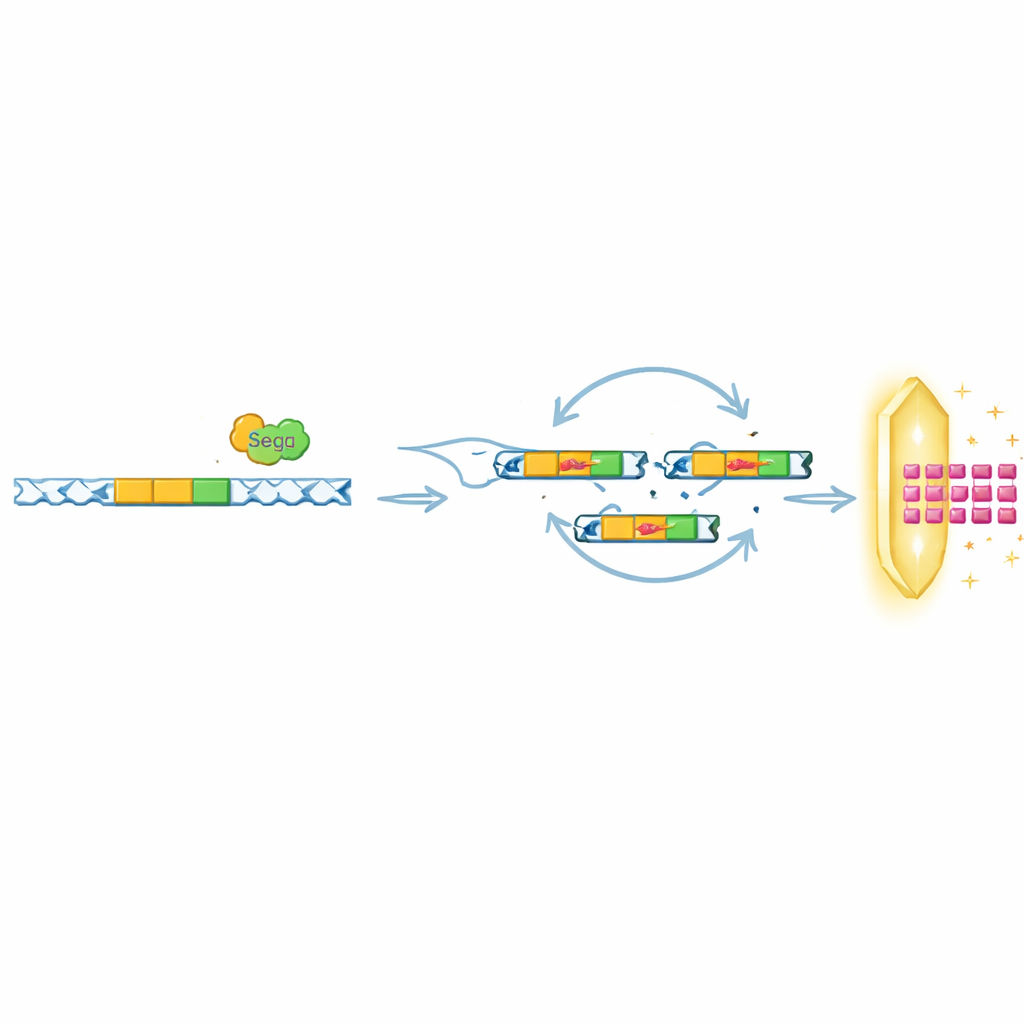
Powtarzanie tego samego chwyta przeciw różnym obronom
Co ciekawe, badacze stwierdzili, że rola SegB wykracza poza pomoc T6 w obejściu Septu. W innych eksperymentach wystawiali fagi na działanie różnych bakteryjnych systemów, w tym OLD i ToxIN, które także blokują infekcję, ale w zupełnie inny sposób. Pod presją OLD SegB napędzał amplifikację odległego regionu DNA kodującego małe białko wirusowe Gp49.2, które fizycznie wiąże się i hamuje białko obronne OLD. Pod presją ToxIN w spokrewnionym fagu SegB był wymagany do amplifikacji kolejnego genu antyobronnego, tifA. W wielu genomach fagów z publicznych baz danych geny podobne do SegB często występowały w pobliżu klastrów tRNA, co sugeruje, że ta strategia sprzęgania cięcia DNA z lokalną lub dalekosiężną amplifikacją genów może być powszechna w przyrodzie.
Co to oznacza dla wyścigu zbrojeń wirus–bakteria
Dla czytelnika nietechnicznego kluczowy przekaz jest taki, że niektóre wirusy nie czekają wyłącznie na powolne, punktowe mutacje w swoim DNA, by się przystosować. Zamiast tego potrafią szybko „rozciągać” części swojego genomu niczym akordeon, tworząc wiele dodatkowych kopii przydatnych genów pod atakiem i kurcząc się z powrotem, gdy kopie przestają być potrzebne. W tym przypadku endonukleaza tnąca DNA nazwana SegB zapoczątkowuje przegrupowania genomowe, które amplifikują geny tRNA i inne czynniki antyobronne, pozwalając fagom pokonać kilka różnych bakteryjnych systemów odpornościowych. Odkrycie to ujawnia elastyczną, szybkoreagującą strategię, która pomaga wirusom utrzymać przewagę w ich starciu z bakteriami.
Cytowanie: Chihara, K., Azam, A.H., Egorov, A.A. et al. Phage homing endonuclease amplifies anti-defense genes to evade bacterial immunity. Nat Commun 17, 3468 (2026). https://doi.org/10.1038/s41467-026-71036-4
Słowa kluczowe: odporność bakteriofagów, bakteryjna obrona antywirusowa, amplifikacja genomu, endonukleaza homingowa, wyścig zbrojeń bakterie–fagi