Clear Sky Science · it
L’endonucleasi di omingizzazione del fago amplifica geni anti-difesa per eludere l’immunità batterica
Come i virus sovrastano le difese batteriche
I batteri e i virus che li infettano, chiamati fagi, sono impegnati in una corsa agli armamenti a scala microscopica. I batteri evolvono nuovi modi per rilevare e bloccare i fagi invasori, mentre i fagi sviluppano contromosse per sfuggire a queste difese. Questo studio rivela un trucco virale sorprendente: alcuni fagi possono copiare e amplificare rapidamente porzioni specifiche del proprio DNA che li aiutano a sconfiggere diversi sistemi immunitari batterici, aumentando di fatto la quantità dei loro strumenti anti-difesa proprio quando serve di più.
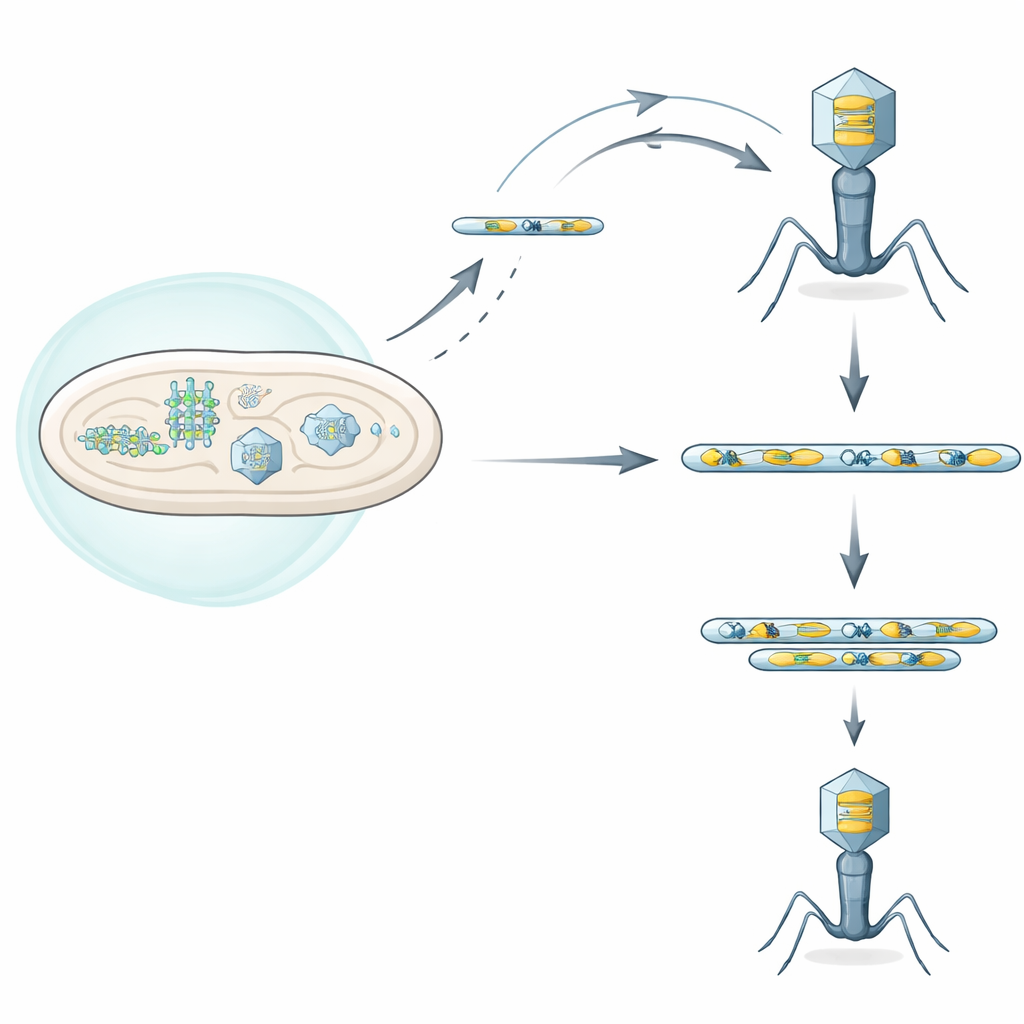
Un duello tra scudi batterici e assalitori virali
I batteri possiedono molti sistemi di difesa che rilevano l’infezione virale e la bloccano, a volte uccidendo la cellula infetta per proteggere la popolazione più ampia. Gli autori si sono concentrati su uno di questi sistemi, chiamato Septu, trovato in un ceppo clinico di Escherichia coli. Septu attacca una piccola ma vitale molecola, un RNA di trasferimento (tRNA) necessario per tradurre il codice genetico in proteine. Tagliando questo tRNATyr, Septu priva sia la cellula sia il fago invasore di un ingrediente chiave per la sintesi proteica, arrestando la replicazione virale. Eppure alcuni fagi riescono comunque a proliferare nonostante Septu, suggerendo che hanno evoluto vie di fuga ingegnose.
Copie extra di tRNA come riserva virale
Lavorando con un fago T-even noto come T6, i ricercatori hanno isolato rari mutanti “fuggitivi” in grado di replicarsi in presenza di Septu. Quando hanno sequenziato questi genomi virali, non hanno trovato una singola mutazione chiara condivisa da tutti gli scappati. Invece, hanno scoperto che ogni fago di fuga aveva amplificato massicciamente un breve segmento di DNA contenente due elementi: il gene completo per il tRNATyr e un gene vicino chiamato segB, che codifica per un’endonucleasi di omingizzazione, una proteina che taglia il DNA. Questi segmenti amplificati formavano ripetizioni in tandem, come lo stesso paragrafo incollato più volte di seguito. Le copie extra aumentavano la produzione di tRNATyr, fornendo abbastanza tRNA per superare l’attività di taglio di Septu e permettendo così la ripresa della replicazione virale.
Un enzima che taglia il DNA e guida l’espansione del genoma
Il gruppo si è poi chiesto se SegB fosse semplicemente un passeggero in questa regione amplificata o il motore del processo. Evolvendo fagi privi di SegB, o portatori di una versione inattiva della proteina, hanno dimostrato che solo i fagi con un SegB funzionante potevano costruire queste ripetizioni di DNA sotto pressione immunitaria. Test biochimici hanno confermato che SegB taglia punti specifici nel genoma del fago, spesso vicino ai geni per tRNA. Dopo che SegB introduce rotture, la macchina di ricombinazione virale può riunire il DNA in modi che duplicano accidentalmente i segmenti vicini. Quando Septu è presente, le varianti che per caso acquisiscono più copie di tRNATyr godono di un forte vantaggio di sopravvivenza e rapidamente dominano la popolazione fagica. Una volta rimossa la pressione difensiva, queste copie extra tendono a collassare di nuovo, mostrando che le amplificazioni sono dinamiche e reversibili.
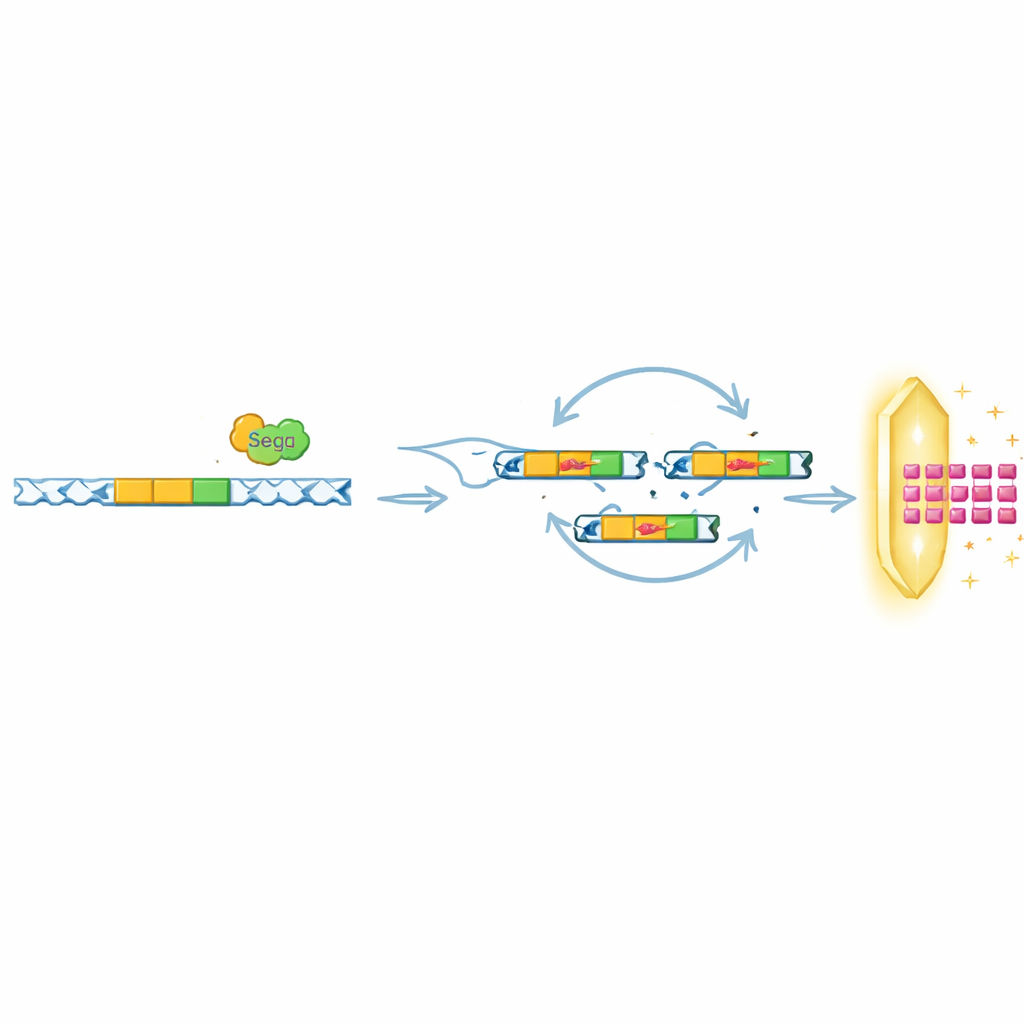
Riutilare lo stesso trucco contro difese diverse
È interessante che i ricercatori abbiano scoperto che il ruolo di SegB va oltre l’aiuto a T6 per eludere Septu. In altri esperimenti, hanno sfidato i fagi con sistemi batterici diversi, inclusi OLD e ToxIN, che bloccano l’infezione ma in modi molto differenti. Sotto la pressione di OLD, SegB ha guidato l’amplificazione di una regione di DNA distante che codifica per una piccola proteina virale, Gp49.2, che si lega fisicamente e inibisce la proteina di difesa OLD. Sotto la pressione di ToxIN in un fago correlato, SegB è stato necessario per amplificare un altro gene anti-difesa, tifA. Analizzando molti genomi fagici presenti nelle banche dati pubbliche, geni come SegB sono stati frequentemente trovati vicini a cluster di tRNA, suggerendo che questa strategia di accoppiare il taglio del DNA con amplificazioni geniche locali o a distanza potrebbe essere diffusa in natura.
Cosa significa per la corsa agli armamenti virus–batteri
Per un non specialista, il messaggio chiave è che alcuni virus non si limitano ad aspettare lente mutazioni puntiformi nel loro DNA per adattarsi. Al contrario, possono rapidamente “allungare” parti del loro genoma come una fisarmonica, creando copie multiple di geni utili quando sono sotto attacco e ridimensionandole quando non servono più. In questo caso, un’enzima che taglia il DNA chiamato SegB innesca riorganizzazioni del genoma che amplificano geni per tRNA e altri fattori anti-difesa, permettendo ai fagi di sopraffare diversi sistemi immunitari batterici. Ciò rivela una strategia flessibile e a risposta rapida che aiuta i virus a restare un passo avanti nella loro battaglia con i batteri.
Citazione: Chihara, K., Azam, A.H., Egorov, A.A. et al. Phage homing endonuclease amplifies anti-defense genes to evade bacterial immunity. Nat Commun 17, 3468 (2026). https://doi.org/10.1038/s41467-026-71036-4
Parole chiave: immunità dei bacteriofagi, difesa antivirale batterica, amplificazione del genoma, endonucleasi di omingizzazione, corsa agli armamenti fago–batterio