Clear Sky Science · nl
Fagen homing-endonuclease vergroot anti-verdedigingsgenen om bacteriële immuniteit te omzeilen
Hoe virussen bacteriële verdedigingsmechanismen te slim af zijn
Bacteriën en de virussen die ze infecteren, fagen genoemd, zitten verwikkeld in een microscopische wapenwedloop. Bacteriën ontwikkelen nieuwe manieren om binnendringende fagen te detecteren en te blokkeren, terwijl fagen tegenmaatregelen ontwikkelen om door deze verdedigingen heen te glippen. Deze studie onthult een verrassende virale truc: sommige fagen kunnen snel specifieke stukken van hun eigen DNA kopiëren en amplificeren die hen helpen verschillende bacteriële immuunsystemen te overwinnen, en zo het volume van hun anti-verdedigingsinstrumenten verhogen precies wanneer ze die het meest nodig hebben.
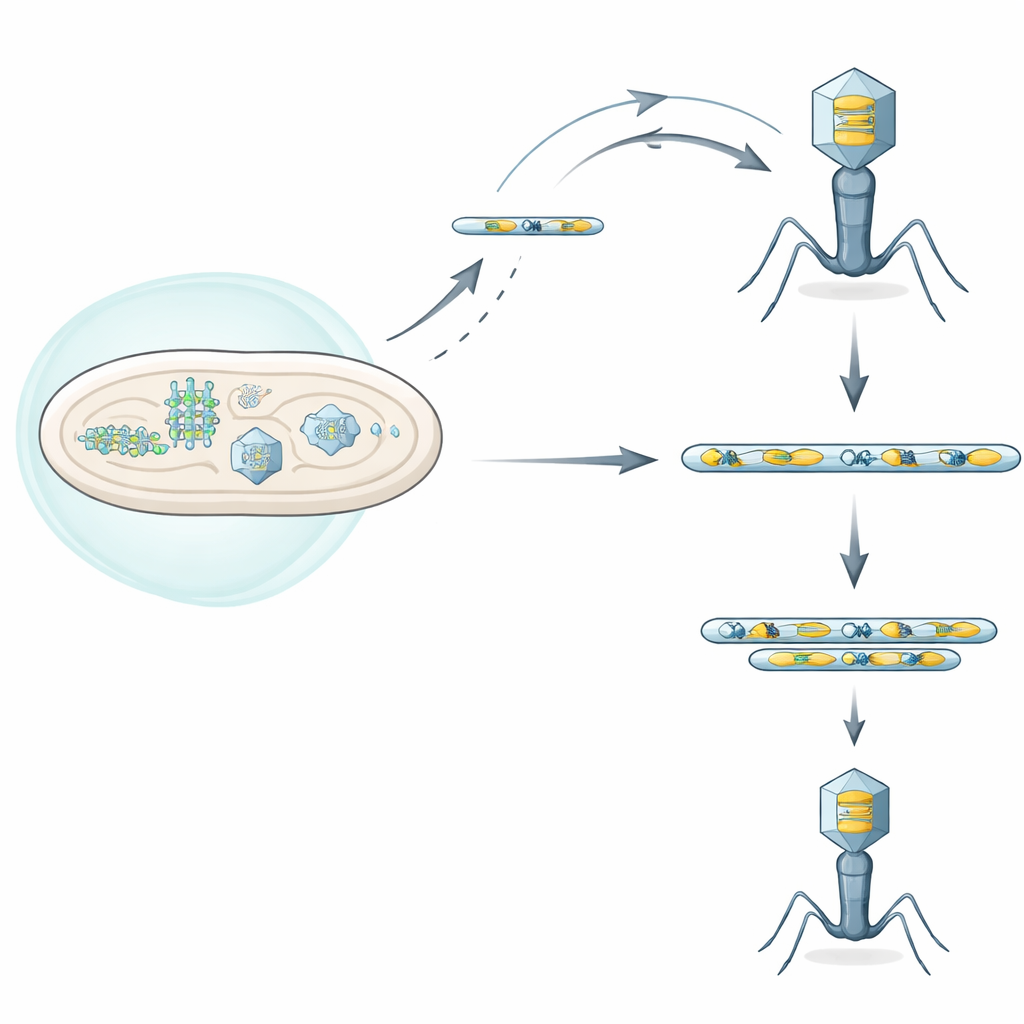
Een duel tussen bacteriële schilden en virale aanvallers
Bacteriën dragen veel verdedigingssystemen die een virale infectie waarnemen en deze neerhalen, soms zelfs door de geïnfecteerde cel te doden om de bredere populatie te beschermen. De auteurs richtten zich op een zodanig systeem, Septu genoemd, aangetroffen in een klinische stam van Escherichia coli. Septu valt een klein maar vitaal molecuul aan, een transfer-RNA (tRNA) dat nodig is om genetische code in eiwitten te vertalen. Door dit tRNATyr te knippen, berooft Septu zowel de cel als de binnendringende faag van een sleutelbestanddeel voor eiwitsynthese, waardoor virale replicatie stopt. Toch slagen sommige fagen er nog steeds in te groeien ondanks Septu, wat suggereert dat zij slimme ontsnappingsroutes hebben ontwikkeld.
Extra tRNA-kopieën als virale reservevoorraad
Werkend met een T-even faag bekend als T6 isoleerden de onderzoekers zeldzame “ontsnappings”-mutanten die konden repliceren in aanwezigheid van Septu. Toen ze deze virale genoomsequenties analyseerden, vonden ze niet één nette mutatie die alle ontsnappers gemeen hadden. In plaats daarvan ontdekten ze dat elke ontsnappende faag een enorme amplificatie had van een kort DNA-segment met twee kenmerken: het volledige tRNATyr-gen en een nabijgelegen gen genaamd segB, dat codeert voor een homing-endonuclease, een DNA-knippend eiwit. Deze versterkte segmenten vormden tandemherhalingen, alsof dezelfde alinea vele malen achter elkaar was geplakt. De extra kopieën verhoogden de productie van tRNATyr, leverden voldoende tRNA om Septu’s knipactiviteit te boven te komen en maakten hervatting van virale replicatie mogelijk.
Een DNA-knipend enzym dat genoomuitbreiding aandrijft
Het team vroeg zich vervolgens af of SegB slechts passagier was in dit geamplificeerde gebied of de aandrijver van het proces. Door fagen te laten evolueren die SegB misten of een uitgeschakelde versie van het eiwit droegen, toonden ze aan dat alleen fagen met een werkende SegB deze DNA-herhalingen konden opbouwen onder immuun-druk. Biochemische tests bevestigden dat SegB op specifieke plaatsen in het faaggenoom knipt, vaak in de buurt van tRNA-genen. Nadat SegB breuken in het DNA introduceert, kan de virale recombinatiemachinerie het DNA op manieren herverbinden die per ongeluk nabije segmenten dupliceren. Wanneer Septu aanwezig is, hebben varianten die toevallig meer tRNATyr-kopieën krijgen een sterk overlevingsvoordeel en nemen ze snel de faagpopulatie over. Zodra de verdedigingsdruk verdwijnt, neigen deze extra kopieën ertoe weer in te storten, wat aantoont dat de amplificaties dynamisch en omkeerbaar zijn.
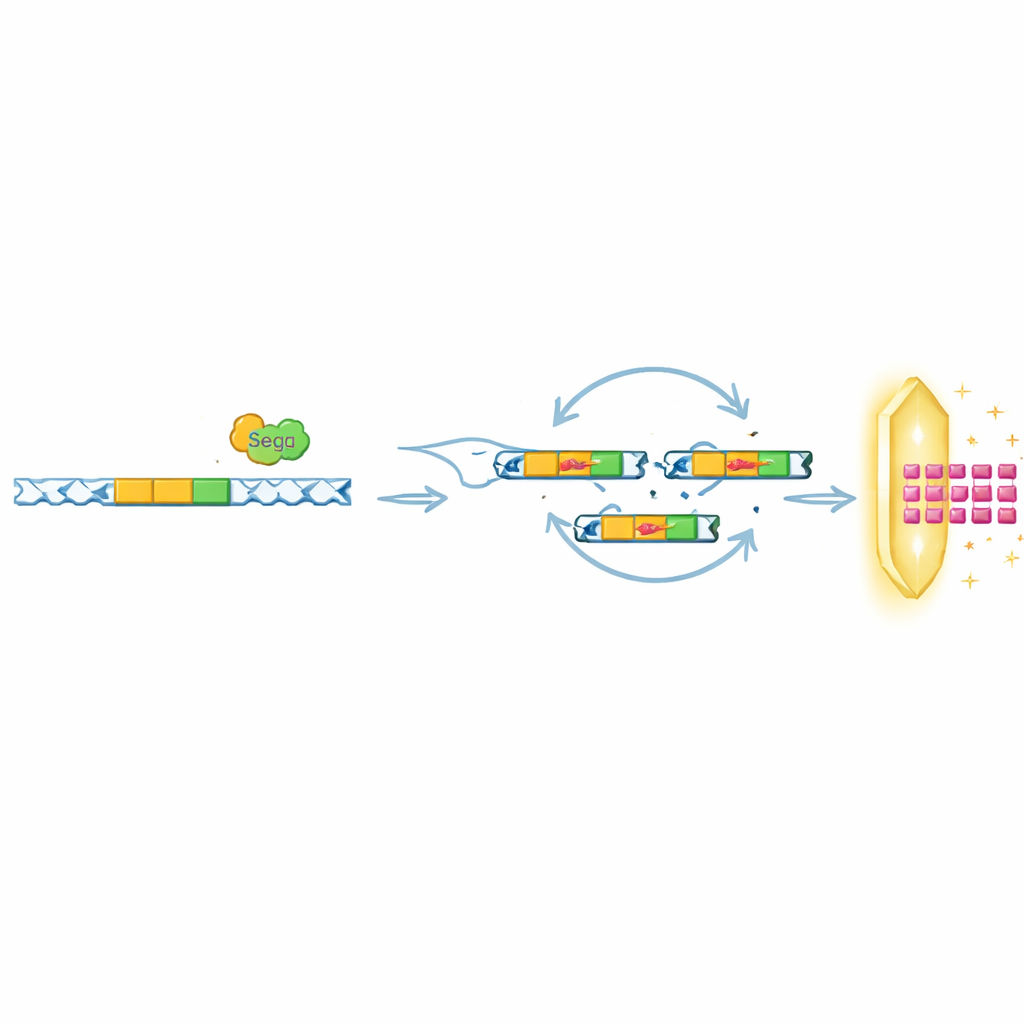
Dezelfde truc hergebruiken tegen verschillende verdedigingen
Intrigerend genoeg vonden de onderzoekers dat SegB’s rol verder reikt dan het helpen van T6 om Septu te slim af te zijn. In andere experimenten daagden ze fagen uit met verschillende bacteriële systemen, waaronder OLD en ToxIN, die ook infectie blokkeren maar op heel verschillende manieren. Onder OLD-druk dreef SegB amplificatie van een verderop gelegen DNA-regio aan die codeert voor een klein viraal eiwit, Gp49.2, dat fysiek bindt aan en het OLD-verdedigingseiwit remt. Onder ToxIN-druk in een verwante faag was SegB vereist voor het amplificeren van weer een ander anti-verdedigingsgen, tifA. In veel faaggenomen uit openbare databases werden genen zoals SegB vaak dicht bij tRNA-clusters aangetroffen, wat suggereert dat deze strategie van het koppelen van DNA-knippen aan lokale of langeafstandsgene-amplificatie wijdverspreid in de natuur kan zijn.
Wat dit betekent voor de virus–bacterie wapenwedloop
Voor niet-specialisten is de kernboodschap dat sommige virussen niet simpelweg wachten op trage, enkelletterige mutaties in hun DNA om zich aan te passen. In plaats daarvan kunnen ze delen van hun genoom snel “uitrekken” als een accordeon, meerdere extra kopieën van nuttige genen maken wanneer ze worden aangevallen en weer inkrimpen wanneer die kopieën niet langer nodig zijn. In dit geval laat een DNA-knipend enzym genaamd SegB genoomherschikkingen ontstaan die tRNA-genen en andere anti-verdedigingsfactoren amplificeren, waardoor fagen meerdere verschillende bacteriële immuunsystemen kunnen overwinnen. Dit onthult een flexibele, snel reagerende strategie die virussen helpt een stap voor te blijven in hun strijd met bacteriën.
Bronvermelding: Chihara, K., Azam, A.H., Egorov, A.A. et al. Phage homing endonuclease amplifies anti-defense genes to evade bacterial immunity. Nat Commun 17, 3468 (2026). https://doi.org/10.1038/s41467-026-71036-4
Trefwoorden: bacteriofaagimmuniteit, bacteriële antivirale verdediging, genoomamplificatie, homing-endonuclease, faag–bacterie wapenwedloop