Clear Sky Science · pt
Endonuclease de homing de fago amplia genes anti-defesa para evadir a imunidade bacteriana
Como vírus driblam defesas bacterianas
Bactérias e os vírus que as infectam, chamados fagos, estão travados em uma corrida armamentista microscópica. As bactérias evoluem novas maneiras de detectar e bloquear fagos invasores, enquanto os fagos desenvolvem contra-medidas para escapar dessas defesas. Este estudo revela um truque viral surpreendente: alguns fagos podem copiar e amplificar rapidamente trechos específicos de seu próprio DNA que os ajudam a derrotar diferentes sistemas imunes bacterianos, efetivamente aumentando a potência de suas ferramentas anti-defesa justamente quando mais precisam.
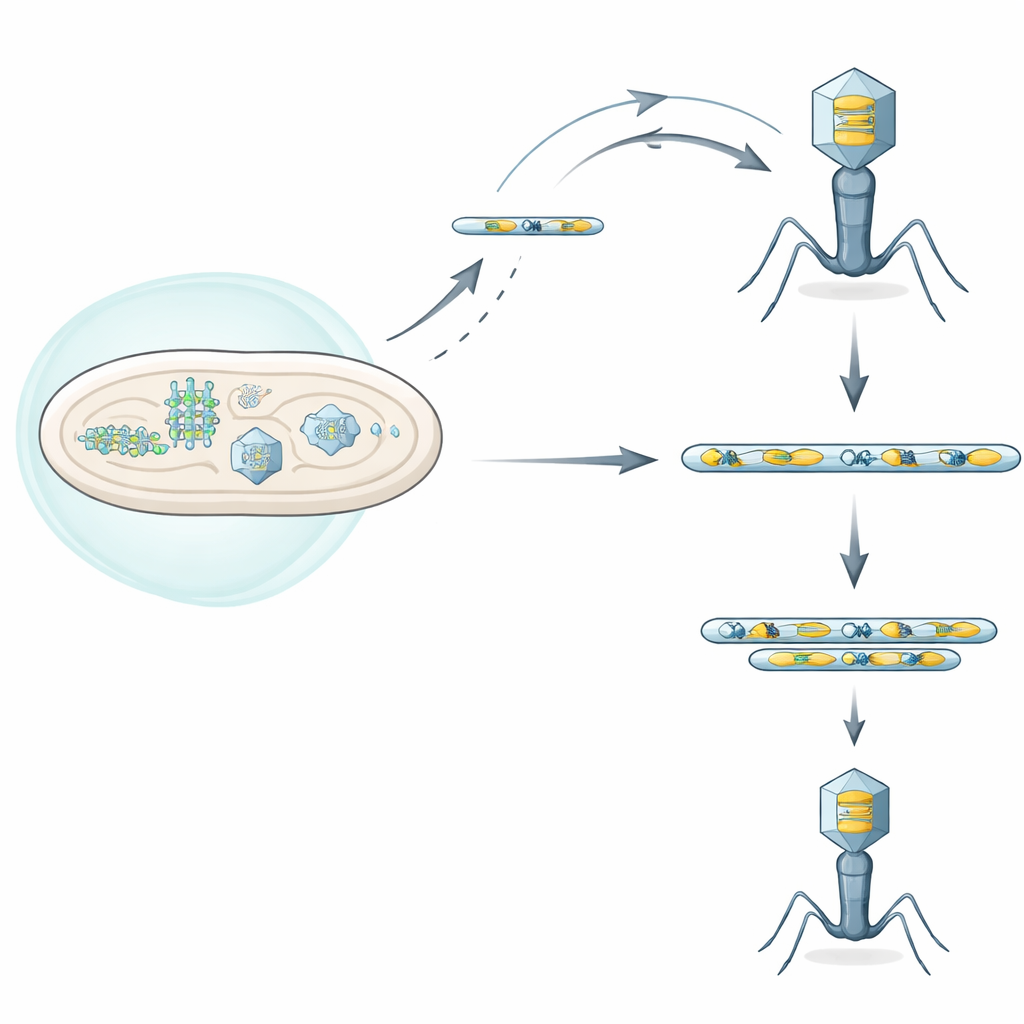
Um duelo entre escudos bacterianos e atacantes virais
Bactérias possuem muitos sistemas de defesa que detectam a infecção viral e a interrompem, às vezes até matando a célula infectada para proteger a população mais ampla. Os autores se concentraram em um desses sistemas, chamado Septu, encontrado em uma estirpe clínica de Escherichia coli. O Septu ataca uma molécula pequena mas vital, um RNA de transferência (tRNA) necessário para traduzir o código genético em proteínas. Ao cortar esse tRNATyr, o Septu priva tanto a célula quanto o fago invasor de um ingrediente chave para a síntese proteica, interrompendo a replicação viral. Ainda assim, alguns fagos conseguem crescer apesar do Septu, sugerindo que evoluíram rotas de escape engenhosas.
Cópias extras de tRNA como reserva viral
Trabalhando com um fago T-even conhecido como T6, os pesquisadores isolaram raros mutantes “escapistas” que podiam se replicar na presença do Septu. Quando sequenciaram esses genomas virais, não encontraram uma única mutação comum a todos os escapistas. Em vez disso, descobriram que cada fago escapista havia amplificado massivamente um segmento curto de DNA contendo duas características: o gene completo de tRNATyr e um gene próximo chamado segB, que codifica uma endonuclease de homing, uma proteína que corta DNA. Esses segmentos amplificados formaram repetições em tandem, como o mesmo parágrafo colado várias vezes em sequência. As cópias extras aumentaram a produção de tRNATyr, fornecendo tRNA suficiente para superar a atividade de corte do Septu e permitindo que a replicação viral reiniciasse.
Uma enzima que corta DNA e impulsiona a expansão do genoma
A equipe então investigou se o SegB era apenas um passageiro nessa região amplificada ou o motor do processo. Ao evoluir fagos sem SegB, ou com uma versão inativa da proteína, mostraram que apenas fagos com um SegB funcional podiam construir essas repetições de DNA sob pressão imune. Testes bioquímicos confirmaram que o SegB corta pontos específicos no genoma do fago, frequentemente perto de genes de tRNA. Depois que o SegB introduz quebras, a maquinaria de recombinação viral pode religar o DNA de maneiras que duplicam acidentalmente segmentos próximos. Quando o Septu está presente, variantes que por acaso ganham mais cópias de tRNATyr possuem uma forte vantagem de sobrevivência e rapidamente dominam a população de fagos. Uma vez que a pressão da defesa é removida, essas cópias extras tendem a colapsar novamente, mostrando que as ampliações são dinâmicas e reversíveis.
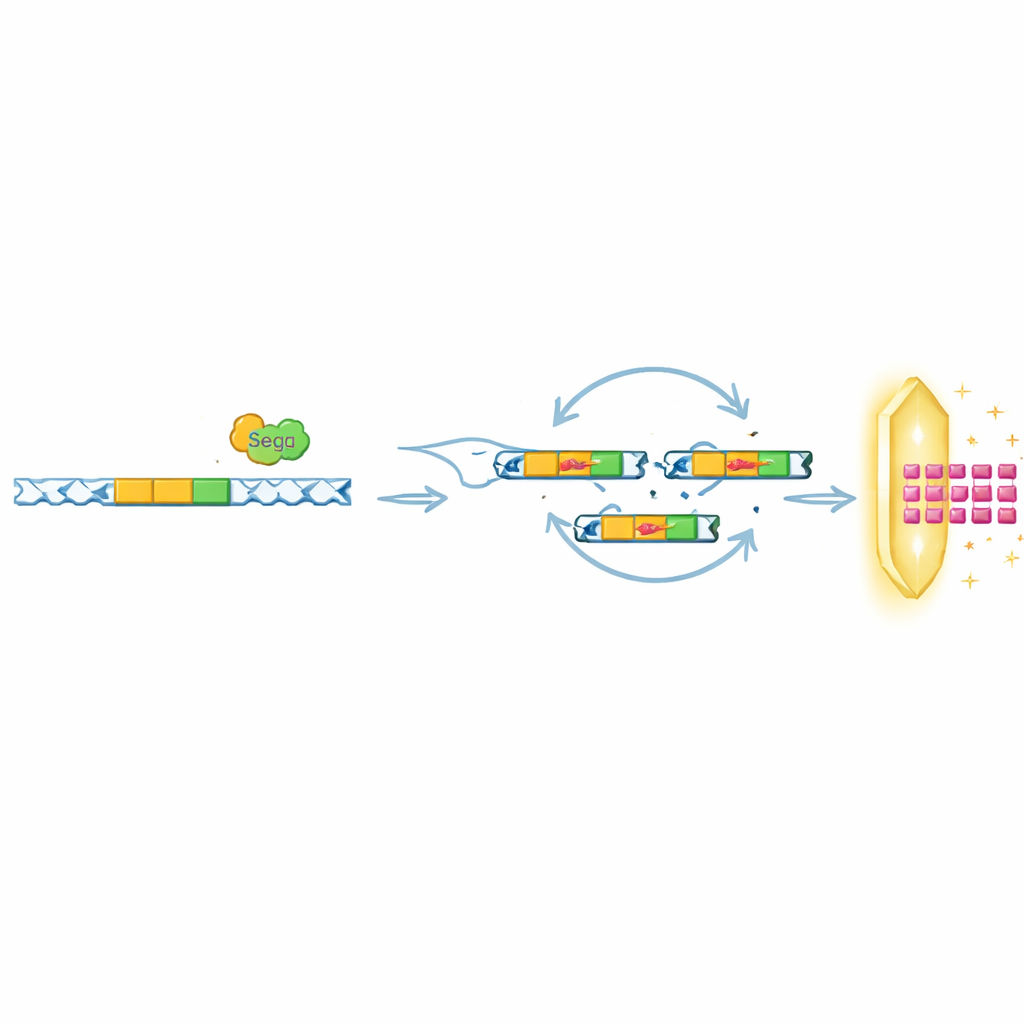
Reaplicando o mesmo truque contra defesas diferentes
De forma intrigante, os pesquisadores descobriram que o papel do SegB vai além de ajudar o T6 a enganar o Septu. Em outros experimentos, eles desafiaram fagos com diferentes sistemas bacterianos, incluindo OLD e ToxIN, que também bloqueiam a infecção, mas por mecanismos muito distintos. Sob pressão do OLD, o SegB dirigiu a amplificação de uma região distante do DNA que codifica uma pequena proteína viral, Gp49.2, que se liga fisicamente e inibe a proteína de defesa OLD. Sob pressão do ToxIN em um fago relacionado, o SegB foi necessário para amplificar outro gene anti-defesa, tifA. Em muitos genomas de fagos em bancos de dados públicos, genes como SegB foram frequentemente encontrados próximos a aglomerados de tRNA, sugerindo que essa estratégia de acoplar corte de DNA com amplificação gênica local ou de longo alcance pode ser comum na natureza.
O que isso significa para a corrida armamentista vírus–bactérias
Para um não especialista, a mensagem chave é que alguns vírus não esperam apenas por mutações lentas de uma única letra em seu DNA para se adaptar. Em vez disso, eles podem rapidamente “esticar” partes do genoma como um acordeão, fazendo múltiplas cópias extras de genes úteis quando estão sob ataque e encolhendo novamente quando essas cópias não são mais necessárias. Neste caso, uma enzima que corta DNA chamada SegB provoca rearranjos genômicos que amplificam genes de tRNA e outros fatores anti-defesa, permitindo que fagos ultrapassem vários sistemas imunes bacterianos diferentes. Isso revela uma estratégia flexível e de resposta rápida que ajuda os vírus a se manterem um passo à frente na batalha com as bactérias.
Citação: Chihara, K., Azam, A.H., Egorov, A.A. et al. Phage homing endonuclease amplifies anti-defense genes to evade bacterial immunity. Nat Commun 17, 3468 (2026). https://doi.org/10.1038/s41467-026-71036-4
Palavras-chave: imunidade de bacteriófagos, defesa antiviral bacteriana, amplificação do genoma, endonuclease de homing, corrida armamentista fago–bactéria