Clear Sky Science · de
Phagen-Homing-Endonuklease vervielfacht Anti-Abwehr-Gene, um bakterieller Immunität zu entgehen
Wie Viren bakterielle Abwehrmechanismen überlisten
Bakterien und die Viren, die sie infizieren — sogenannte Phagen — befinden sich in einem mikroskopischen Wettrüsten. Bakterien entwickeln ständig neue Wege, eindringende Phagen zu erkennen und zu blockieren, während Phagen Gegenstrategien ausbilden, um diese Abwehrmechanismen zu umgehen. Diese Studie enthüllt einen überraschenden viralen Trick: Einige Phagen können bestimmte Abschnitte ihres eigenen DNA-Angebots schnell kopieren und verstärken, die ihnen helfen, verschiedene bakterielle Immunsysteme zu überwinden, und dadurch ihre Anti-Abwehr-Werkzeuge genau dann lauter stellen, wenn sie sie am dringendsten brauchen.
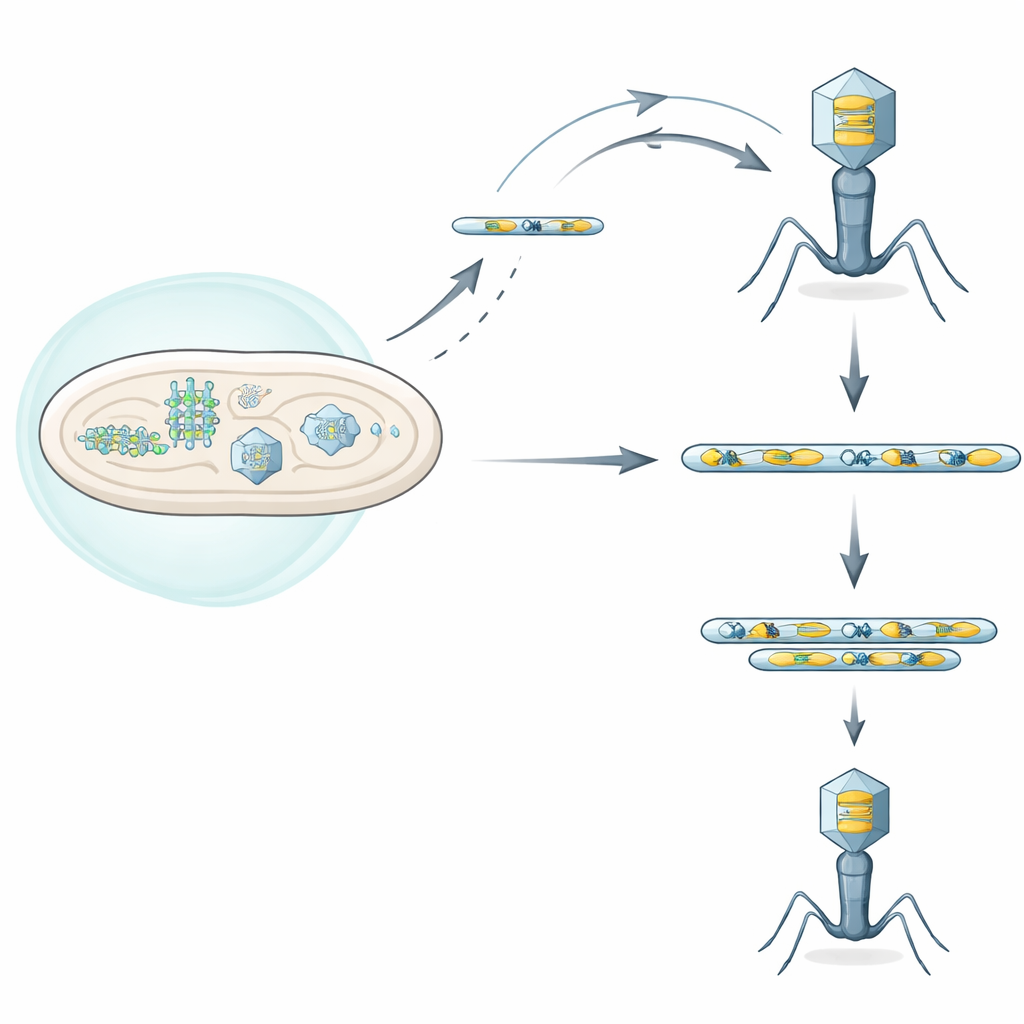
Ein Duell zwischen bakteriellen Schilden und viralen Angreifern
Bakterien besitzen viele Abwehrsysteme, die eine Virusinfektion wahrnehmen und diese stoppen — manchmal töten sie sogar die infizierte Zelle, um die übrige Population zu schützen. Die Autoren konzentrierten sich auf ein solches System namens Septu, das in einem klinischen Stamm von Escherichia coli vorkommt. Septu greift ein kleines, aber essenzielles Molekül an, eine Transfer-RNA (tRNA), die zur Übersetzung des genetischen Codes in Proteine benötigt wird. Durch das Schneiden dieser tRNATyr beraubt Septu sowohl die Zelle als auch den eindringenden Phagen eines Schlüsselbausteins der Proteinsynthese und stoppt so die virale Replikation. Dennoch gelingt es einigen Phagen, trotz Septu zu wachsen, was darauf hindeutet, dass sie clevere Ausweichstrategien entwickelt haben.
Zusätzliche tRNA-Kopien als viraler Reservevorrat
Die Forscher arbeiteten mit einem T-even-Phagen namens T6 und isolierten seltene „Escape“-Mutanten, die sich in Gegenwart von Septu replizieren konnten. Beim Sequenzieren dieser viralen Genome fanden sie keine einzige, gemeinsame Punktmutation in allen Escape-Varianten. Stattdessen entdeckten sie, dass jeder Escape-Phage ein kurzes DNA-Segment massiv vermehrt hatte, das zwei Merkmale enthielt: das vollständige tRNATyr-Gen und ein in der Nähe gelegenes Gen namens segB, das eine Homing-Endonuklease kodiert — ein DNA-schneidendes Protein. Diese amplifizierten Segmente bildeten Tandemwiederholungen, wie wenn derselbe Absatz viele Male hintereinander eingefügt wird. Die zusätzlichen Kopien erhöhten die tRNATyr-Produktion, lieferten genug tRNA, um Septus Schneidaktivität zu kompensieren, und erlaubten so die Wiederaufnahme der viralen Replikation.
Ein DNA-schneidendes Enzym, das Genomexpansion antreibt
Das Team fragte dann, ob SegB nur ein Mitläufer in diesem amplifizierten Bereich oder der Treiber des Prozesses sei. Indem sie Phagen ohne SegB oder mit einer deaktivierten Version des Proteins evolvieren ließen, zeigten sie, dass nur Phagen mit funktionierendem SegB unter immunem Druck diese DNA-Wiederholungen aufbauen konnten. Biochemische Tests bestätigten, dass SegB an spezifischen Stellen im Phagengenom schneidet, oft in der Nähe von tRNA-Genen. Nachdem SegB Brüche eingeführt hat, kann die virale Rekombinationsmaschinerie DNA so wiedervereinigen, dass benachbarte Segmente versehentlich dupliziert werden. In Gegenwart von Septu haben Varianten, die zufällig mehr tRNATyr-Kopien erlangen, einen starken Überlebensvorteil und setzen sich rasch in der Phagenpopulation durch. Sobald der Abwehrdruck wegfällt, neigen diese zusätzlichen Kopien dazu, wieder zu kollabieren — ein Hinweis darauf, dass die Amplifikationen dynamisch und reversibel sind.
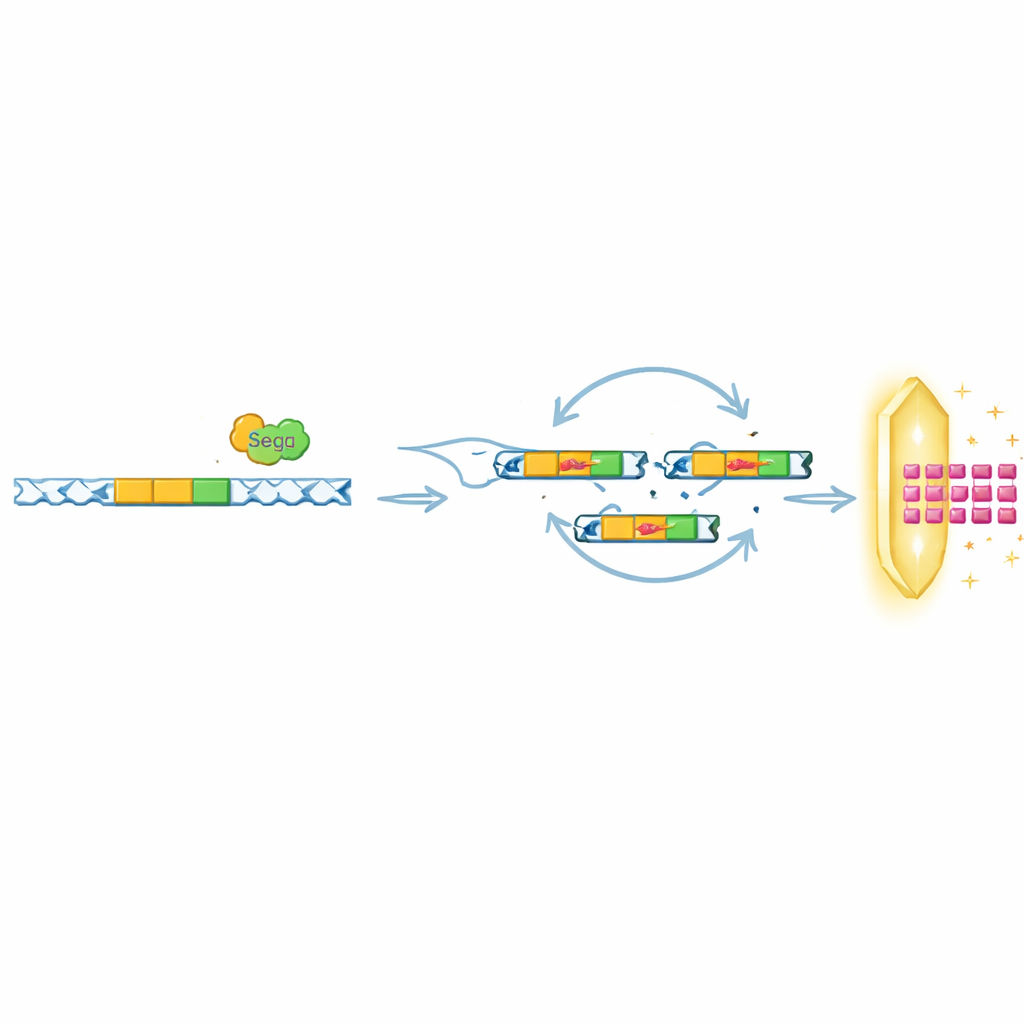
Den gleichen Trick gegen verschiedene Abwehrmechanismen wiederverwenden
Interessanterweise reicht SegBs Rolle über die Hilfe von T6 gegen Septu hinaus. In weiteren Experimenten setzten die Forscher Phagen unterschiedlichen bakteriellen Systemen aus, darunter OLD und ToxIN, die ebenfalls Infektionen blockieren, aber auf sehr unterschiedliche Weisen. Unter OLD-Druck förderte SegB die Amplifikation einer entfernten DNA-Region, die ein kleines virales Protein, Gp49.2, kodiert, das physikalisch an das OLD-Abwehrprotein bindet und es hemmt. Unter ToxIN-Druck in einem verwandten Phagen war SegB notwendig, um ein weiteres Anti-Abwehr-Gen, tifA, zu amplifizieren. In vielen Phagengenomen in öffentlichen Datenbanken fanden sich Gene wie SegB häufig in der Nähe von tRNA-Clustern, was darauf hindeutet, dass diese Strategie, DNA-Schnitt mit lokaler oder fernreichender Genamplifikation zu koppeln, in der Natur weit verbreitet sein könnte.
Was das für das Virus–Bakterien-Wettrüsten bedeutet
Für Nicht-Spezialisten ist die Kernbotschaft, dass einige Viren nicht einfach auf langsame Einzelbuchstabenmutationen in ihrer DNA warten, um sich anzupassen. Stattdessen können sie Teile ihres Genoms schnell „ausdehnen“ wie ein Akkordeon und mehrere zusätzliche Kopien hilfreicher Gene erzeugen, wenn sie angegriffen werden, und sich wieder zusammenziehen, wenn diese Kopien nicht mehr benötigt werden. In diesem Fall löst eine DNA-schneidende Endonuklease namens SegB Genomumordnungen aus, die tRNA-Gene und andere Anti-Abwehr-Faktoren amplifizieren und es Phagen ermöglichen, mehrere verschiedene bakterielle Immunsysteme zu überwältigen. Das offenbart eine flexible, schnell reagierende Strategie, die Viren hilft, im Kampf mit Bakterien einen Schritt voraus zu bleiben.
Zitation: Chihara, K., Azam, A.H., Egorov, A.A. et al. Phage homing endonuclease amplifies anti-defense genes to evade bacterial immunity. Nat Commun 17, 3468 (2026). https://doi.org/10.1038/s41467-026-71036-4
Schlüsselwörter: Bakteriophagen-Immunität, bakterielle antivirale Abwehr, Genomverstärkung, Homing-Endonuklease, Phagen–Bakterien Wettrüsten