Clear Sky Science · fr
L’endonucléase homing des phages amplifie des gènes anti‑défense pour échapper à l’immunité bactérienne
Comment les virus déjouent les défenses bactériennes
Les bactéries et les virus qui les infectent, appelés phages, sont engagés dans une course aux armements microscopique. Les bactéries développent de nouveaux moyens de détecter et de bloquer les phages envahisseurs, tandis que les phages mettent au point des contre‑mouvements pour contourner ces défenses. Cette étude révèle un stratagème viral surprenant : certains phages peuvent copier et amplifier très rapidement des fragments spécifiques de leur propre ADN qui leur permettent de battre différents systèmes immunitaires bactériens, augmentant ainsi temporairement l’efficacité de leurs outils anti‑défense au moment où ils en ont le plus besoin.
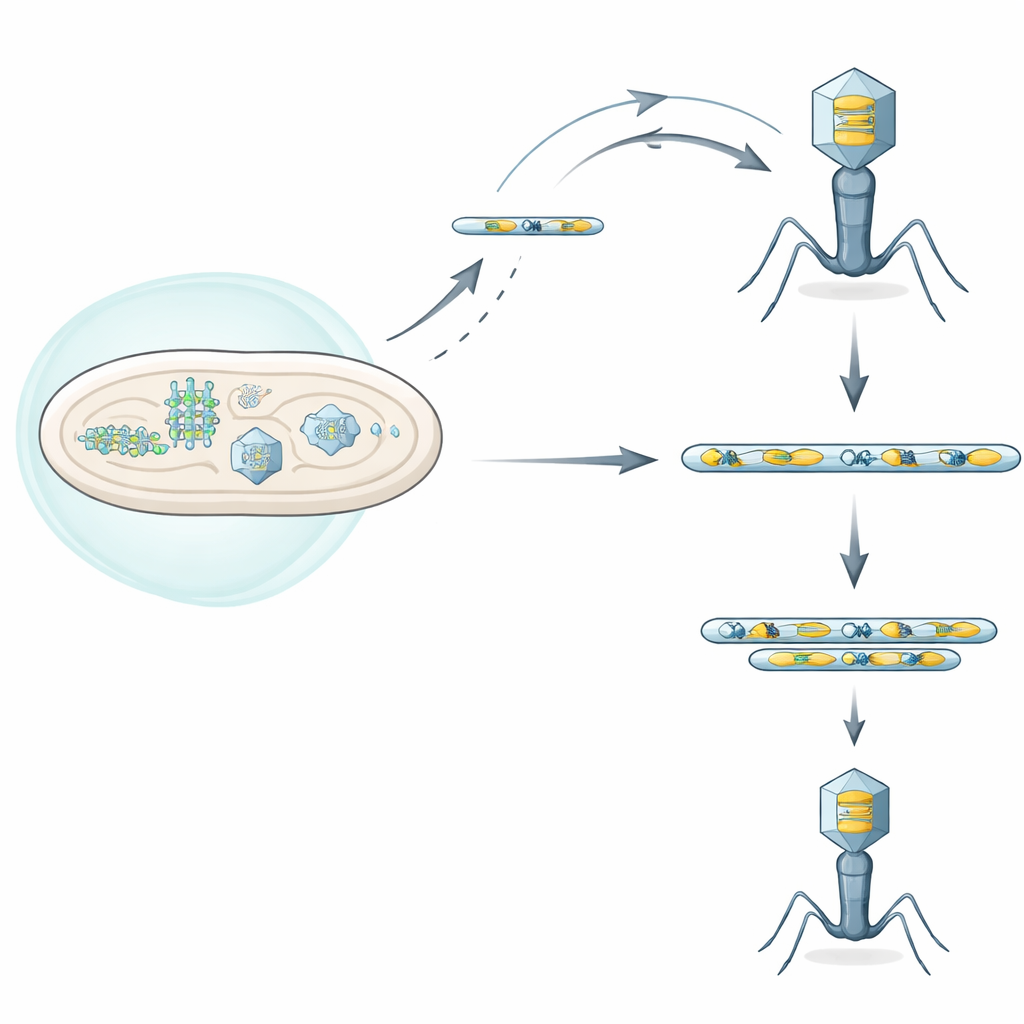
Un duel entre boucliers bactériens et attaquants viraux
Les bactéries possèdent de nombreux systèmes de défense qui détectent l’infection virale et la neutralisent, allant parfois jusqu’à tuer la cellule infectée pour protéger la population environnante. Les auteurs se sont concentrés sur l’un de ces systèmes, appelé Septu, retrouvé dans une souche clinique d’Escherichia coli. Septu attaque une petite molécule vitale, un ARN de transfert (ARNt) nécessaire pour traduire le code génétique en protéines. En coupant cet ARNtTyr, Septu prive à la fois la cellule et le phage envahisseur d’un ingrédient clé pour la synthèse protéique, arrêtant ainsi la réplication virale. Pourtant, certains phages parviennent malgré tout à se développer en présence de Septu, ce qui suggère qu’ils ont évolué des voies d’échappement ingénieuses.
Copies supplémentaires d’ARNt comme réserve virale
Travaillant avec un phage de type T appelé T6, les chercheurs ont isolé de rares mutants « échappés » capables de se répliquer en présence de Septu. Lorsqu’ils ont séquencé ces génomes viraux, ils n’ont pas trouvé une mutation unique commune à tous les échappés. Au lieu de cela, ils ont découvert que chaque phage échappé avait amplifié massivement un court segment d’ADN contenant deux éléments : le gène complet de l’ARNtTyr et un gène voisin nommé segB, qui code pour une endonucléase homing, une protéine qui coupe l’ADN. Ces segments amplifiés formaient des répétitions en tandem, comme un même paragraphe collé plusieurs fois de suite. Les copies supplémentaires augmentaient la production d’ARNtTyr, fournissant suffisamment d’ARNt pour compenser l’activité de coupe de Septu et permettant à la réplication virale de reprendre.
Une enzyme qui coupe l’ADN et entraîne l’expansion du génome
L’équipe s’est alors demandé si SegB n’était qu’un passager dans cette région amplifiée ou le moteur du processus. En faisant évoluer des phages dépourvus de SegB, ou portant une version inactivée de la protéine, ils ont montré que seuls les phages dotés d’un SegB fonctionnel pouvaient assembler ces répétitions d’ADN sous la pression immunitaire. Des tests biochimiques ont confirmé que SegB coupe à des endroits spécifiques du génome du phage, souvent à proximité des gènes d’ARNt. Après que SegB introduit des cassures, la machinerie de recombinaison virale peut recoller l’ADN de manières qui dupliquent accidentellement les segments voisins. En présence de Septu, les variantes qui acquièrent par hasard davantage de copies d’ARNtTyr disposent d’un fort avantage sélectif et envahissent rapidement la population de phages. Une fois la pression défensive levée, ces copies supplémentaires ont tendance à s’effondrer, montrant que les amplifications sont dynamiques et réversibles.
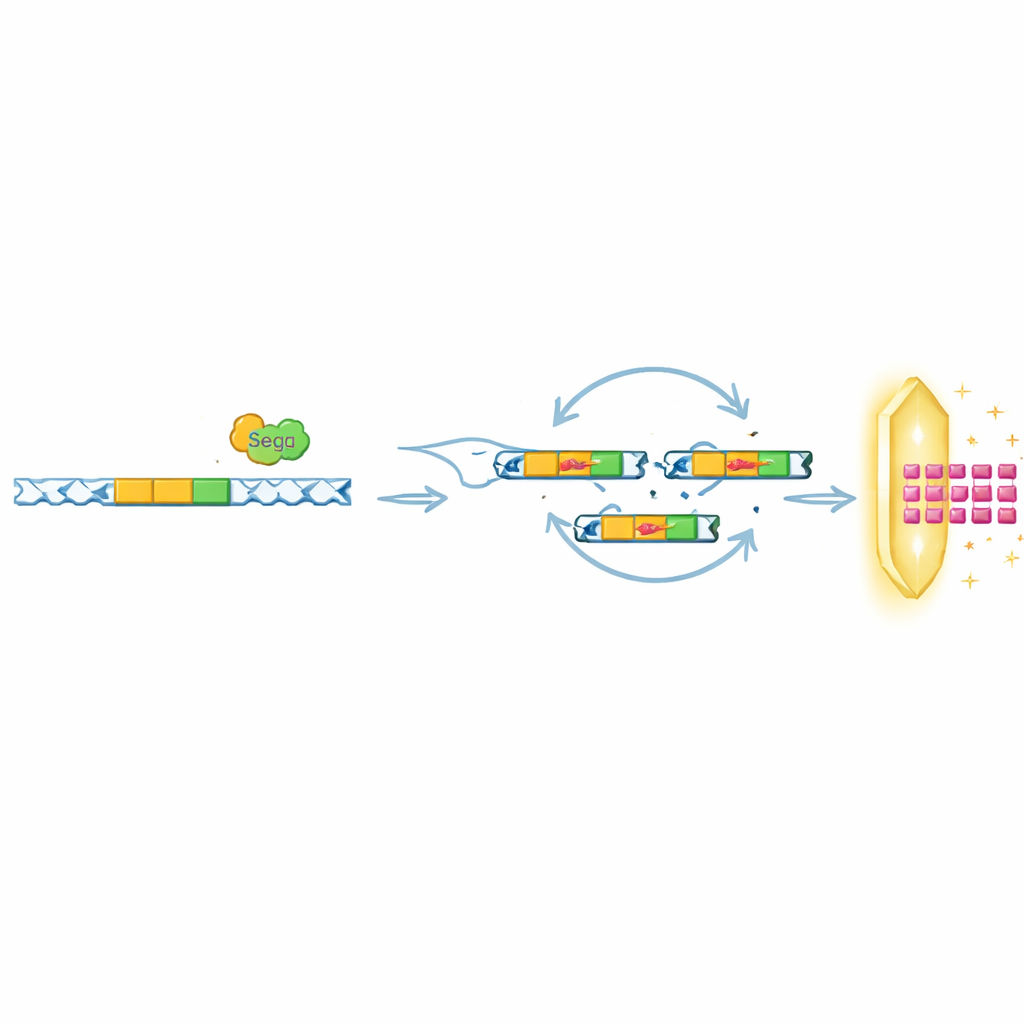
Réutiliser la même astuce contre diverses défenses
De façon intrigante, les chercheurs ont constaté que le rôle de SegB va au‑delà de l’aide apportée à T6 pour déjouer Septu. Dans d’autres expériences, ils ont soumis des phages à différents systèmes bactériens, dont OLD et ToxIN, qui bloquent également l’infection mais par des mécanismes très différents. Sous la pression d’OLD, SegB a entraîné l’amplification d’une région d’ADN distante qui code une petite protéine virale, Gp49.2, laquelle se lie physiquement et inhibe la protéine de défense OLD. Sous la pression de ToxIN, dans un phage apparenté, SegB était nécessaire pour amplifier un autre gène anti‑défense, tifA. Dans de nombreux génomes de phages disponibles dans les bases publiques, des gènes semblables à SegB se trouvent fréquemment à proximité de clusters d’ARNt, ce qui suggère que cette stratégie d’associer la coupure de l’ADN à l’amplification locale ou à distance de gènes pourrait être répandue dans la nature.
Ce que cela signifie pour la course aux armements virus–bactérie
Pour un non‑spécialiste, le message clé est que certains virus n’attendent pas simplement de lentes mutations ponctuelles dans leur ADN pour s’adapter. Ils peuvent au contraire « étirer » rapidement des parties de leur génome comme un accordéon, en produisant plusieurs copies supplémentaires de gènes utiles sous l’attaque puis en les réduisant lorsqu’elles ne sont plus nécessaires. Ici, une enzyme coupant l’ADN appelée SegB déclenche des réarrangements du génome qui amplifient des gènes d’ARNt et d’autres facteurs anti‑défense, permettant aux phages de surmonter plusieurs systèmes immunitaires bactériens. Cela révèle une stratégie flexible et à réponse rapide qui aide les virus à garder une longueur d’avance dans leur bataille contre les bactéries.
Citation: Chihara, K., Azam, A.H., Egorov, A.A. et al. Phage homing endonuclease amplifies anti-defense genes to evade bacterial immunity. Nat Commun 17, 3468 (2026). https://doi.org/10.1038/s41467-026-71036-4
Mots-clés: immunité des bactériophages, défense antivirale bactérienne, amplification du génome, endonucléase homing, course aux armements phage–bactérie