Clear Sky Science · zh
一种类桥接的脂质转运蛋白对应对疟原虫侵入阶段的形成至关重要
疟原虫如何构建其侵入装备
疟原虫通过不断侵入新的红细胞来生存。为此,每个在细胞内生长的寄生体必须构建数十个准备破裂出来并攻击新细胞的微小后代。这一构建工程需要大量新的膜,主要由被称为脂质的脂肪分子构成。这里总结的研究揭示了一种关键的“桥接”蛋白,它在寄生虫内部运输脂质,使其能够组装侵入所需的机械结构。理解这条隐蔽的补给线可能为阻断疟疾打开新的途径。
受感染细胞内的隐秘结构
一旦进入红细胞,疟原虫便迅速繁殖。在其生命周期的晚期,它会变成一个充满多个细胞核的大细胞。在每个未来子细胞周围,寄生虫构建一个支持性的壳,称为内膜复合体(inner membrane complex,IMC)。这一壳位于外表面之下,对于塑造子代并为其进入下一个红细胞提供动力均至关重要。从头构建IMC需要来自寄生虫内部工厂——内质网(ER)——稳定的大量脂质供应。研究人员提出的重大问题是,这些脂质如何如此迅速且高效地从内质网移动到正在生长的IMC。
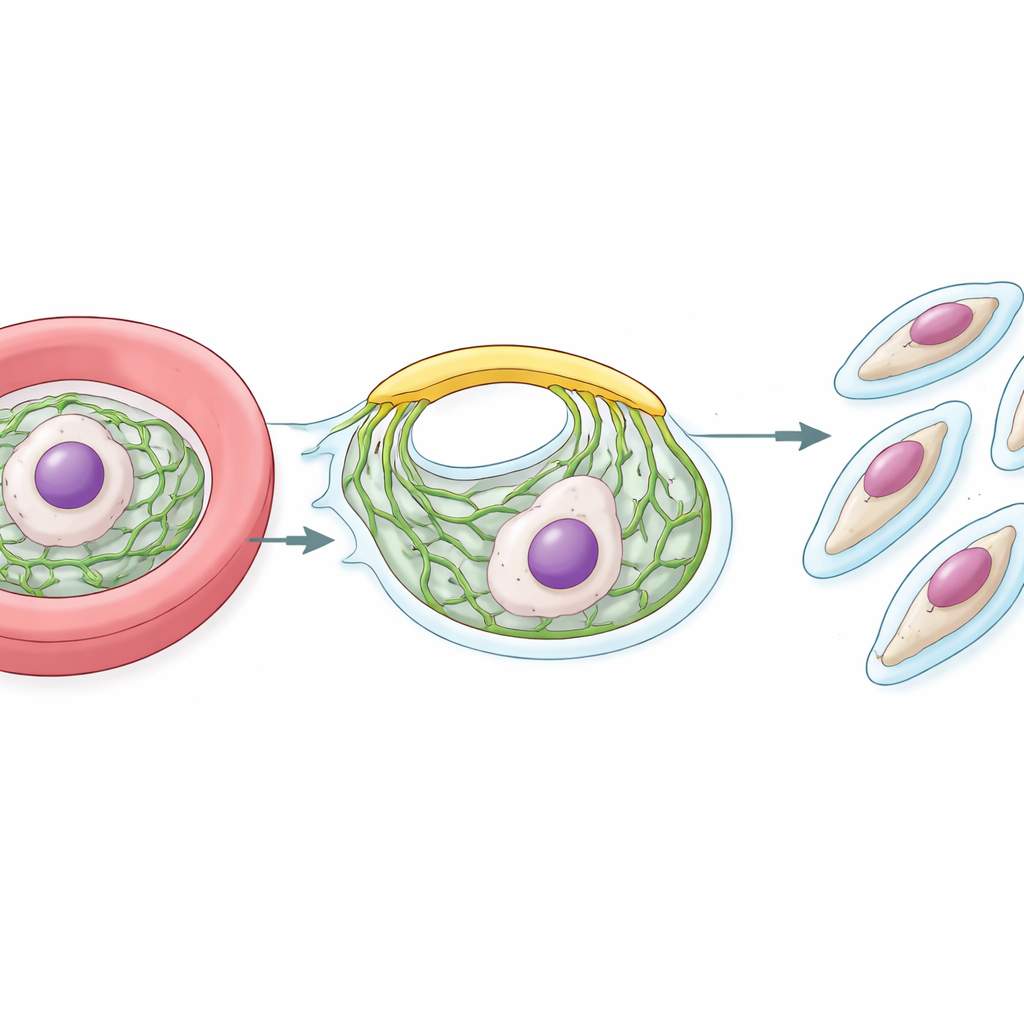
发现脂质桥
在许多生物体中,脂质可以在紧密接触的相邻膜之间直接移动,借助特殊的载体蛋白。研究组从已知的内质网锚定蛋白VAP入手,VAP会抓取含有短“FFAT”基序的伙伴。研究人员使用一种近邻标记方法,列出了位于疟原虫内质网表面靠近VAP的蛋白。在众多候选者中,他们鉴定出若干处理脂质的蛋白,并将关注点集中在一个巨大且类似于VPS13的蛋白上——VPS13家族在酵母和人类细胞中被描述为“类桥接”脂质转运器。他们将该寄生虫蛋白命名为PfVPS13L1。
桥如何连接两层膜
基于计算的结构预测显示,PfVPS13L1形成一条长杆状分子,内部有一条槽可以同时容纳多种脂质分子。杆的一端携带一个能与VAP结合的FFAT基序,将该端固定到脂质来源的内质网上。另一端包含能附着IMC的适配区域。研究人员证明,这一端与他们命名为PfAegerolysin的IMC蛋白发生相互作用,表明PfVPS13L1在物理上搭起了内质网与正在生长的IMC之间的桥梁。高分辨率显微镜证实,PfVPS13L1恰好聚集在围绕未来子细胞形成新IMC膜的位置。
当桥断裂会发生什么
为测试该桥的功能,科学家们使用了一种快速的“错误定位”技巧:通过化学方法将PfVPS13L1从其正常位置牵引到寄生虫的外表面,有效使其失能。当在IMC需要生长之前短时执行该操作,寄生虫便无法产生正常的后代。IMC开始成形但随后停滞;它没有完全包裹每个细胞核,而是保持在小而不完整的状态。结果,许多被壳包裹的小体缺乏细胞核,而额外的遗传物质和细胞质被留在一个大的残余团块中。其他结构,例如特化的分泌细胞器,仍能形成,这强调了主要失败点在于为IMC提供膜物质。
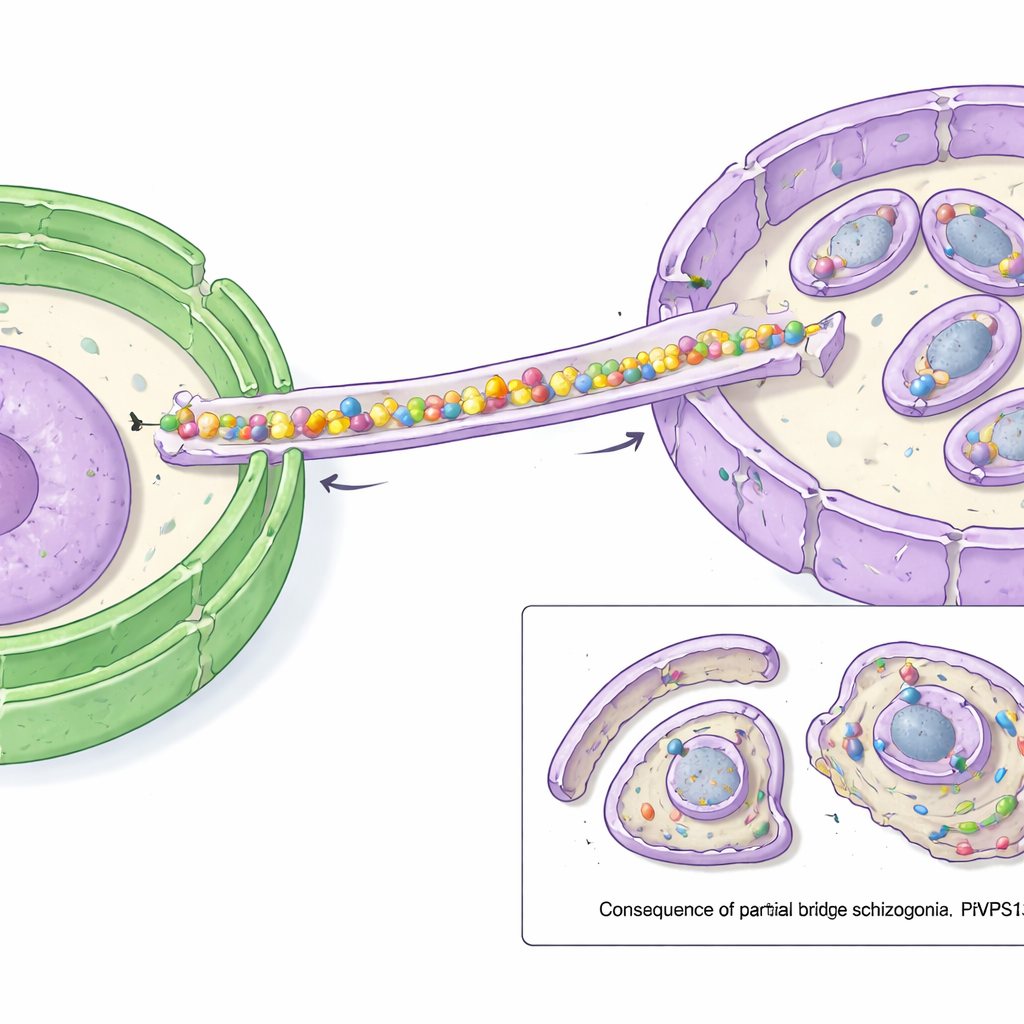
这对抗击疟疾为何重要
该研究表明,PfVPS13L1是一个关键的脂质桥,为IMC的快速扩展提供燃料,使疟原虫能够生成完全形成、具侵袭性的子代。没有来自内质网的大宗脂质转运通道,寄生虫会组装出无法继续感染周期的缺陷后代。由于类似的类桥接蛋白在多种细胞类型中发挥作用,PfVPS13L1代表了对这一保守机制的寄生虫特异性改造。针对这一桥或将其固定到IMC的合作伙伴,可能提供一种新的抗疟策略,旨在悄然切断寄生虫为其侵入机械提供所需膜的供应。
引用: Guillén-Samander, A., Perepelkina, N., Horáčková, V. et al. A bridge-like lipid transfer protein is critical for generation of invasive stages in malaria parasites. Nat Commun 17, 3030 (2026). https://doi.org/10.1038/s41467-026-70887-1
关键词: 疟疾, 脂质转运, 膜生物发生, 恶性疟原虫, 内膜复合体