Clear Sky Science · ru
Белковый переносчик липидов вида «мост» критичен для образования инвазивных стадий у паразитов малярии
Как паразиты малярии строят свой механизм инвазии
Паразиты, вызывающие малярию, выживают, постоянно инфицируя новые эритроциты. Для этого каждый паразит, растущий внутри клетки, должен собрать десятки мелких потомков, готовых вырваться наружу и атаковать новые клетки. Этот строительный проект требует огромного количества новой мембраны, которая в основном состоит из жироподобных молекул — липидов. В приведённом исследовании раскрыт ключевой «мостовой» белок, переносящий липиды внутри паразита и позволяющий ему собирать машины для инвазии. Понимание этой скрытой «поставки» может открыть новые пути для блокировки малярии.
Скрытая архитектура внутри инфицированной клетки
Оказавшись внутри эритроцита, паразит малярии быстро размножается. На поздних стадиях цикла он превращается в большую клетку, заполненную множеством ядер. Вокруг каждой будущей дочерней клетки паразит строит опорную оболочку, называемую внутренним мембранным комплексом, или IMC. Эта оболочка располагается прямо под внешней поверхностью и важна как для формирования потомства, так и для обеспечения их проникновения в следующий эритроцит. Построение IMC с нуля требует постоянного потока липидов от внутренней фабрики паразита — эндоплазматического ретикулума (ER). Главный вопрос, который поставили исследователи, — как эти липиды так быстро и эффективно перемещаются от ER к растущему IMC.
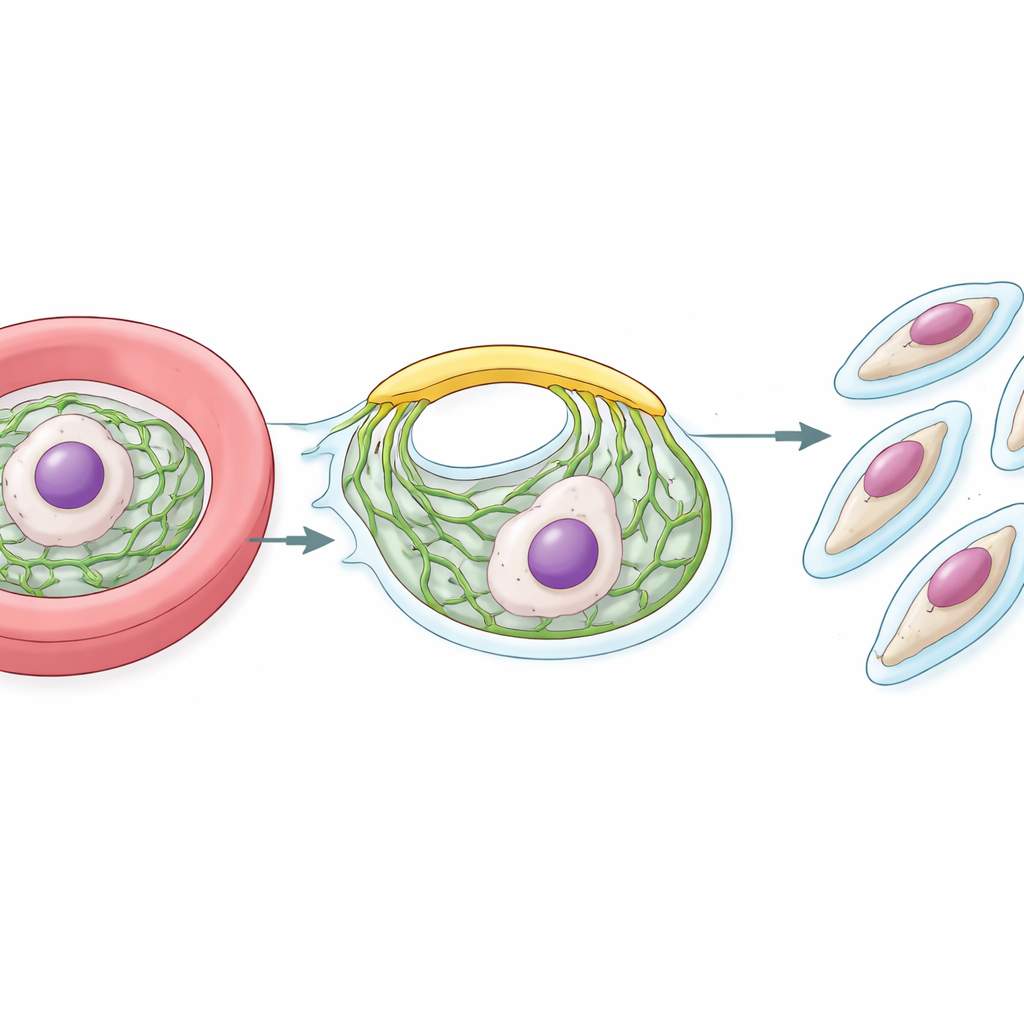
Поиск липидного моста
У многих организмов липиды могут перемещаться напрямую между соседними мембранами на участках тесного контакта при участии специальных переносчиков. Команда начала с известного анкерного белка ER, называемого VAP, который связывает партнёров, содержащих короткие мотивы «FFAT». Используя метод мечение близости, они каталогизировали белки, находящиеся рядом с VAP на поверхности ER у паразитов малярии. Среди многих кандидатов они обнаружили несколько белков, работающих с липидами, и сосредоточились на гигантском белке, похожем на VPS13 — семейство «мостовых» переносчиков липидов, известных по дрожжам и клеткам человека. Этот белок паразита назвали PfVPS13L1.
Как мост соединяет две мембраны
Компьютерные структурные предсказания показали, что PfVPS13L1 образует длинную стержнеподобную молекулу с внутренней канавкой, способной вмещать сразу множество молекул липидов. Один конец стержня несёт мотив FFAT, который связывается с VAP на ER, фиксируя этот конец у источника липидов. Другой конец содержит адаптерные области, прикрепляющиеся к IMC. Исследователи показали, что этот «хвост» взаимодействует с белком IMC, который они назвали PfAegerolysin, что указывает на то, что PfVPS13L1 физически образует мост между ER и растущим IMC. Микроскопия высокого разрешения подтвердила, что PfVPS13L1 собирается точно там, где формируется новая мембрана IMC вокруг будущих дочерних клеток.
Что происходит, когда мост разрушается
Чтобы проверить функцию моста, учёные использовали трюк быстрого «неправильного локализования»: они химически переместили PfVPS13L1 с его обычного места на наружную поверхность паразита, фактически инактивировав его. Когда это выполняли непосредственно перед стадией, на которой должен расти IMC, паразиты уже не могли производить нормальное потомство. IMC начинал формироваться, но затем останавливался; вместо того чтобы полностью обёртывать каждое ядро, он оставался маленьким и неполным. В результате многие мелкие оболочечные образования лишились ядер, тогда как дополнительный генетический материал и цитоплазма остались в большом остаточном комке. Другие структуры, такие как специализированные секреторные органеллы, при этом всё ещё формировались, что подчёркивает: основная ошибка заключалась в поставке мембраны для IMC.
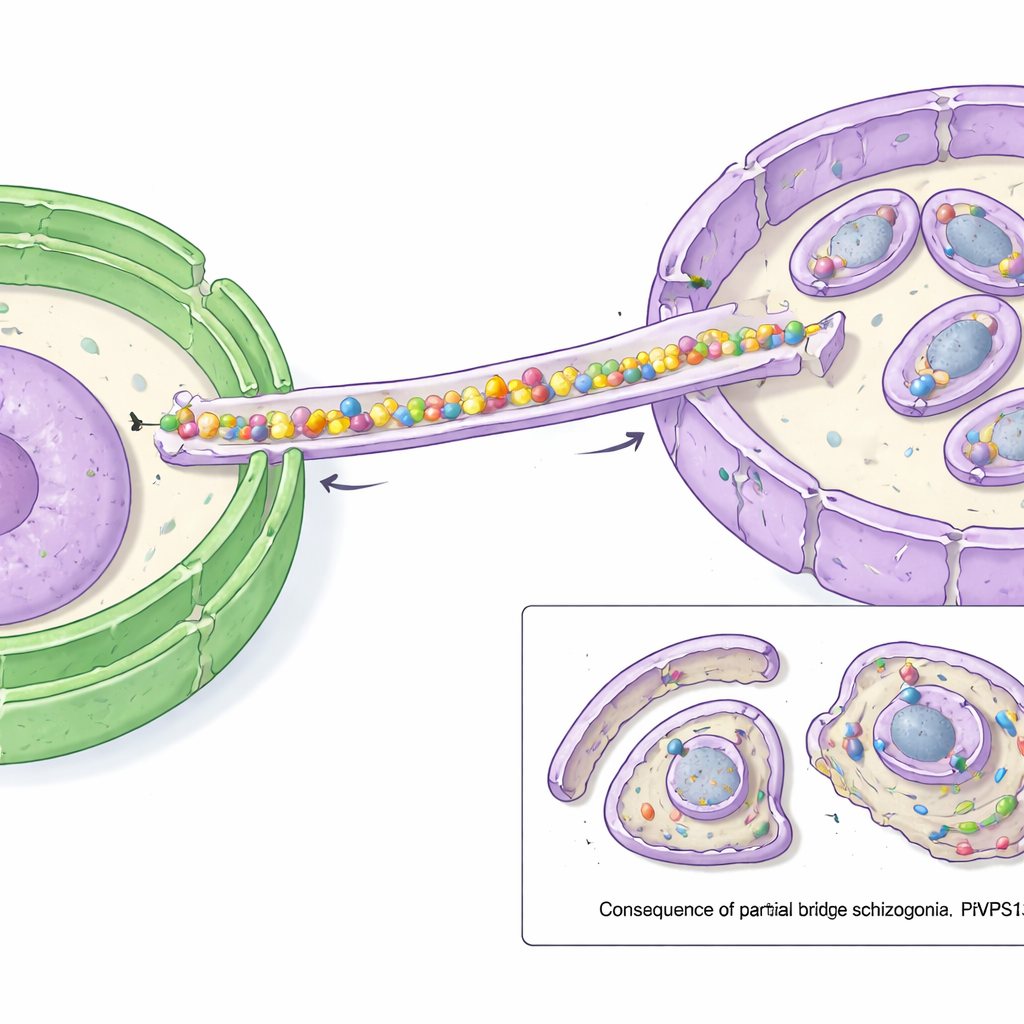
Почему это важно для борьбы с малярией
Исследование показывает, что PfVPS13L1 — ключевой липидный мост, обеспечивающий быстрое расширение IMC и позволяющий паразитам малярии создать полностью сформированное, инвазивное потомство. Без этого оптового пути переноса липидов из ER паразиты собирают дефектных потомков, неспособных продолжить цикл инфекции. Поскольку подобные «мостовые» белки действуют во многих типах клеток, PfVPS13L1 представляет собой специфическую для паразита адаптацию консервативного механизма. Нацеленность на этот мост или на его партнёров, закрепляющих его на IMC, может предложить новую стратегию противомалярийных препаратов, направленную на «тихое» лишение машин инвазии паразита необходимых мембран.
Цитирование: Guillén-Samander, A., Perepelkina, N., Horáčková, V. et al. A bridge-like lipid transfer protein is critical for generation of invasive stages in malaria parasites. Nat Commun 17, 3030 (2026). https://doi.org/10.1038/s41467-026-70887-1
Ключевые слова: малярия, перенос липидов, биогенез мембран, Plasmodium falciparum, внутренний мембранный комплекс