Clear Sky Science · fr
Une protéine de transfert de lipides en forme de pont est essentielle à la génération des stades invasifs chez les parasites du paludisme
Comment les parasites du paludisme construisent leur équipement d’invasion
Les parasites du paludisme survivent en envahissant sans cesse de nouveaux globules rouges. Pour cela, chaque parasite se développant à l’intérieur d’une cellule doit fabriquer des dizaines de petits descendants prêts à éclore et à attaquer d’autres cellules. Ce chantier exige d’importantes quantités de nouvelle membrane, constituée en grande partie de molécules grasses appelées lipides. L’étude résumée ici révèle une protéine « pont » clé qui transporte des lipides à l’intérieur du parasite, lui permettant d’assembler la machinerie d’invasion. Comprendre cette chaîne d’approvisionnement cachée pourrait ouvrir de nouvelles voies pour bloquer le paludisme.
L’architecture cachée à l’intérieur d’une cellule infectée
Une fois à l’intérieur d’un globule rouge, le parasite se multiplie rapidement. Tard dans son cycle, il devient une grosse cellule remplie de nombreux noyaux. Autour de chaque futur parasite fille, le parasite construit une coque de soutien appelée complexe membranaire interne, ou IMC. Cette couche se situe juste sous la surface externe et est essentielle à la fois pour donner forme aux descendants et pour les aider à pénétrer dans le prochain globule rouge. Construire l’IMC à partir de rien nécessite un flux constant de lipides provenant de l’usine interne du parasite, le réticulum endoplasmique (RE). La grande question que se sont posée les chercheurs était de savoir comment ces lipides se déplacent si rapidement et efficacement du RE vers l’IMC en croissance.
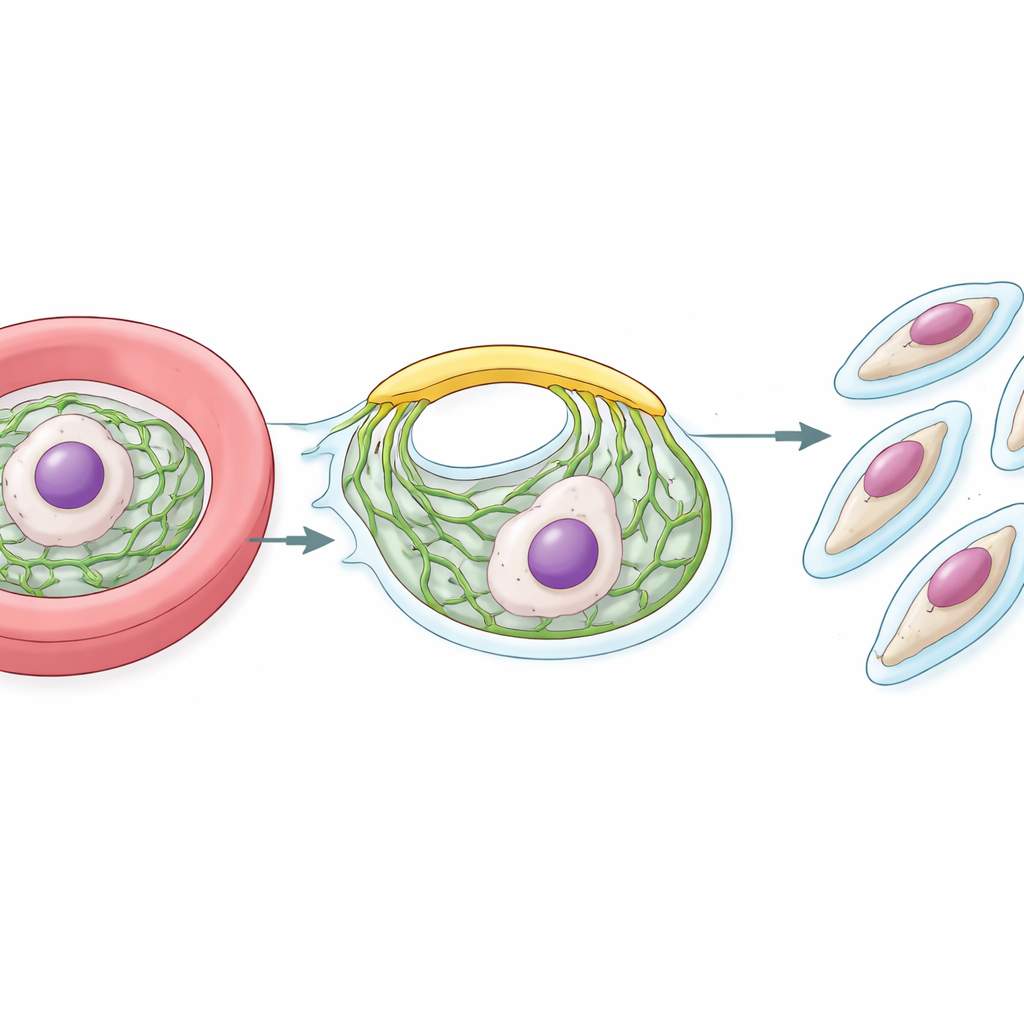
À la recherche du pont lipidique
Chez de nombreux organismes, les lipides peuvent se déplacer directement entre membranes voisines aux sites de contact rapproché, aidés par des protéines transporteurs spécialisées. L’équipe est partie d’une protéine ancrée au RE connue sous le nom de VAP, qui recrute des partenaires contenant de courts motifs « FFAT ». En utilisant une méthode de marquage par proximité, ils ont répertorié les protéines situées près de VAP à la surface du RE chez les parasites du paludisme. Parmi de nombreux candidats, ils ont identifié plusieurs protéines manipulant les lipides et se sont concentrés sur une gigantesque protéine ressemblant à VPS13, une famille de transporteurs lipidiques « en forme de pont » connue chez la levure et les cellules humaines. Ils ont nommé cette protéine parasitaire PfVPS13L1.
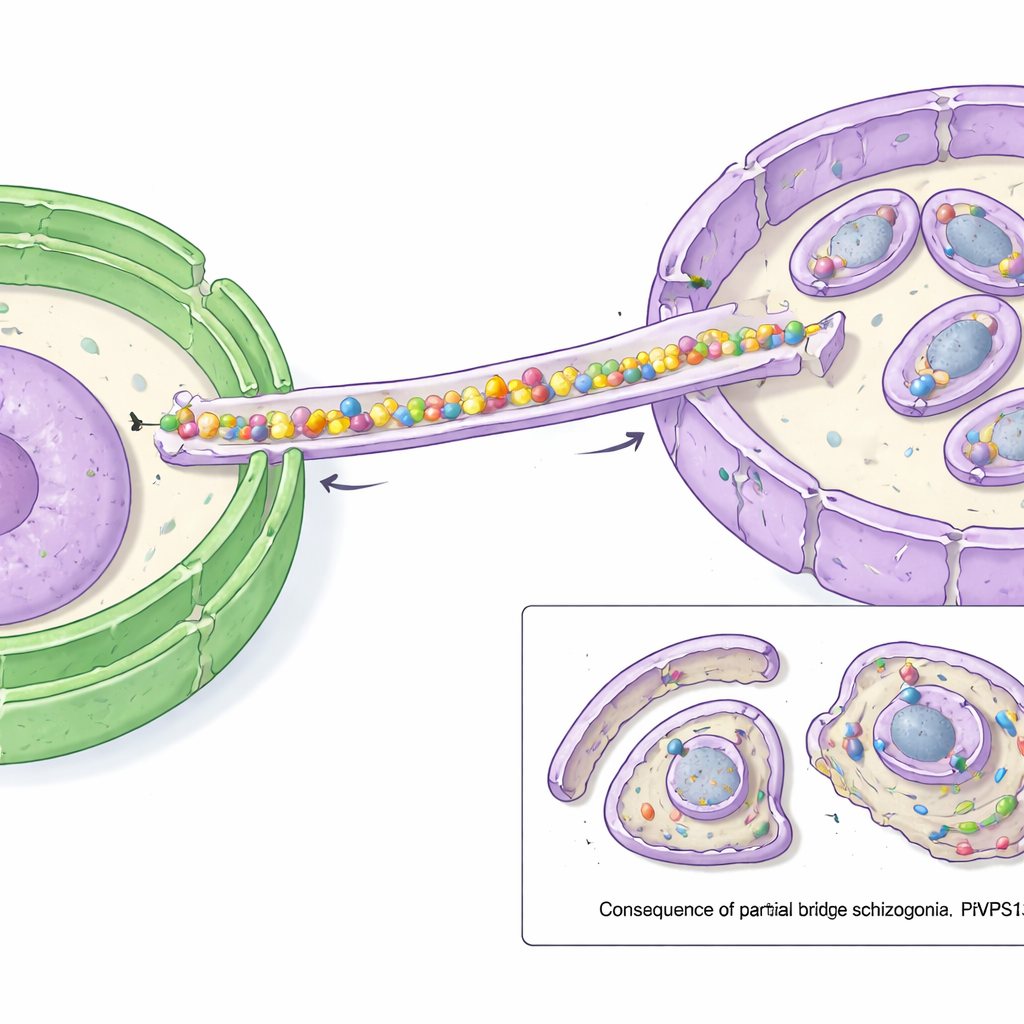
Comment le pont relie deux membranes
Des prédictions structurelles basées sur ordinateur ont révélé que PfVPS13L1 forme une longue molécule en forme de tige avec une rainure interne capable d’accueillir de nombreuses molécules lipidiques simultanément. Une extrémité de la tige porte un motif FFAT qui se lie à VAP au niveau du RE, fixant ainsi cette extrémité à la source lipidique. L’autre extrémité contient des régions adaptatrices qui s’attachent à l’IMC. Les chercheurs ont montré que cette pointe interagit avec une protéine de l’IMC qu’ils ont qualifiée de PfAegerolysin, indiquant que PfVPS13L1 fait physiquement le lien entre le RE et l’IMC en croissance. La microscopie à haute résolution a confirmé que PfVPS13L1 se concentre précisément là où la nouvelle membrane de l’IMC se forme autour des futurs descendants.
Que se passe-t-il lorsque le pont se rompt
Pour tester la fonction du pont, les scientifiques ont utilisé un tour de « délocalisation » rapide : ils ont chimiquement attiré PfVPS13L1 hors de sa position normale vers la surface externe du parasite, le rendant ainsi inactif. Lorsqu’ils ont effectué cette manipulation juste avant l’étape où l’IMC doit croître, les parasites n’ont plus pu produire de descendants normaux. L’IMC a commencé à se former mais s’est ensuite enlisé ; au lieu d’envelopper complètement chaque noyau, il est resté petit et incomplet. En conséquence, de nombreux petits corps entourés d’une coque étaient dépourvus de noyau, tandis que du matériel génétique et du cytoplasme supplémentaires restaient à l’arrière dans un gros reliquat. D’autres structures, comme des organites sécrétoires spécialisés, se formaient encore, ce qui souligne que l’échec principal tenait à l’approvisionnement en membrane pour l’IMC.
Pourquoi cela importe pour la lutte contre le paludisme
L’étude montre que PfVPS13L1 est un pont lipidique crucial qui alimente l’expansion rapide de l’IMC, permettant aux parasites du paludisme de générer des descendants entièrement formés et invasifs. Sans cette voie de transfert massif de lipides depuis le RE, les parasites assemblent des descendants défectueux incapables de poursuivre le cycle d’infection. Parce que des protéines en forme de pont similaires opèrent dans de nombreux types cellulaires, PfVPS13L1 représente une adaptation spécifique au parasite d’un mécanisme conservé. Cibler ce pont, ou ses partenaires qui l’ancrent à l’IMC, pourrait offrir une nouvelle stratégie pour des médicaments antipaludiques visant à priver silencieusement la machinerie d’invasion du parasite des membranes dont elle a besoin.
Citation: Guillén-Samander, A., Perepelkina, N., Horáčková, V. et al. A bridge-like lipid transfer protein is critical for generation of invasive stages in malaria parasites. Nat Commun 17, 3030 (2026). https://doi.org/10.1038/s41467-026-70887-1
Mots-clés: paludisme, transfert de lipides, biogenèse membranaire, Plasmodium falciparum, complexe membranaire interne