Clear Sky Science · pl
Białko transportujące lipidy w formie mostu jest kluczowe dla powstawania inwazyjnych stadiów u pasożytów malarii
Jak pasożyty malarii budują swój sprzęt inwazyjny
Pasożyty malarii przetrwają dzięki nieustannemu wnikaniu do nowych czerwonych krwinek. Aby to zrobić, każdy pasożyt rozwijający się wewnątrz komórki musi zbudować dziesiątki drobnych potomków gotowych wyłamać się i zaatakować świeże komórki. Ten projekt budowlany wymaga ogromnych ilości nowej błony, zbudowanej w większości z cząsteczek tłuszczowych zwanych lipidami. Omówione tutaj badanie ujawnia kluczowe „mostowe” białko, które przenosi lipidy wewnątrz pasożyta, umożliwiając mu złożenie maszyny inwazyjnej. Zrozumienie tej ukrytej linii zaopatrzenia może otworzyć nowe sposoby blokowania malarii.
Ukryta architektura wewnątrz zainfekowanej komórki
Po przedostaniu się do czerwonej krwinki pasożyt malarii szybko się mnoży. W późnym etapie cyklu przekształca się w dużą komórkę wypełnioną wieloma jądrami. Wokół każdej przyszłej komórki potomnej pasożyt buduje wspierającą powłokę zwaną wewnętrznym kompleksem błonowym, czyli IMC. Ta powłoka leży tuż pod zewnętrzną powierzchnią i jest niezbędna zarówno do nadania kształtu potomkom, jak i do zapewnienia siły potrzebnej do ich wejścia do następnej krwinki. Budowa IMC od podstaw wymaga stałego dopływu lipidów z wewnętrznej fabryki pasożyta — siateczki śródplazmatycznej (ER). Główne pytanie, jakie postawili badacze, brzmiało: jak te lipidy poruszają się tak szybko i wydajnie od ER do rosnącego IMC?
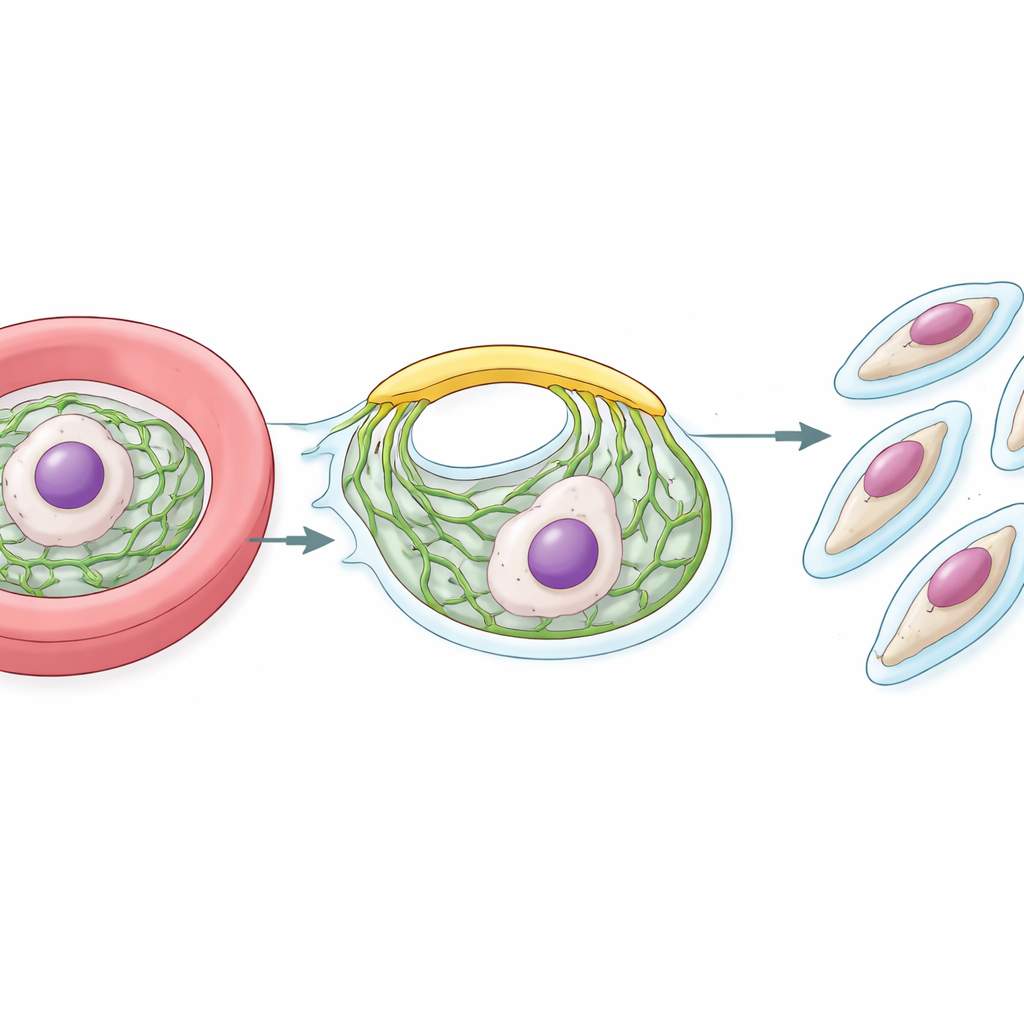
Odnalezienie mostu lipidowego
W wielu organizmach lipidy mogą przemieszczać się bezpośrednio między sąsiadującymi błonami w miejscach bliskiego kontaktu, wspomagane przez wyspecjalizowane białka nośnikowe. Zespół zaczął od znanego białka kotwiczącego ER o nazwie VAP, które wiąże partnerów zawierających krótkie motywy „FFAT”. Korzystając z metody znakowania bliskości, skatalogowali białka znajdujące się w pobliżu VAP na powierzchni ER w pasożytach malarii. Wśród wielu kandydatów zidentyfikowali kilka białek zajmujących się lipidami i skupili się na olbrzymim białku przypominającym VPS13 — rodzinę „mostowych” transporterów lipidów znanych z drożdży i komórek ludzkich. Nazwali to pasożytnicze białko PfVPS13L1.
Jak most łączy dwie błony
Prognozy strukturalne oparte na komputerze ujawniły, że PfVPS13L1 tworzy długą, prętowatą cząsteczkę z wewnętrznym rowkiem, który może pomieścić wiele cząsteczek lipidów naraz. Jeden koniec pręta niesie motyw FFAT, który wiąże się z VAP na ER, przytwierdzając ten koniec do źródła lipidów. Drugi koniec zawiera regiony adapterowe, które zaczepiają się o IMC. Badacze wykazali, że ta końcówka oddziałuje z białkiem IMC, które nazwali PfAegerolysin, co wskazuje, że PfVPS13L1 fizycznie łączy ER z rosnącym IMC. Mikroskopia o wysokiej rozdzielczości potwierdziła, że PfVPS13L1 skupia się dokładnie tam, gdzie formuje się nowa błona IMC wokół przyszłych komórek potomnych.
Co się dzieje, gdy most zostaje zniszczony
Aby sprawdzić funkcję mostu, naukowcy użyli szybkiego triku „przemieszczania”: chemicznie odciągnęli PfVPS13L1 z jego normalnej pozycji na powierzchnię zewnętrzną pasożyta, skutecznie go dezaktywując. Gdy zrobiono to tuż przed etapem, w którym IMC musi rosnąć, pasożyty nie były w stanie wyprodukować prawidłowych potomków. IMC zaczęło się tworzyć, ale później zablokowało się; zamiast owijać się całkowicie wokół każdego jądra, pozostało małe i niekompletne. W rezultacie wiele drobnych, opakowanych w skorupkę ciał pozbawionych było jąder, podczas gdy dodatkowy materiał genetyczny i cytoplazma pozostawały w dużym resztkowym kształcie. Inne struktury, takie jak wyspecjalizowane organelle wydzielnicze, nadal się formowały, co podkreśla, że główna usterka dotyczyła dostarczania błony do IMC.
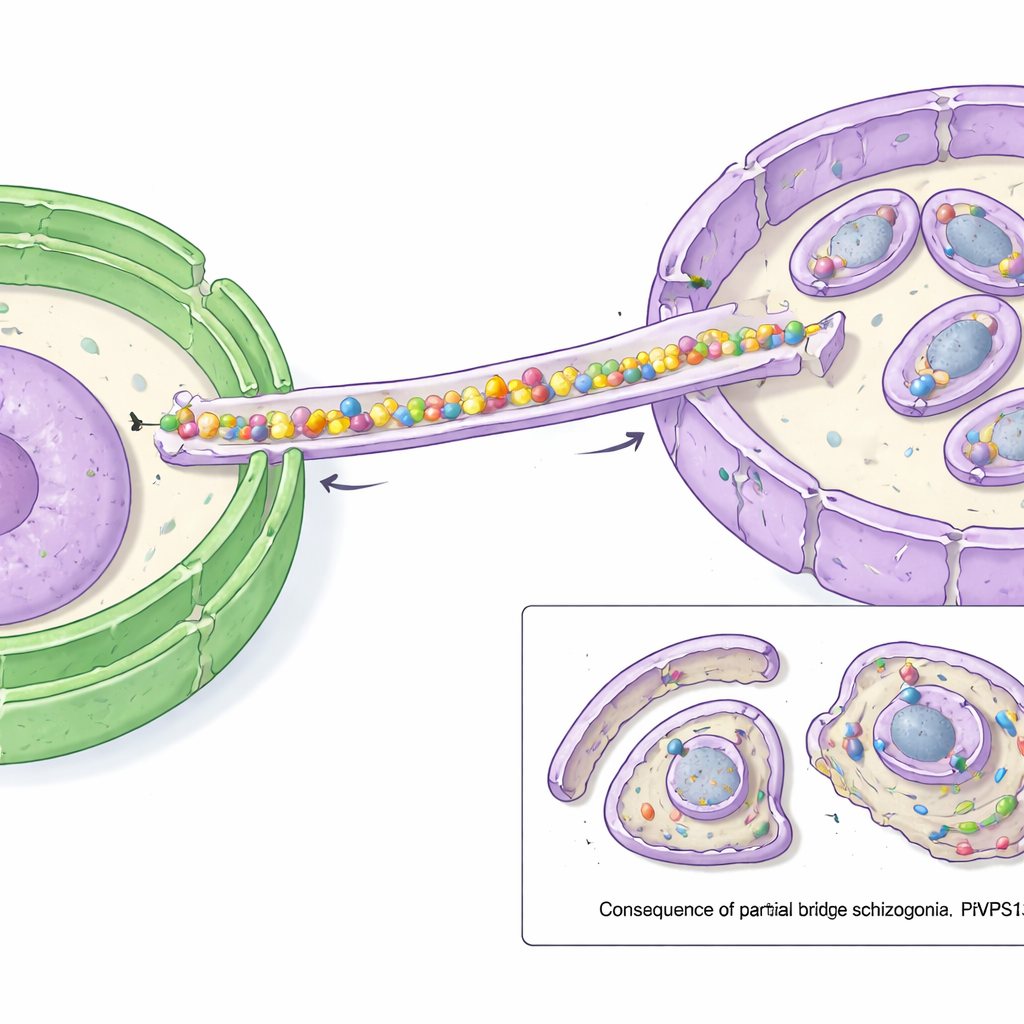
Dlaczego to ważne w walce z malarią
Badanie pokazuje, że PfVPS13L1 jest kluczowym mostem lipidowym, który zasila szybkie rozszerzanie IMC, pozwalając pasożytom malarii generować w pełni ukształtowane, inwazyjne potomstwo. Bez tej masowej ścieżki transportu lipidów z ER pasożyty składają wadliwych potomków, które nie mogą kontynuować cyklu infekcji. Ponieważ podobne białka w formie mostu działają w wielu typach komórek, PfVPS13L1 stanowi pasożytniczą adaptację zachowanego mechanizmu. Celowanie w ten most lub jego partnerów, które mocują go do IMC, mogłoby stanowić nową strategię leków przeciwmalarycznych polegającą na cichym głodzeniu maszyny inwazyjnej pasożyta z potrzebnych błon.
Cytowanie: Guillén-Samander, A., Perepelkina, N., Horáčková, V. et al. A bridge-like lipid transfer protein is critical for generation of invasive stages in malaria parasites. Nat Commun 17, 3030 (2026). https://doi.org/10.1038/s41467-026-70887-1
Słowa kluczowe: malaria, transfer lipidów, biogeneza błon, Plasmodium falciparum, wewnętrzny kompleks błonowy