Clear Sky Science · nl
Een brugachtige lipidoverdracht-eiwit is cruciaal voor de vorming van invasieve stadia bij malaria-parasieten
Hoe malariaparasieten hun invasie-uitrusting bouwen
Malariaparasieten overleven door continu nieuwe rode bloedcellen binnen te dringen. Om dat te doen moet elke parasiet die binnen een cel groeit tientallen kleine nakomelingen bouwen die klaar zijn om eruit te barsten en nieuwe cellen aan te vallen. Dit bouwproject vereist enorme hoeveelheden nieuw membraan, grotendeels gemaakt van vetachtige moleculen die lipiden genoemd worden. De studie die hier samengevat wordt, ontdekt een sleutelproteïne in de vorm van een "brug" die lipiden binnen de parasiet transporteert, waardoor deze de invasieapparatuur kan assembleren. Inzicht in deze verborgen bevoorradingslijn zou nieuwe manieren kunnen openen om malaria te blokkeren.
De verborgen architectuur binnen een geïnfecteerde cel
Eens binnen een rode bloedcel vermenigvuldigt de malariaparasiet zich snel. Laat in zijn cyclus verandert hij in een grote cel vol met vele kernen. Rond elke toekomstige dochtercel bouwt de parasiet een ondersteunende schil genaamd het innerlijk membraancomplex, of IMC. Deze schil ligt net onder het buitenoppervlak en is essentieel zowel voor de vormgeving van de nakomelingen als voor het aandrijven van hun binnendringing in de volgende rode bloedcel. Het opbouwen van het IMC vanaf nul vraagt om een stabiele aanvoer van lipiden vanuit de interne fabriek van de parasiet, het endoplasmatisch reticulum (ER). De grote vraag die de onderzoekers stelden was hoe deze lipiden zo snel en efficiënt van het ER naar het groeiende IMC verplaatsen.
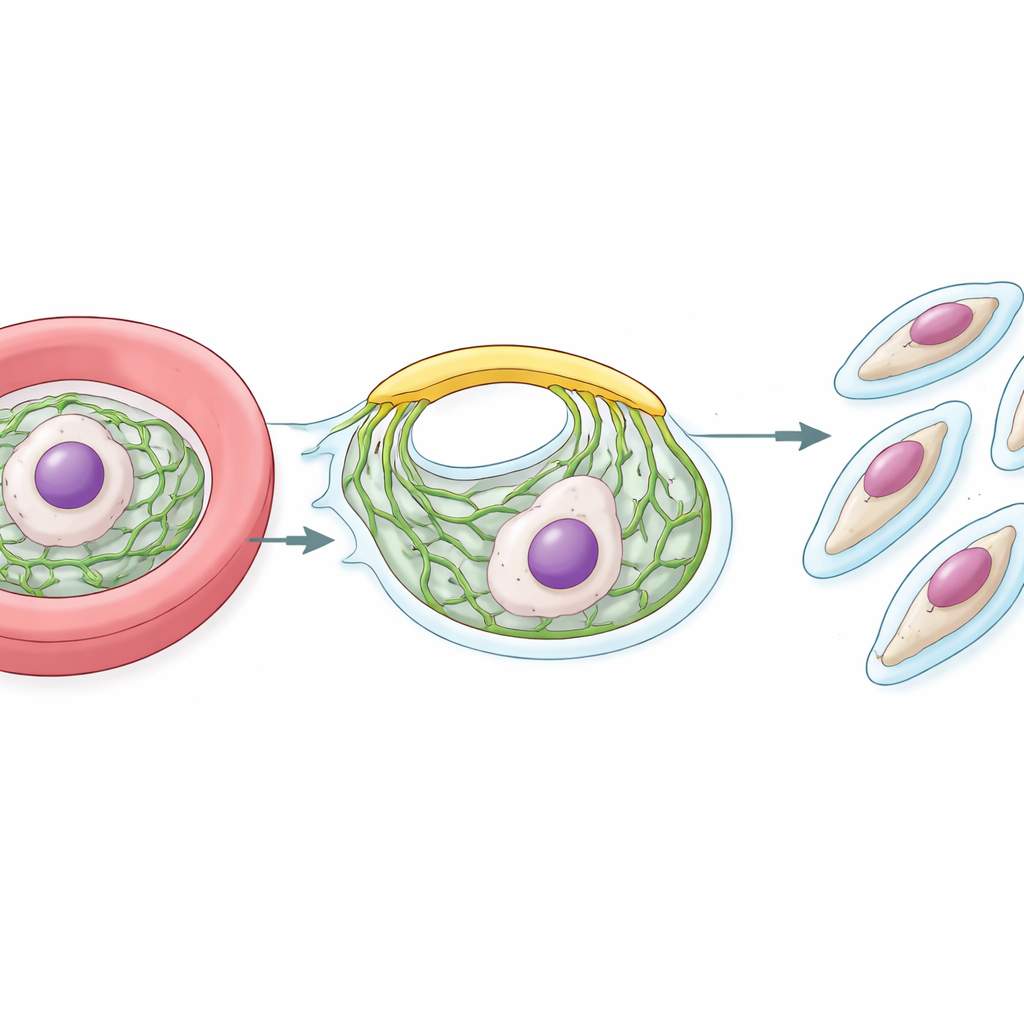
De vinding van de lipidbrug
In veel organismen kunnen lipiden rechtstreeks bewegen tussen aangrenzende membranen op nauwe contactplaatsen, geholpen door speciale draag-eiwitten. Het team begon bij een bekend ER-ankerprotein genaamd VAP, dat partners vasthoudt die korte "FFAT"-motieven bevatten. Met een nabijheidslabelingmethode brachten ze eiwitten in kaart die zich dicht bij VAP op het ER-oppervlak bevinden in malariaparasieten. Onder vele kandidaten identificeerden ze verscheidene lipidebehandelende eiwitten en concentreerden ze zich op een reusachtig eiwit dat leek op VPS13, een familie van "brugachtige" lipide-transporteurs bekend uit gist- en menselijke cellen. Ze noemden dit parasitaire eiwit PfVPS13L1.
Hoe de brug twee membranen verbindt
Computergebaseerde structurele voorspellingen toonden aan dat PfVPS13L1 een lange, staafvormige molecule vormt met een interne groef die vele lipidemoleculen tegelijk kan bevatten. Het ene uiteinde van de staaf draagt een FFAT-motief dat bindt aan VAP in het ER en dat uiteinde zo aan de lipidenbron vastzet. Het andere uiteinde bevat adapterregio's die zich vastklampen aan het IMC. De onderzoekers toonden aan dat deze tip interactie aangaat met een IMC-eiwit dat zij PfAegerolysin noemden, wat aangeeft dat PfVPS13L1 fysiek het ER en het groeiende IMC overbrugt. Microscopen met hoge resolutie bevestigden dat PfVPS13L1 zich concentreert precies daar waar nieuw IMC-membraan zich vormt rond toekomstige dochtercellen.
Wat er gebeurt als de brug breekt
Om te testen wat de brug doet, gebruikten de wetenschappers een snel "mislocalisatie"-truc: ze sleepten PfVPS13L1 chemisch weg van zijn normale plaats naar het buitenoppervlak van de parasiet, waarmee ze het effectief uitschakelden. Wanneer dit werd gedaan net vóór het stadium waarin het IMC moet groeien, konden parasieten geen normale nakomelingen meer produceren. Het IMC begon zich te vormen maar stokte vervolgens; in plaats van zich volledig rond elke kern te wikkelen bleef het klein en onvolledig. Als gevolg daarvan ontbraken bij veel kleine, omhulde lichaampjes de kernen, terwijl extra genetisch materiaal en cytoplasma achterbleven in een grote restblob. Andere structuren, zoals gespecialiseerde secretaire organellen, vormden zich nog steeds, wat benadrukt dat de belangrijkste tekortkoming lag in de toevoer van membraan voor het IMC.
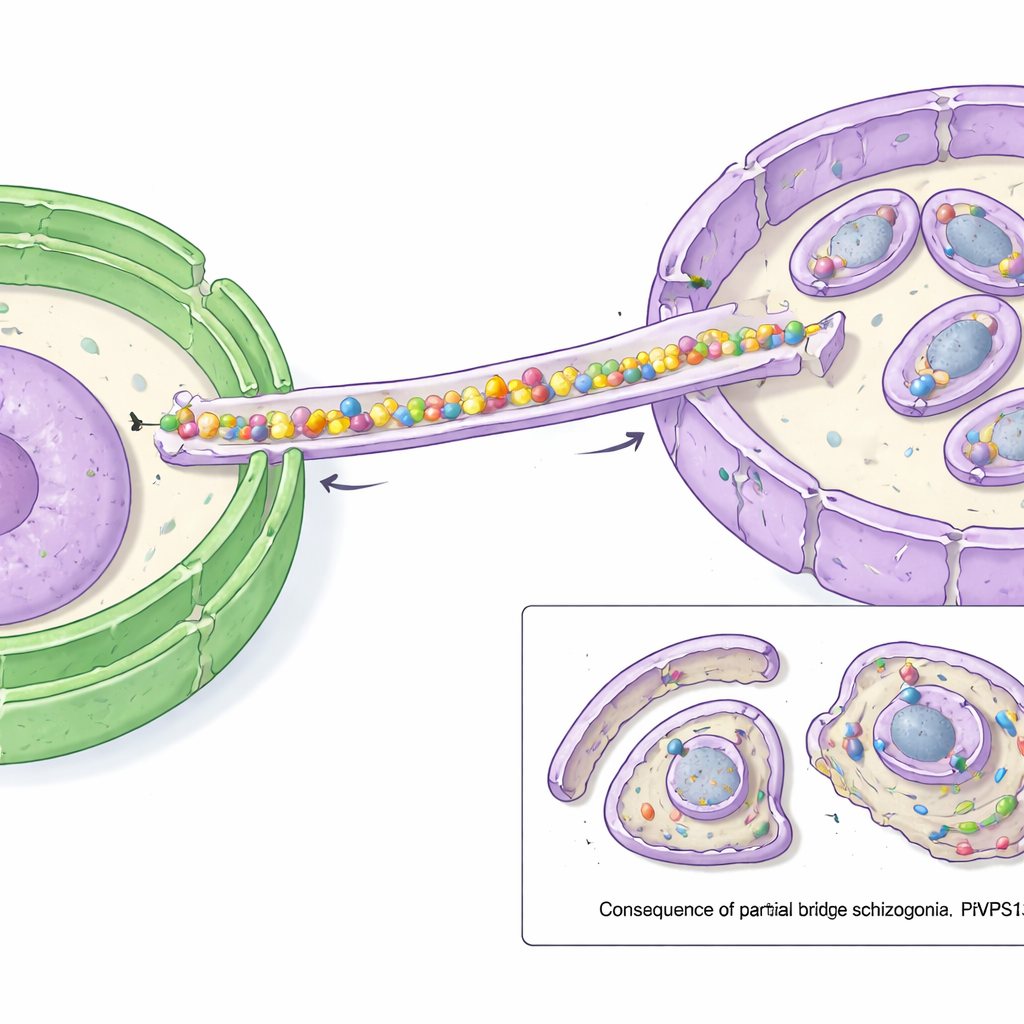
Waarom dit van belang is voor de bestrijding van malaria
De studie toont aan dat PfVPS13L1 een cruciale lipidbrug is die de snelle uitbreiding van het IMC voedt, waardoor malariaparasieten volledig gevormde, invasieve nakomelingen kunnen genereren. Zonder deze grootschalige lipidoverdrachtspad vanuit het ER assembleren de parasieten defecte nakomelingen die de infectiecyclus niet kunnen voortzetten. Omdat vergelijkbare brugachtige eiwitten in veel celtypen functioneren, vertegenwoordigt PfVPS13L1 een parasiet-specifieke aanpassing van een geconserveerd mechanisme. Het richten op deze brug, of op zijn partners die het aan het IMC verankeren, zou een nieuwe strategie kunnen vormen voor antimalariamiddelen die subtiel het invasieapparaat van de parasiet van het benodigde membraan verarmen.
Bronvermelding: Guillén-Samander, A., Perepelkina, N., Horáčková, V. et al. A bridge-like lipid transfer protein is critical for generation of invasive stages in malaria parasites. Nat Commun 17, 3030 (2026). https://doi.org/10.1038/s41467-026-70887-1
Trefwoorden: malaria, lipidoverdracht, membraanbiogenese, Plasmodium falciparum, innerlijk membraancomplex