Clear Sky Science · sv
En broliknande lipidochöverföringsprotein är avgörande för bildandet av invasiva stadier i malaria-parasiter
Hur malariaparasiter bygger sitt invasionsutrustning
Malariaparasiter överlever genom att ständigt invadera nya röda blodkroppar. För att göra detta måste varje parasit som växer inne i en cell bygga dussintals små avkommor som är redo att bryta sig ut och angripa nya celler. Detta byggprojekt kräver stora mängder nytt membran, till största delen uppbyggt av fettsyraliknande molekyler kallade lipider. Studien som sammanfattas här upptäcker ett nyckelprotein som fungerar som en "bro" och transporterar lipider inne i parasiten, vilket gör det möjligt att montera invasionsmaskineriet. Att förstå denna dolda försörjningslinje kan öppna nya vägar för att blockera malaria.
Den dolda arkitekturen inne i en infekterad cell
När parasiten väl är inne i en röd blodkropp förökar den sig snabbt. Sent i cykeln omvandlas den till en stor cell fylld med många kärnor. Runt varje framtida dottercell bygger parasiten ett stödjande skal kallat det inre membrankomplexet, eller IMC. Detta skal ligger precis under ytan och är avgörande både för att forma avkommorna och för att driva deras inträde i nästa röda blodkropp. Att bygga IMC från grunden kräver ett stadigt flöde av lipider från parasitens interna fabrik, det endoplasmatiska retiklet (ER). Den stora frågan forskarna ställde var hur dessa lipider rör sig så snabbt och effektivt från ER till det växande IMC.
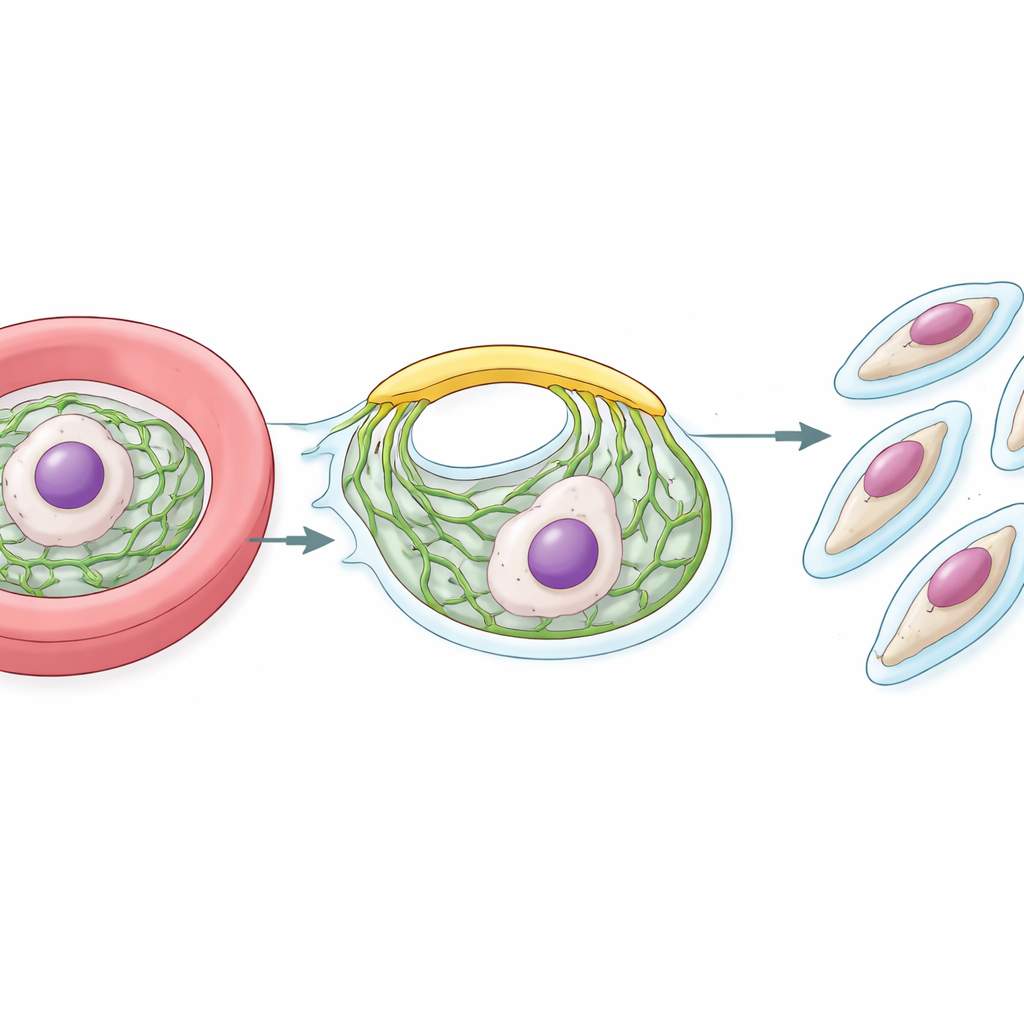
Att finna lipidbron
I många organismer kan lipider förflytta sig direkt mellan intilliggande membraner vid nära kontaktställen, assisterade av särskilda bärarproteiner. Teamet utgick från ett känt ER-ankarsprotein kallat VAP, som binder partnerproteiner som innehåller korta "FFAT"-motiv. Genom en närhetsmärkningsteknik katalogiserade de proteiner som sitter nära VAP på ER-ytan i malariaparasiter. Bland många kandidater identifierade de flera lipidhanteringsproteiner och fokuserade på ett jättestort som liknade VPS13, en familj av "bro-liknande" lipidtransportörer kända från jäst och humana celler. De namngav detta parasitprotein PfVPS13L1.
Hur bron kopplar samman två membraner
Databaserade strukturbeskrivningar visade att PfVPS13L1 bildar en lång, stavformad molekyl med en intern fåra som kan hålla många lipidmolekyler samtidigt. Ena änden av staven bär ett FFAT-motiv som binder till VAP vid ER och förankrar den änden till lipidkällan. Den andra änden innehåller adapterregioner som hakar fast vid IMC. Forskarna visade att denna spets interagerar med ett IMC-protein som de kallade PfAegerolysin, vilket indikerar att PfVPS13L1 fysiskt fungerar som en bro mellan ER och det växande IMC. Högupplöst mikroskopi bekräftade att PfVPS13L1 samlas exakt där nytt IMC-membran bildas runt de framtida dottercellerna.
Vad som händer när bron bryts
För att testa vad bron gör använde forskarna ett snabbt "felplacering"-knep: de kemiskt drog PfVPS13L1 bort från dess normala position till parasitens yta, vilket effektivt inaktiverade det. När detta gjordes strax innan stadiet då IMC måste växa kunde parasiterna inte längre producera normala avkommor. IMC började bildas men stannade sedan av; istället för att omsluta varje kärna fullständigt förblev det litet och ofullständigt. Som ett resultat saknade många små skalomslutna kroppar kärnor, medan extra genetiskt material och cytoplasma lämnades kvar i en stor kvarvarande klump. Andra strukturer, såsom specialiserade sekretoriska organeller, bildades fortfarande, vilket understryker att huvudfelet låg i att förse IMC med membran.
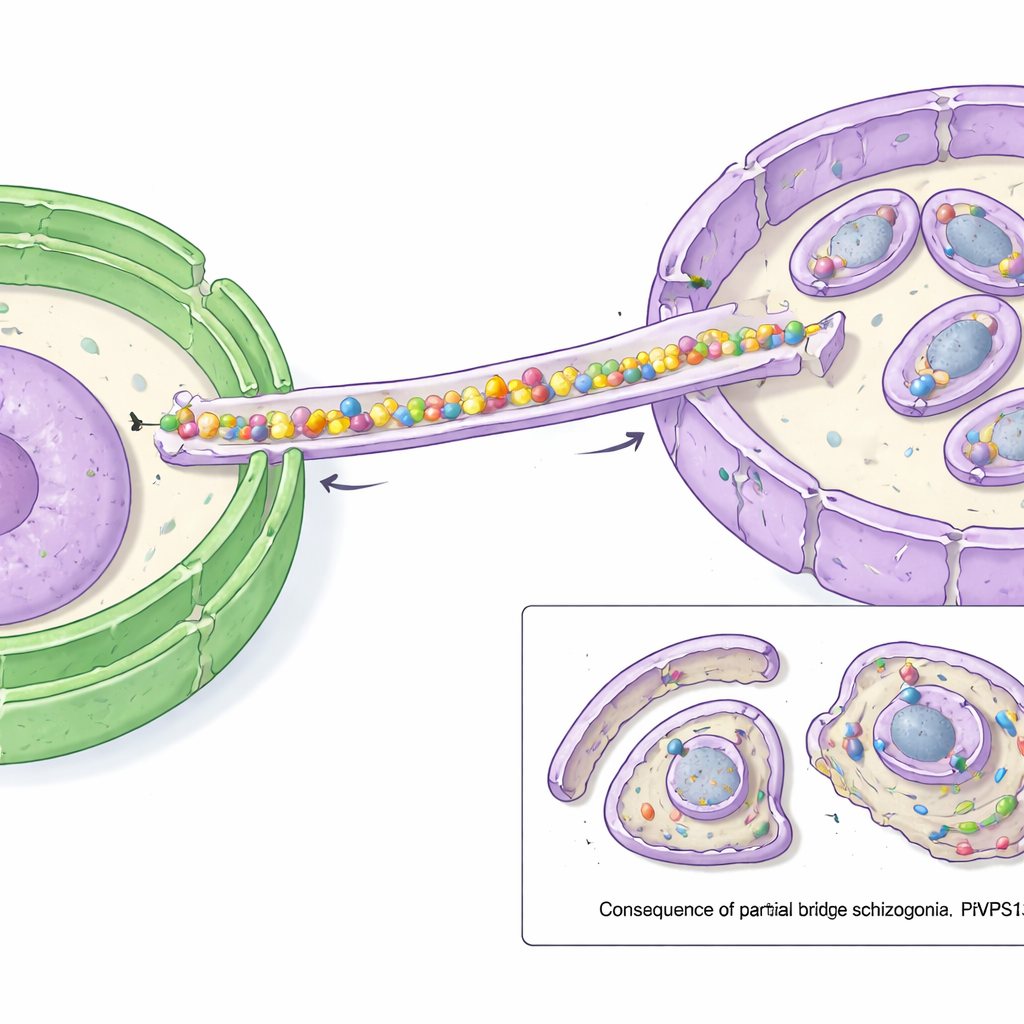
Varför detta är viktigt för kampen mot malaria
Studien visar att PfVPS13L1 är en avgörande lipidbro som driver den snabba expansionen av IMC, vilket gör det möjligt för malariaparasiter att generera fullbildade, invasiva avkommor. Utan denna bulköverföringsväg av lipider från ER bygger parasiterna defekta avkommor som inte kan fortsätta infektionens cykel. Eftersom liknande bro-liknande proteiner finns i många celltyper representerar PfVPS13L1 en parassitspecifik anpassning av en bevarad mekanism. Att rikta in sig på denna bro, eller dess partner som säkrar den mot IMC, skulle kunna erbjuda en ny strategi för antimalariamedel som tyst svälter parasitens invasionsmaskineri på de membran det behöver.
Citering: Guillén-Samander, A., Perepelkina, N., Horáčková, V. et al. A bridge-like lipid transfer protein is critical for generation of invasive stages in malaria parasites. Nat Commun 17, 3030 (2026). https://doi.org/10.1038/s41467-026-70887-1
Nyckelord: malaria, lipidöverföring, membranbiogenes, Plasmodium falciparum, inre membrankomplex