Clear Sky Science · he
חלבון מעביר שומנים בדמיון לגשר חיוני ליצירת שלבים פולשניים בטפילי מלריה
איך טפילי המלריה בונים את כלי החדירה שלהם
טפילי המלריה שורדים על ידי פלישה אינסופית לתאי דם אדומים חדשים. כדי לעשות זאת, כל טפיל הגדל בתוך תא חייב לבנות עשרות צאצאים זעירים שמוכנים לפרוץ החוצה ולתקוף תאים טריים. פרויקט הבנייה הזה דורש כמויות עצומות של ממברנה חדשה, שמורכבת בעיקר ממולקולות שומן הנקראות ליפידים. המחקר המתואר כאן חושף חלבון "גשר" מרכזי שמוביל ליפידים בתוך הטפיל, ומאפשר לו להרכיב את כלי החדירה. הבנת קו האספקה החבוי הזה עשויה לפתוח דרכים חדשות לחסום את המלריה.
הארכיטקטורה הסמויה בתוך תא נגוע
לאחר כניסתו לתא דם אדום, הטפיל מתרבה במהירות. בשלב מאוחר במחזורו הוא הופך לתא גדול שמלא בגרעינים רבים. מסביב לכל תא בת עתידי, הטפיל בונה מעטפת תומכת שנקראת המִרְכָּבַת הממברנה הפנימית, או IMC. מעטפת זו יושבת מתחת לפני השטח החיצוני והיא חיונית הן לעיצוב הצאצאים והן להפעלת יכולתם להיכנס לתא הדם הבא. בניית ה‑IMC מאפס דורשת זרם קבוע של ליפידים ממפעל הפנימי של הטפיל, הרשת האנדופלסמטית (ER). השאלה המרכזית שהחוקרים שאלו היא כיצד ליפידים אלה נעים במהירות וביעילות מהרשת ה‑ER אל ה‑IMC המתפתח.
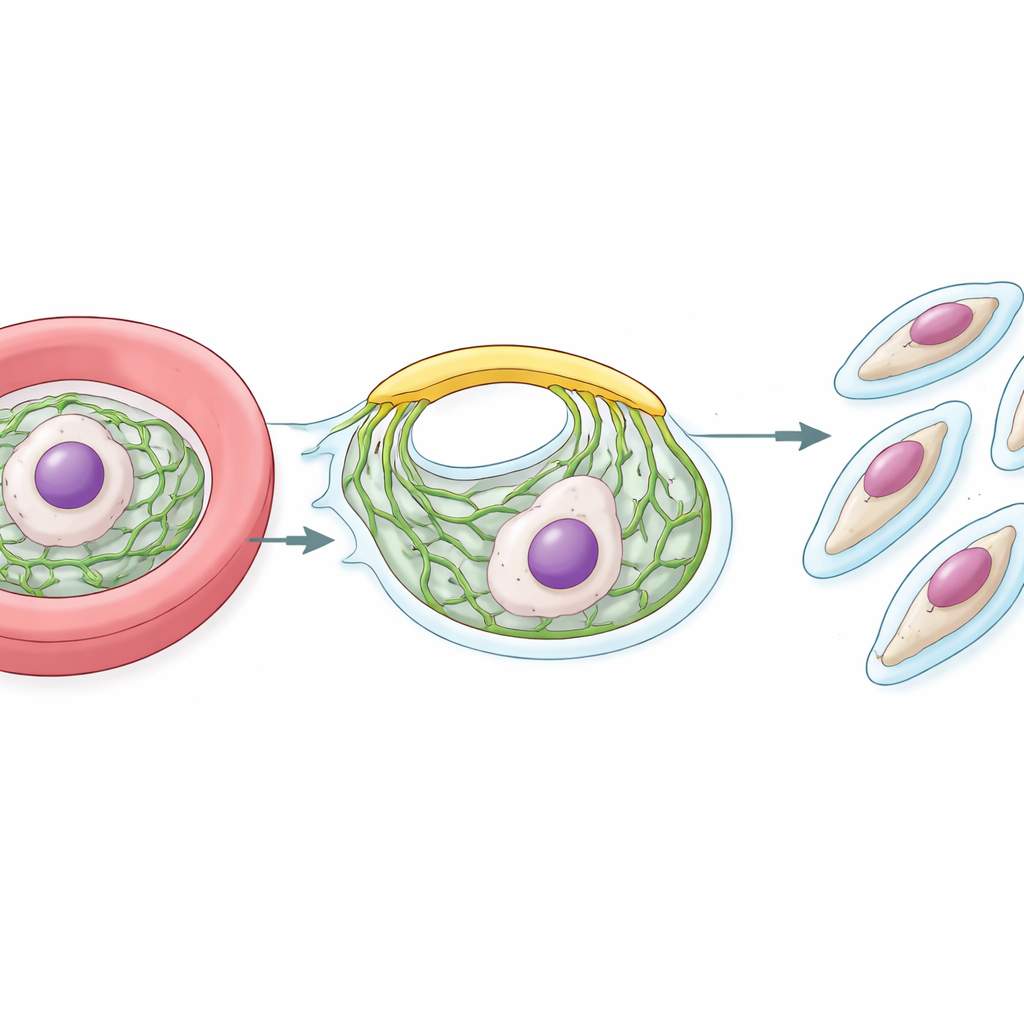
גילוי גשר הליפידים
במאורגניזמים רבים ליפידים יכולים לנוע ישירות בין ממברנות סמוכות באתרי מגע, בסיוע חלבונים נשאיים מיוחדים. הצוות התחיל מחלבון מעגן ברשת ה‑ER שנקרא VAP, שמושך שותפים שמכילים מוטיבים קצרים מסוג "FFAT". באמצעות שיטת תיוג קרבה, הם קיבעו קטלוג של חלבונים היושבים בסמיכות ל‑VAP על פני שטח ה‑ER בטפילי המלריה. בין מועמדים רבים זוהו כמה חלבונים המטפלים בליפידים והם התמקדו בחלבון ענק שהתאים ל‑VPS13, משפחה של מעבירים ליפידים "בדמיון לגשר" הידועה על שמוש בני יסט ותאים אנושיים. הם נתנו לחלבון הטפיל את השם PfVPS13L1.
כיצד הגשר מחבר שתי ממברנות
תחזיות מבניות מבוססות מחשב חשפו ש‑PfVPS13L1 יוצר מולקולה ארוכה בצורת מוט עם חריץ פנימי שיכול להכיל מולקולות ליפיד רבות בבת אחת. קצה אחד של המוט נושא מוטיב FFAT הקושר את VAP ב‑ER, וקובע את אותו קצה כמקור הליפידים. הקצה השני מכיל אזורים מתאמים שנצמדים ל‑IMC. החוקרים הראו שהקצה הזה מתקשר עם חלבון IMC אותו קראו PfAegerolysin, מה שמרמז כי PfVPS13L1 גשר פיזי בין ה‑ER ל‑IMC המתפתח. מיקרוסקופיה ברזולוציה גבוהה אישרה כי PfVPS13L1 מקבץ עצמו בדיוק במקום שבו ממברנת ה‑IMC החדשה נבנית סביב תאי הבת העתידיים.
מה קורה כשהגשר נשבר
כדי לבדוק את תפקיד הגשר, המדענים השתמשו בטריק מהיר של "שינוי מיקום": הם הסיטו כימית את PfVPS13L1 מהמיקום הרגיל שלו אל פני השטח החיצוני של הטפיל, ובכך נטרלו אותו בפועל. כאשר נעשה זאת ממש לפני השלב שבו ה‑IMC חייב לגדול, הטפילים לא יכלו עוד לייצר צאצאים תקינים. ה‑IMC התחיל להיווצר אך נעצר; במקום להתקפל במלואו סביב כל גרעין, הוא נשאר קטן וחסר. כתוצאה מכך, גופים קטנים עטופים בקליפה רבים נותרו חסרי גרעין, בעוד חומר גנטי וציטופלזמה עודפים הושארו בגוש גדול שולי. מבנים אחרים, כמו אברונים סקרטוריים מיוחדים, עדיין נוצרו, מה שמדגיש שהכשל העיקרי היה באספקת ממברנה ל‑IMC.
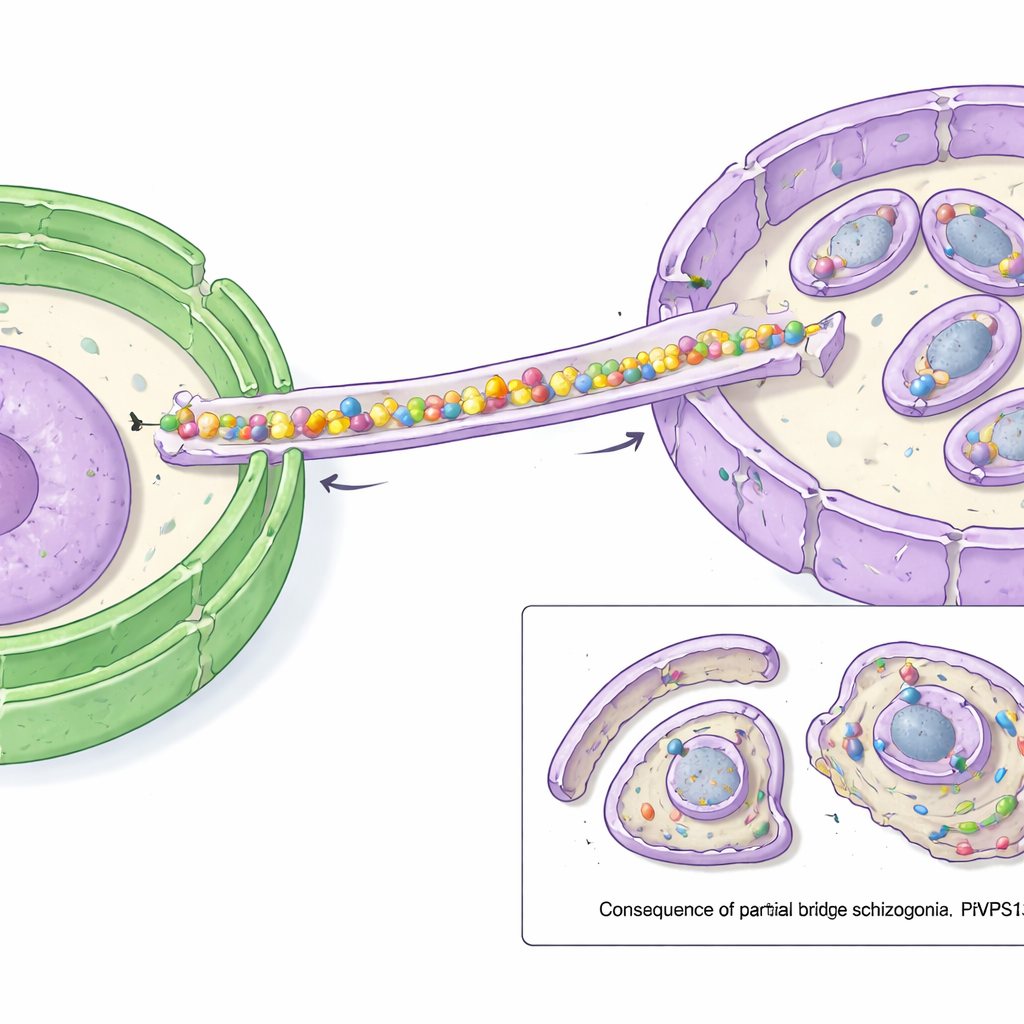
מדוע הדבר חשוב במאבק במלריה
המחקר מראה ש‑PfVPS13L1 הוא גשר ליפידים חיוני המניע את ההתרחבות המהירה של ה‑IMC, ומאפשר לטפילי המלריה לייצר צאצאים שלמים ופולשניים. ללא מסלול העברת הליפידים ההמוני הזה מה‑ER, הטפילים מרכיבים צאצאים פגומים שאינם יכולים להמשיך את מעגל ההדבקה. מאחר שחלבונים דמויי‑גשר דומים פועלים בסוגים רבים של תאים, PfVPS13L1 מייצג הסתגלות ספציפית לטפיל של מנגנון שמור. מיתוג הגשר הזה, או של שותפיו שמייצבים אותו ב‑IMC, עשוי להציע אסטרטגיה חדשה לתרופות אנטימלריות שמטרתן להרעיב בשקט את כלי החדירה של הטפיל מהממברנות שהוא צריך.
ציטוט: Guillén-Samander, A., Perepelkina, N., Horáčková, V. et al. A bridge-like lipid transfer protein is critical for generation of invasive stages in malaria parasites. Nat Commun 17, 3030 (2026). https://doi.org/10.1038/s41467-026-70887-1
מילות מפתח: מלריה, העברת שומנים, ביוגנזה של ממברנות, Plasmodium falciparum, מִרְכָּבַת הממברנה הפנימית