Clear Sky Science · de
Ein brückenartiges Lipid-Transferprotein ist entscheidend für die Bildung invasiver Stadien bei Malariaerregern
Wie Malariaerreger ihre Invasionsausrüstung aufbauen
Malariaerreger überleben, indem sie fortwährend neue rote Blutkörperchen infestieren. Dazu muss jeder Parasit, der innerhalb einer Zelle heranwächst, Dutzende winziger Nachkommen bauen, die bereit sind auszubrechen und neue Zellen anzugreifen. Dieses Bauvorhaben erfordert große Mengen neuer Membran, die überwiegend aus Fettmolekülen, sogenannten Lipiden, besteht. Die hier zusammengefasste Studie entdeckt ein zentrales „Brücken“-Protein, das Lipide innerhalb des Parasiten transportiert und so den Zusammenbau der Invasionsmaschinerie ermöglicht. Das Verständnis dieser verborgenen Lieferkette könnte neue Wege eröffnen, Malaria zu blockieren.
Die verborgene Architektur in einer infizierten Zelle
Sobald der Parasit in einem roten Blutkörperchen ist, vermehrt er sich rasch. Spät in seinem Zyklus verwandelt er sich in eine große Zelle, die viele Zellkerne enthält. Um jede zukünftige Tochterzelle herum baut der Parasit eine stützende Hülle, das sogenannte innere Membrankomplex (IMC). Diese Hülle liegt direkt unter der Außenwand und ist sowohl für die Formgebung der Nachkommen als auch für deren Fähigkeit, in das nächste rote Blutkörperchen einzudringen, unerlässlich. Der Aufbau des IMC von Grund auf erfordert einen stetigen Strom von Lipiden aus der internen Fabrik des Parasiten, dem endoplasmatischen Retikulum (ER). Die zentrale Frage der Forscher war, wie diese Lipide so schnell und effizient vom ER zum wachsenden IMC gelangen.
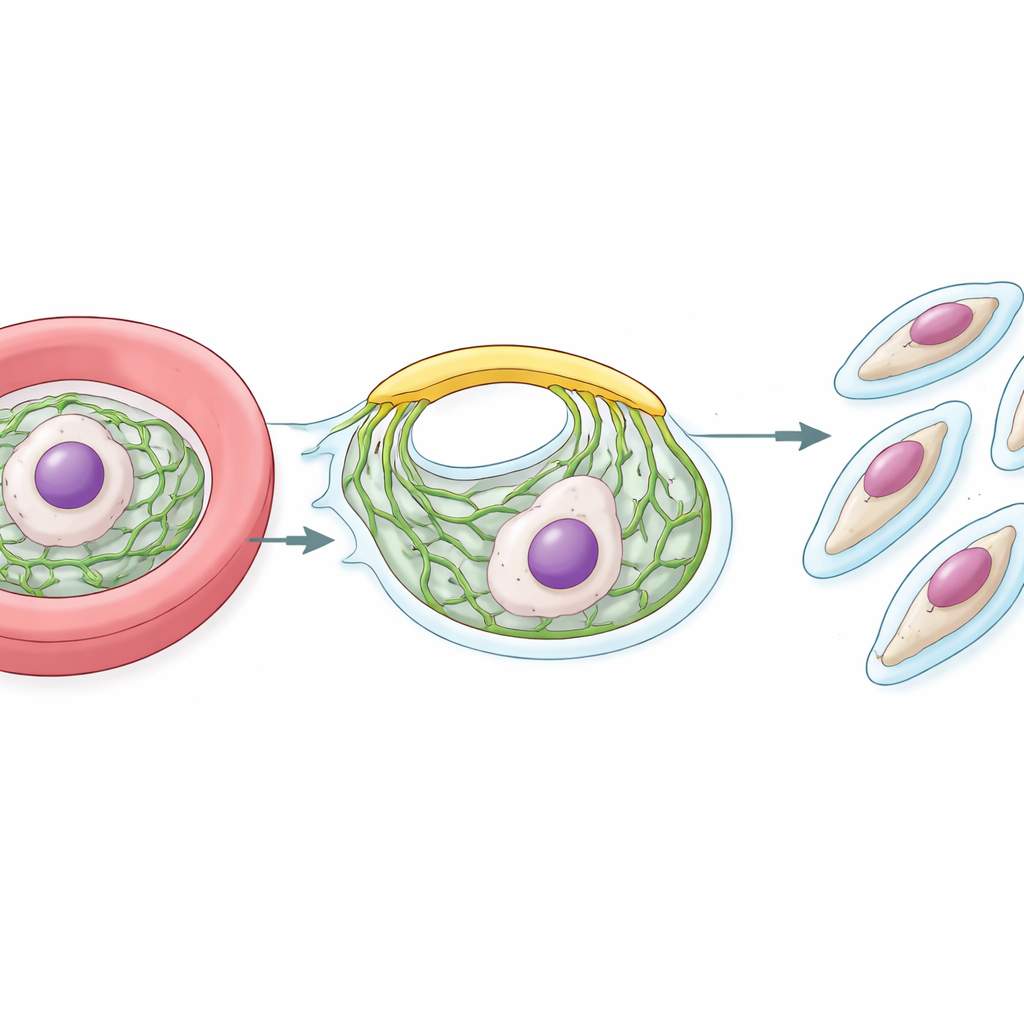
Die Entdeckung der Lipidbrücke
In vielen Organismen können Lipide direkt zwischen benachbarten Membranen an Kontaktstellen wandern, unterstützt von speziellen Transportproteinen. Das Team begann mit einem bekannten ER-Verankerungsprotein namens VAP, das Partner mit kurzen „FFAT“-Motiven anzieht. Mithilfe einer Proximity-Labeling-Methode katalogisierten sie Proteine, die in der Nähe von VAP an der ER-Oberfläche in Malariaparasiten sitzen. Unter vielen Kandidaten identifizierten sie mehrere lipidverarbeitende Proteine und konzentrierten sich auf ein riesiges Molekül, das VPS13 ähnelte – einer Familie von „brückenartigen“ Lipidtransportern, die aus Hefe und menschlichen Zellen bekannt sind. Sie nannten dieses Parasitenprotein PfVPS13L1.
Wie die Brücke zwei Membranen verbindet
Computergestützte Strukturvorhersagen zeigten, dass PfVPS13L1 eine lange, stäbchenförmige Struktur mit einer inneren Rinne bildet, die viele Lipidmoleküle gleichzeitig aufnehmen kann. Ein Ende des Stäbchens trägt ein FFAT-Motiv, das an VAP am ER bindet und dieses Ende an der Lipidquelle fixiert. Das andere Ende besitzt Adapterbereiche, die am IMC andocken. Die Forscher zeigten, dass diese Spitze mit einem IMC-Protein interagiert, das sie PfAegerolysin nannten, was darauf hinweist, dass PfVPS13L1 physisch das ER und das wachsende IMC überbrückt. Hochauflösende Mikroskopie bestätigte, dass PfVPS13L1 genau dort konzentriert ist, wo sich neue IMC-Membran um zukünftige Tochterzellen bildet.
Was passiert, wenn die Brücke bricht
Um die Funktion der Brücke zu testen, nutzten die Wissenschaftler einen schnellen „Fehlplatzierungs“-Trick: Sie zogen PfVPS13L1 chemisch von seiner normalen Position an die Außenfläche des Parasiten, wodurch es effektiv deaktiviert wurde. Wenn dies kurz vor der Phase geschah, in der das IMC wachsen muss, konnten die Parasiten keine normalen Nachkommen mehr produzieren. Das IMC begann sich zwar zu bilden, blieb dann aber stehen; statt sich vollständig um jeden Kern zu legen, blieb es klein und unvollständig. Infolgedessen fehlten vielen winzigen, schalenumhüllten Einheiten die Zellkerne, während zusätzliches genetisches Material und Zytoplasma in einem großen Restklumpen zurückblieben. Andere Strukturen, wie spezialisierte sekretorische Organellen, bildeten sich weiterhin, was hervorhebt, dass das Hauptproblem in der Membranversorgung des IMC lag.
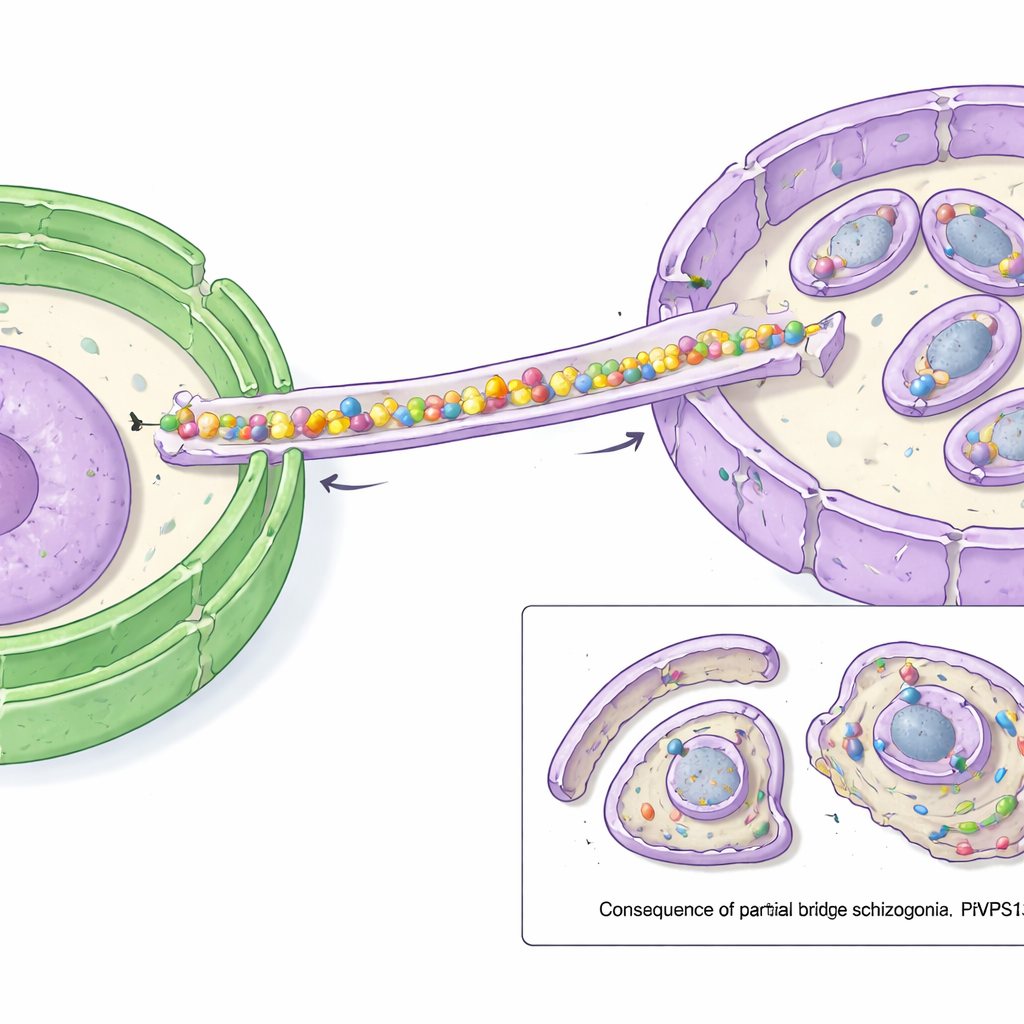
Warum das für den Kampf gegen Malaria wichtig ist
Die Studie zeigt, dass PfVPS13L1 eine entscheidende Lipidbrücke ist, die das schnelle Wachstum des IMC antreibt und es den Malariaerregern ermöglicht, voll entwickelte, invasive Nachkommen zu erzeugen. Ohne diesen Massentransferweg von Lipiden aus dem ER bauen die Parasiten fehlerhafte Nachkommen, die den Infektionszyklus nicht fortsetzen können. Da ähnliche brückenartige Proteine in vielen Zelltypen vorkommen, stellt PfVPS13L1 eine parasitespezifische Anpassung eines konservierten Mechanismus dar. Die Zielsetzung dieser Brücke oder ihrer Partner, die sie am IMC verankern, könnte eine neue Strategie für antimalariale Wirkstoffe bieten, die die Invasionsausrüstung des Parasiten still und gezielt der Membranversorgung berauben.
Zitation: Guillén-Samander, A., Perepelkina, N., Horáčková, V. et al. A bridge-like lipid transfer protein is critical for generation of invasive stages in malaria parasites. Nat Commun 17, 3030 (2026). https://doi.org/10.1038/s41467-026-70887-1
Schlüsselwörter: Malaria, Lipidtransfer, Membranbiogenese, Plasmodium falciparum, Inneres Membrankomplex