Clear Sky Science · es
Una proteína transportadora de lípidos en forma de puente es crítica para la generación de etapas invasivas en parásitos de la malaria
Cómo los parásitos de la malaria construyen su equipo de invasión
Los parásitos de la malaria sobreviven invadiendo de forma continua nuevos glóbulos rojos. Para lograrlo, cada parásito que crece dentro de una célula debe construir docenas de diminutos descendientes listos para estallar y atacar células frescas. Este proyecto de construcción requiere enormes cantidades de membrana nueva, formada en su mayor parte por moléculas grasas llamadas lípidos. El estudio resumido aquí descubre una proteína clave en forma de "puente" que transporta lípidos dentro del parásito, permitiéndole ensamblar la maquinaria de invasión. Comprender esta vía de suministro oculta podría abrir nuevas formas de bloquear la malaria.
La arquitectura oculta dentro de una célula infectada
Una vez dentro de un glóbulo rojo, el parásito de la malaria se multiplica rápidamente. Hacia el final de su ciclo, se convierte en una célula grande abarrotada de muchos núcleos. Alrededor de cada futura célula hija, el parásito construye una cáscara de soporte llamada complejo de membrana interna, o IMC. Esta cáscara se sitúa justo por debajo de la superficie externa y es esencial tanto para dar forma a la descendencia como para impulsar su entrada en el siguiente glóbulo rojo. Construir el IMC desde cero exige un flujo constante de lípidos procedentes de la fábrica interna del parásito, el retículo endoplásmico (RE). La gran pregunta que se plantearon los investigadores fue cómo se mueven estos lípidos tan rápida y eficazmente desde el RE hasta el IMC en crecimiento.
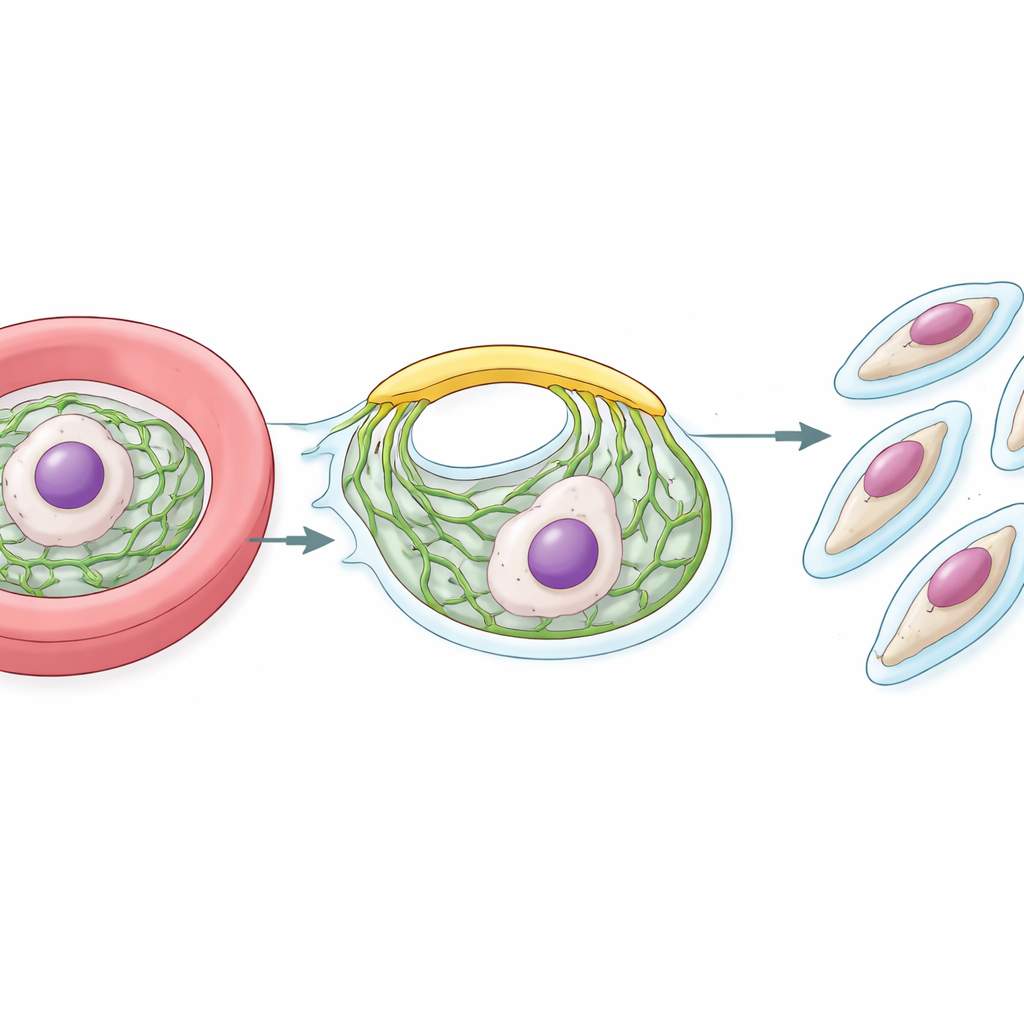
Encontrando el puente de lípidos
En muchos organismos, los lípidos pueden moverse directamente entre membranas vecinas en sitios de contacto próximos, ayudados por proteínas transportadoras especiales. El equipo partió de una proteína anclada al RE conocida como VAP, que captura socios que contienen motivos cortos "FFAT". Usando un método de etiquetado por proximidad, catalogaron las proteínas que se sitúan cerca de VAP en la superficie del RE en los parásitos de la malaria. Entre muchos candidatos identificaron varias proteínas implicadas en el manejo de lípidos y se centraron en una gigante que se parecía a VPS13, una familia de transportadores de lípidos «en forma de puente» conocida en levaduras y células humanas. Nombraron a esta proteína del parásito PfVPS13L1.
Cómo el puente conecta dos membranas
Predicciones estructurales basadas en ordenador revelaron que PfVPS13L1 forma una larga molécula en forma de varilla con una ranura interna capaz de alojar muchas moléculas de lípidos a la vez. Un extremo de la varilla porta un motivo FFAT que se une a VAP en el RE, fijando ese extremo a la fuente de lípidos. El otro extremo contiene regiones adaptadoras que se enganchan al IMC. Los investigadores demostraron que esta punta interactúa con una proteína del IMC que denominaron PfAegerolysin, lo que indica que PfVPS13L1 puentea físicamente el RE y el IMC en crecimiento. Microscopía de alta resolución confirmó que PfVPS13L1 se agrupa precisamente donde se forma nueva membrana del IMC alrededor de las futuras células hijas.
Qué sucede cuando el puente se rompe
Para probar la función del puente, los científicos utilizaron un truco rápido de “deslocalización”: arrastraron químicamente PfVPS13L1 fuera de su posición normal hacia la superficie externa del parásito, inhabilitándola efectivamente. Cuando esto se hizo justo antes de la etapa en la que el IMC debe crecer, los parásitos dejaron de poder producir descendientes normales. El IMC empezó a formarse pero luego se detuvo; en lugar de envolverse completamente alrededor de cada núcleo, permaneció pequeño e incompleto. Como resultado, muchos cuerpos diminutos envueltos en cáscara carecían de núcleos, mientras que material genético y citoplasma sobrante quedaban atrás en una gran masa residual. Otras estructuras, como orgánulos secretores especializados, aún se formaron, lo que subraya que el fallo principal residía en el suministro de membrana para el IMC.
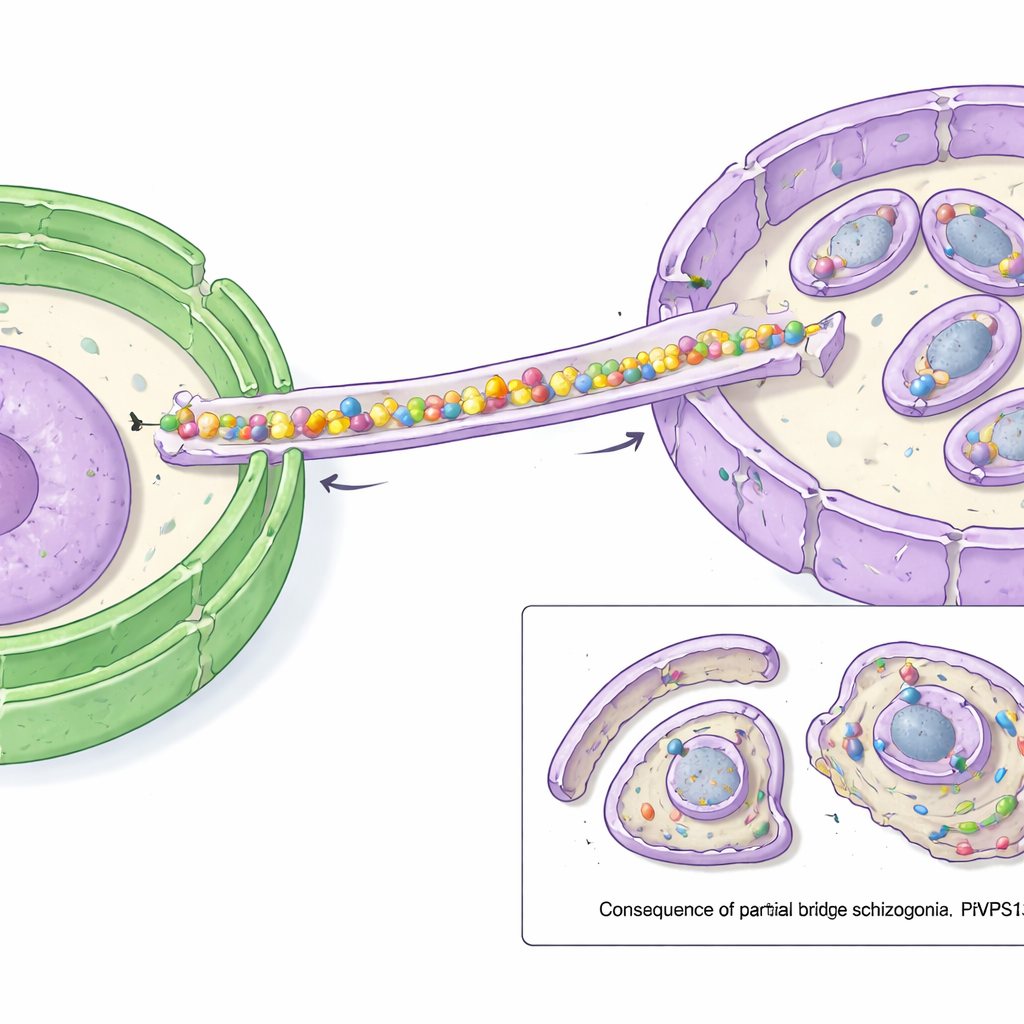
Por qué esto importa para combatir la malaria
El estudio demuestra que PfVPS13L1 es un puente esencial de lípidos que alimenta la rápida expansión del IMC, permitiendo a los parásitos de la malaria generar progenie completamente formadas e invasivas. Sin esta vía de transferencia masiva de lípidos desde el RE, los parásitos ensamblan descendientes defectuosos que no pueden continuar el ciclo de infección. Dado que proteínas similares en forma de puente operan en muchos tipos de células, PfVPS13L1 representa una adaptación específica del parásito de un mecanismo conservado. Apuntar a este puente, o a sus socios que lo aseguran al IMC, podría ofrecer una nueva estrategia para fármacos antipalúdicos destinada a privar silenciosamente a la maquinaria de invasión del parásito de las membranas que necesita.
Cita: Guillén-Samander, A., Perepelkina, N., Horáčková, V. et al. A bridge-like lipid transfer protein is critical for generation of invasive stages in malaria parasites. Nat Commun 17, 3030 (2026). https://doi.org/10.1038/s41467-026-70887-1
Palabras clave: malaria, transferencia de lípidos, biogénesis de membranas, Plasmodium falciparum, complejo de membrana interna