Clear Sky Science · zh
使用比率极化分光的4polar3D单分子成像以测量致密肌动蛋白网络中的三维取向
一种窥见细胞内部隐含秩序的新方法
在每个活细胞内,细长的蛋白纤维构成支架,赋予细胞形状并帮助其运动。这些纤维密集且缠结,甚至先进的显微镜常常只能看到模糊的点阵。本研究引入了一种新成像方法,不仅能显示这些微小分子的位置,还能测量它们在三维空间中的取向,从而让科学家在完整细胞中绘制出这内部支架的隐含结构。
为什么方向信息很重要
许多细胞蛋白类似微小箭头:它们在空间中的方向影响相互作用、组装方式和力的产生。传统的超分辨率显微镜可以精确定位单个荧光分子,但通常忽略它们的倾斜或旋转。对于像细胞边缘的肌动蛋白纤维这样密集的结构,仅位置不足以了解纤维如何排列或如何对细胞膜施加推动与拉拽。能够同时捕获位置和取向、并覆盖大面积的技术,可以填补电子显微等高精度结构方法与可用于活细胞的快速光学方法之间的鸿沟。
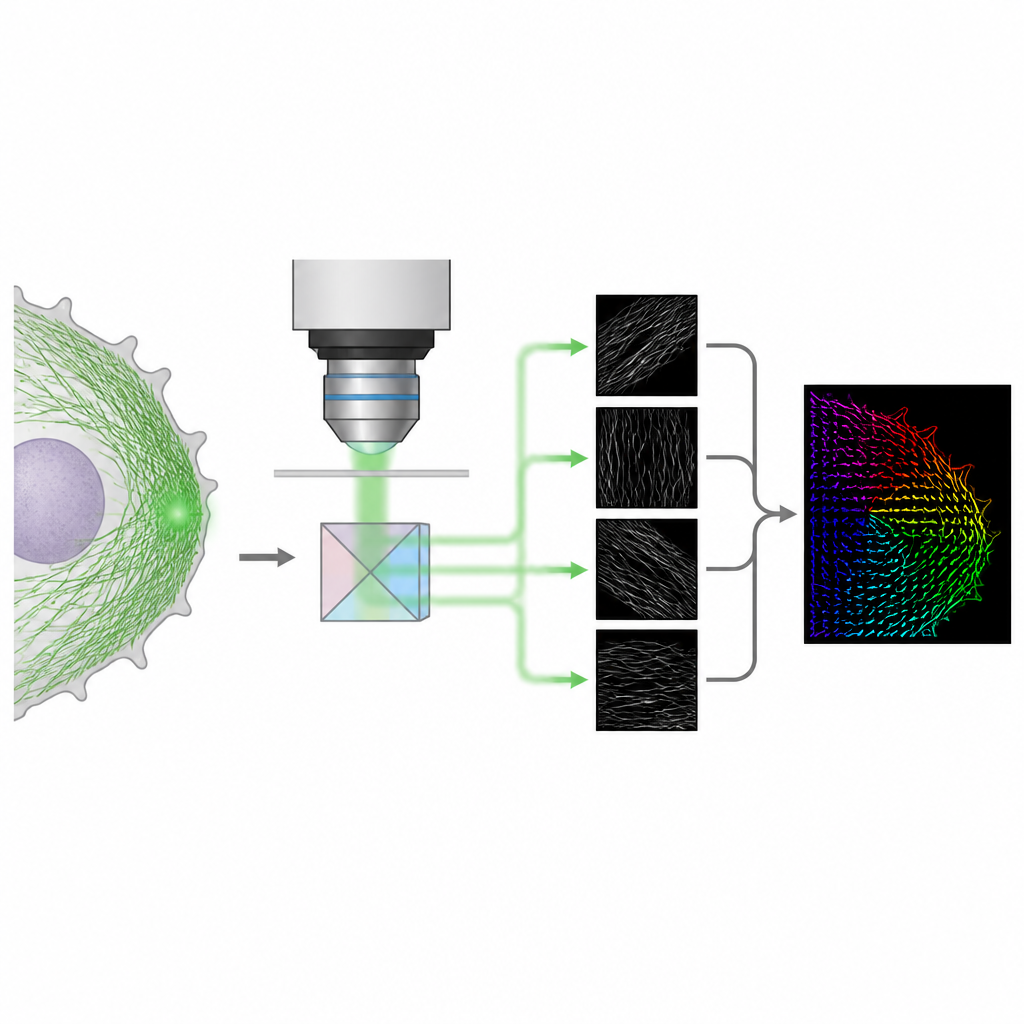
用于三维取向的更简洁光学技巧
作者提出了一种名为4polar3D的方法,能够测量单个荧光分子的取向及其摆动幅度,同时定位其在细胞中的位置。该系统并不通过复杂光学元件重塑每个分子的光场,而是将发射光拆分为四束光,每束通过不同偏振和数值孔径的滤光。通过比较同一分子在这四个通道中的亮度,方法提取出三项关键属性:分子在载玻片平面内的方向、其相对于平面的倾斜程度,以及其旋转的自由度。由于它仅依赖积分亮度而非详细的光斑模型拟合,数据分析快速且稳健,即便在许多分子同时发光时也能工作良好。
在模型膜上的方法验证
为验证4polar3D按预期工作,研究团队首先在带有荧光染料的简单脂质膜上进行测试,该染料倾向于沿脂肪酸链取向。在平整的支持膜上,方法测得染料分子的优选倾角和较大的摆动,这与早期更复杂方法的结果一致。当相同的膜包裹在微小的硅酸盐球体上时,测得的取向随曲率变化:靠近底部的分子更指向显微镜方向,而靠近侧面的分子则更与表面平行。这些测试表明4polar3D能准确恢复广泛范围的倾角,并区分平面内与离平面取向。
在类活细胞中揭示三维肌动蛋白结构
接着,研究者将方法应用于驱动细胞运动和黏附的致密肌动蛋白网络。在快速运动的黑色素瘤细胞中,细胞前缘的薄片称为网状伪足,内部密布肌动蛋白纤维。使用沿纤维结合的荧光标记,4polar3D记录了数百万次单分子事件,并重建出纤维方向的详细图谱。在最尖端附近,肌动蛋白网络显示出平面内分支纤维的混合,具有一对典型的优选方向,同时还存在一类倾出平面的纤维,取向更为多样。再往后,在过渡区和粗大的应力纤维中,纤维主要回到平面内并沿明确方向排列。
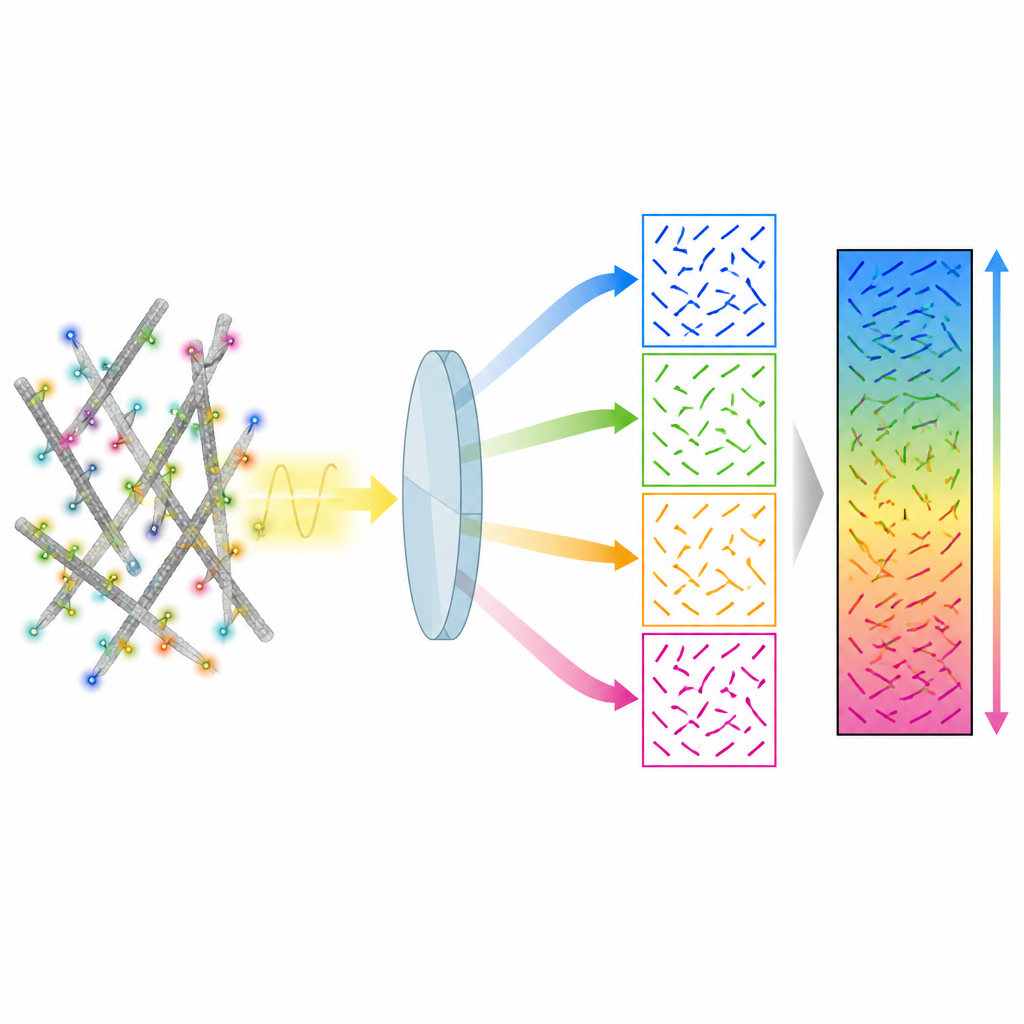
在微小黏附细胞器中发现三维结构
该方法还探测了胞型吸附结构——点蛋白小体(podosome),这些免疫细胞中的微小黏附器件比光学衍射极限还小。通过对数百个点蛋白小体的数据进行平均,作者发现了明确模式:在中心区域,许多肌动蛋白纤维倾出平面并可能向上延伸,而在边缘区域,平面内纤维形成向外放射的环,从每个核心向外指向。相邻点蛋白小体之间,这种有序的放射状图样大多消失。对荧光点表观焦平面的测量表明,核心中离平面的纤维位于玻片表面之上更高的位置,相较于周围的平面环层,支持了一个分层的三维肌动蛋白支架的图景。
这对细胞生物学意味着什么
总之,4polar3D提供了一种实用方法,可用相对简单的光学配置和快速计算在细胞的大面积范围内绘制分子三维指向。尽管在极端倾角下其精度不及某些更复杂的方法,但对大多数取向而言表现良好,且关键是能处理拥挤的、生物学相关的样本。通过揭示肌动蛋白纤维如何在网状伪足和点蛋白小体中穿出和平入细胞平面,这一方法为常规研究打开了通道,使人们能够将纳米尺度的纤维组织与细胞运动、力产生和信号传导联系起来。
引用: Senthil Kumar, C.S., Valades Cruz, C.A., Sison, M. et al. 4polar3D single molecule imaging of 3D orientation in dense actin networks using ratiometric polarization splitting. Nat Commun 17, 4246 (2026). https://doi.org/10.1038/s41467-026-70852-y
关键词: 单分子成像, 肌动蛋白细胞骨架, 偏振显微术, 超分辨率, 细胞力学