Clear Sky Science · pt
Imagem de molécula única 4polar3D da orientação 3D em redes densas de actina usando divisão de polarização ratiométrica
Uma nova maneira de ver a ordem oculta dentro das células
Dentro de cada célula viva, longos e finos filamentos proteicos formam um esqueleto que dá forma à célula e a ajuda a se mover. Essas fibras estão congestionadas e entrelaçadas, de modo que mesmo microscópios avançados frequentemente veem apenas um borrão de pontos. Este estudo apresenta um novo método de imagem que pode revelar não apenas onde essas pequenas moléculas estão, mas como elas estão orientadas em três dimensões, permitindo aos cientistas mapear a arquitetura oculta desse andaime interno em células intactas.
Por que observar a direção importa
Muitas proteínas nas células atuam como pequenas setas: sua direção no espaço afeta como interagem, se montam e geram forças. Microscópios tradicionais de super-resolução podem localizar a posição de moléculas fluorescentes individuais, mas geralmente ignoram como elas estão inclinadas ou rotacionadas. Para estruturas densamente empacotadas, como filamentos de actina na borda celular, saber apenas as posições não é suficiente para entender como as fibras estão dispostas ou como empurram e puxam a membrana celular. Uma técnica que capture posição e orientação ao mesmo tempo, em grandes áreas, pode preencher a lacuna entre métodos estruturais detalhados como a microscopia eletrônica e métodos ópticos mais rápidos usados em células vivas.
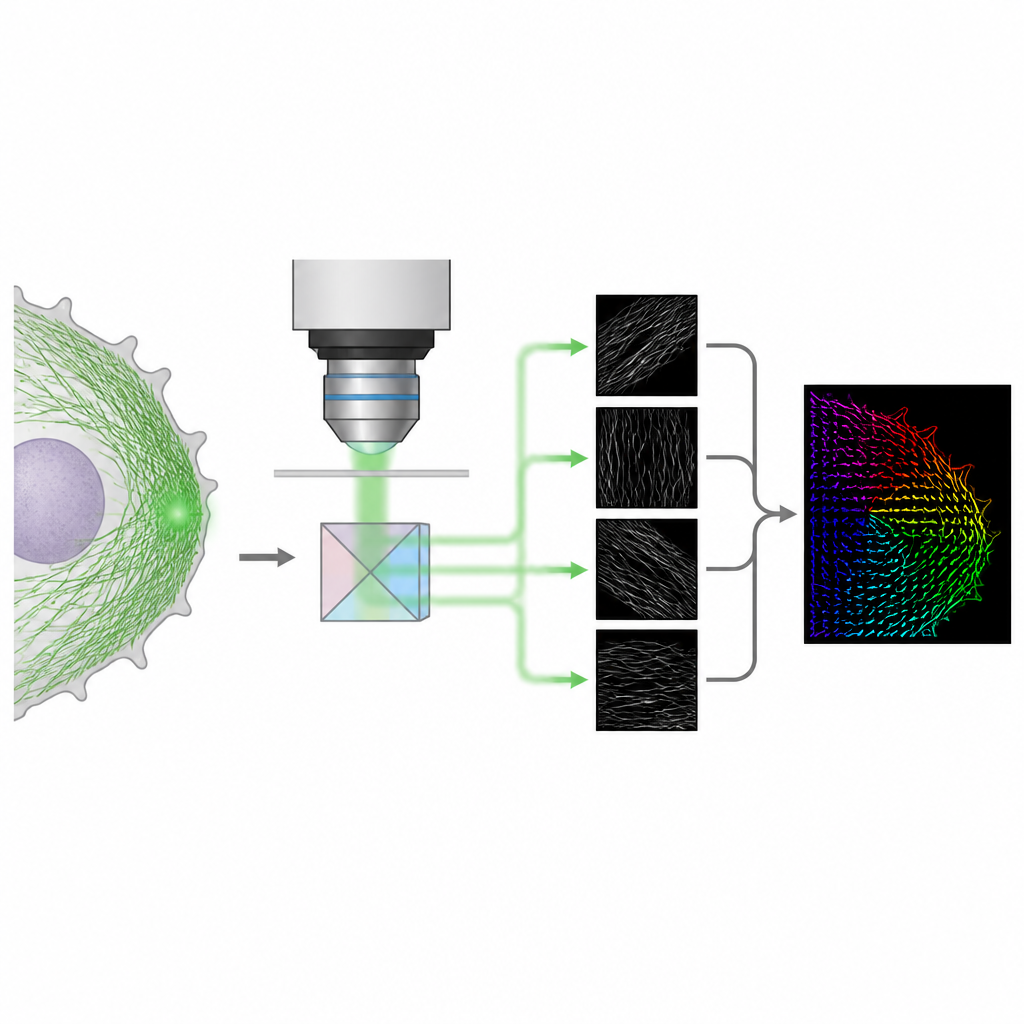
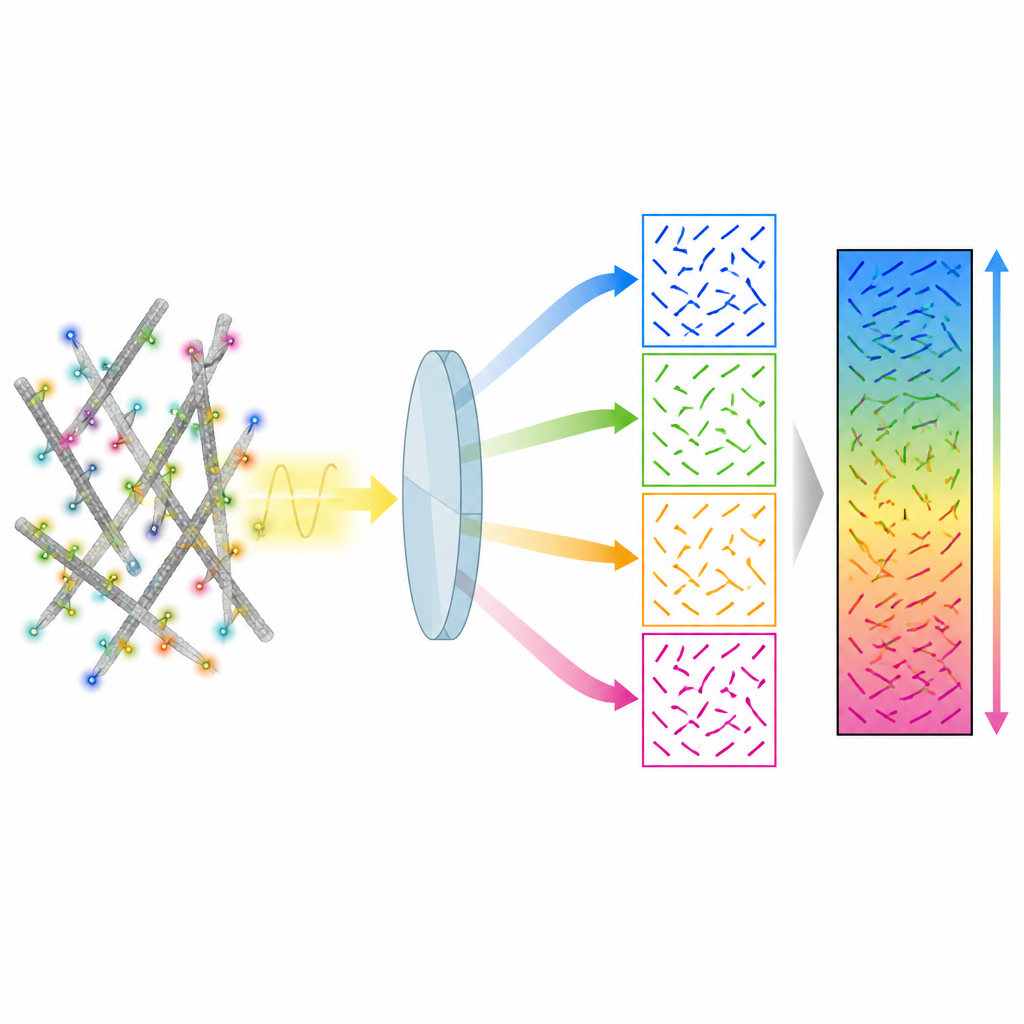
Um truque óptico mais simples para orientação 3D
Os autores apresentam um método chamado 4polar3D que mede como moléculas fluorescentes individuais estão orientadas e quanto elas oscilam, ao mesmo tempo em que as localiza na célula. Em vez de remodelar o padrão de luz emitido por cada molécula com óptica complexa, o sistema divide a luz emitida em quatro feixes, cada um filtrado por uma polarização e abertura numérica diferentes. Comparando quão brilhante a mesma molécula aparece nesses quatro canais, o método extrai três propriedades-chave: a direção da molécula no plano da lâmina do microscópio, quanto ela está inclinada fora desse plano e quão livremente pode girar. Por depender apenas do brilho integrado em vez do ajuste de padrões detalhados, a análise dos dados é rápida e robusta, mesmo quando muitas moléculas emitem luz ao mesmo tempo.
Testando o método em membranas-modelo
Para verificar que o 4polar3D funciona como esperado, a equipe primeiro o testou em membranas lipídicas simples rotuladas com um corante fluorescente que tende a se alinhar com as cadeias de ácidos graxos. Em membranas suportadas e planas, o método mediu uma inclinação preferencial das moléculas do corante e uma oscilação ampla, em acordo com abordagens anteriores mais complexas. Quando a mesma membrana foi enrolada em torno de pequenas esferas de sílica, as orientações medidas seguiram a curvatura da esfera: moléculas próximas ao fundo apontavam mais em direção ao microscópio, enquanto as próximas às laterais tornavam-se mais paralelas à superfície. Esses testes mostraram que o 4polar3D pode recuperar com precisão uma ampla gama de ângulos de inclinação e distinguir entre orientações no plano e fora do plano.
Revelando a arquitetura 3D da actina em células com características vivas
Os pesquisadores então investigaram as redes densas de actina que promovem o movimento e a adesão celular. Em células de melanoma de movimento rápido, a lâmina frontal fina da célula, chamada lamelipódio, está repleta de filamentos de actina. Usando uma etiqueta fluorescente que se liga ao longo desses filamentos, o 4polar3D registrou milhões de eventos de molécula única e reconstruiu um mapa detalhado das direções dos filamentos. Perto da borda extrema, a rede de actina mostrou uma mistura de filamentos ramificados no plano, com um par característico de direções preferenciais, e uma segunda população de filamentos inclinados fora do plano com orientações mais variadas. Mais atrás, na região de transição e em espessas fibras de tensão, os filamentos tornaram-se majoritariamente no plano e alinhados em direções claras.
Descobrindo estrutura 3D em minúsculos organelos de adesão
O método também investigou podossomos, pequenas estruturas de adesão em células imunes que são menores que o limite de difração da luz. Ao fazer a média dos dados de centenas de podossomos, os autores encontraram um padrão claro: no centro, muitos filamentos de actina estavam inclinados fora do plano e provavelmente se estendiam para cima, enquanto ao redor das bordas, filamentos no plano formavam um anel radial apontando para fora de cada núcleo. Entre podossomos vizinhos, esse padrão radial ordenado foi amplamente perdido. Medidas do foco aparente dos pontos fluorescentes sugeriram que os filamentos fora do plano no núcleo ficam mais altos acima da superfície de vidro do que o anel circundante no plano, apoiando um retrato de um andaime de actina em camadas e tridimensional.
O que isso significa para a biologia celular
Em resumo, o 4polar3D oferece uma forma prática de mapear como as moléculas apontam em três dimensões por grandes áreas de uma célula, usando uma montagem óptica relativamente simples e cálculos rápidos. Embora seja menos preciso em ângulos de inclinação extremos do que alguns métodos mais elaborados, ele funciona bem para a maioria das orientações e, crucialmente, consegue lidar com amostras congestionadas e biologicamente relevantes. Ao revelar como filamentos de actina entram e saem do plano celular em lamelipódios e podossomos, essa abordagem abre a porta para estudos rotineiros que conectam a organização das fibras em escala nanométrica ao movimento celular, geração de força e sinalização.
Citação: Senthil Kumar, C.S., Valades Cruz, C.A., Sison, M. et al. 4polar3D single molecule imaging of 3D orientation in dense actin networks using ratiometric polarization splitting. Nat Commun 17, 4246 (2026). https://doi.org/10.1038/s41467-026-70852-y
Palavras-chave: imagem de molécula única, citoesqueleto de actina, microscopia de polarização, super-resolução, mecânica celular