Clear Sky Science · nl
4polar3D single molecule imaging van 3D-orientatie in dichte actinenetwerken met behulp van ratiometrische polarisatie-splitsing
Een nieuwe manier om de verborgen orde binnen cellen te zien
In elke levende cel vormen lange, dunne eiwitfilamenten een geraamte dat de cel zijn vorm geeft en helpt bij beweging. Deze vezels zijn dicht opeengepakt en verward, zodat zelfs geavanceerde microscopen vaak slechts een wazige stipjeswolk tonen. Deze studie introduceert een nieuwe beeldvormingstechniek die niet alleen laat zien waar die kleine moleculen zich bevinden, maar ook hoe ze in drie dimensies georiënteerd zijn, waardoor onderzoekers de verborgen architectuur van dit interne geraamte in intacte cellen kunnen in kaart brengen.
Waarom naar richting kijken ertoe doet
Veel eiwitten in cellen werken als kleine pijltjes: hun richting in de ruimte beïnvloedt hoe ze interageren, assembleren en krachten genereren. Traditionele superresolutiemicroscopen kunnen de positie van individuele fluorescerende moleculen nauwkeurig bepalen, maar negeren meestal hoe ze gekanteld of geroteerd zijn. Voor dicht opeengepakte structuren, zoals actinefilamenten aan de rand van de cel, is alleen positie weten niet genoeg om te begrijpen hoe vezels zijn gerangschikt of hoe ze op het celmembraan duwen en trekken. Een techniek die zowel positie als oriëntatie tegelijk vastlegt, over grote gebieden, kan de kloof dichten tussen gedetailleerde structurele methoden zoals elektronenmicroscopie en snellere optische methoden die in levende cellen worden gebruikt.
Een eenvoudiger optische truc voor 3D-orientatie
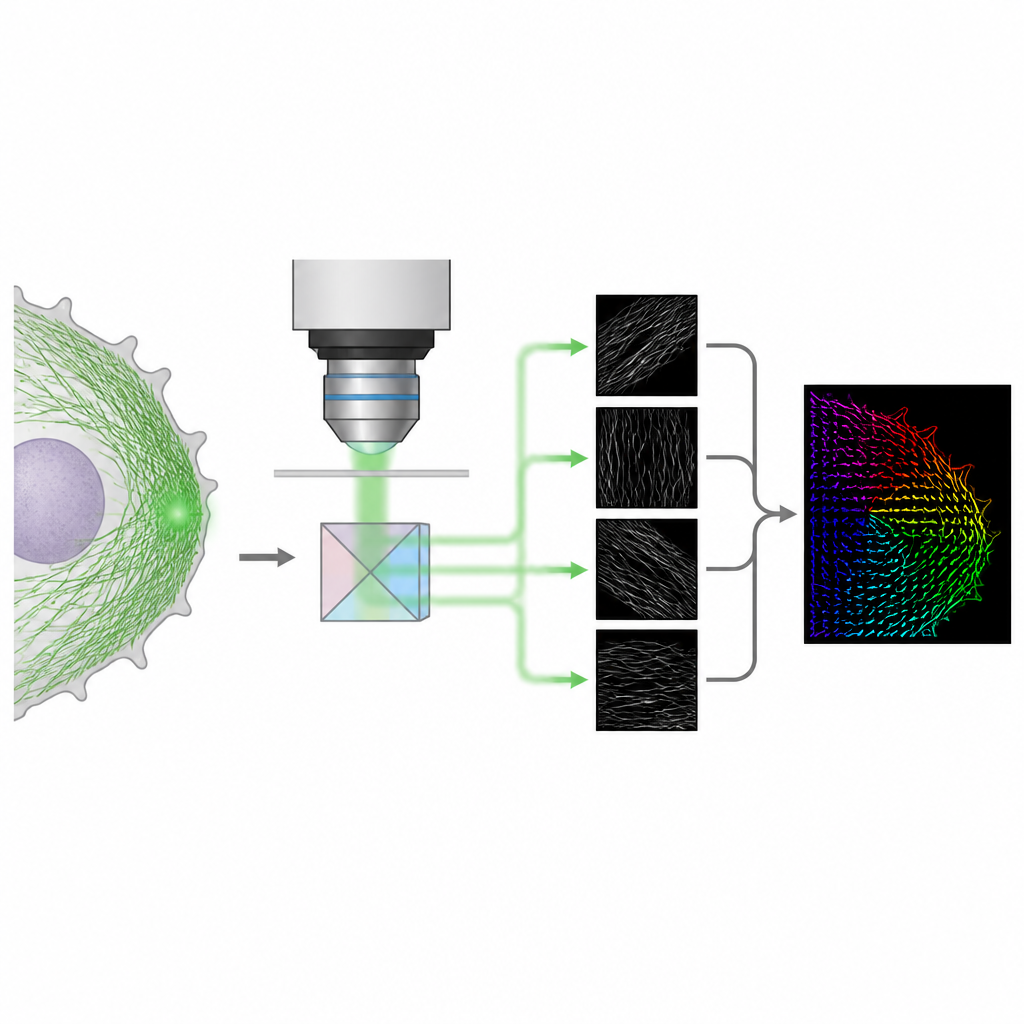
De auteurs presenteren een methode genaamd 4polar3D die meet hoe individuele fluorescerende moleculen georiënteerd zijn en hoeveel ze wiebelen, terwijl ze ook gelokaliseerd worden in de cel. In plaats van het lichtpatroon van elk molecuul met complexe optiek te herschikken, splitst het systeem het uitgezonden licht in vier bundels, elk gefilterd door een andere polarisatie en numerieke apertuur. Door te vergelijken hoe helder hetzelfde molecuul in deze vier kanalen verschijnt, haalt de methode drie sleutel eigenschappen naar voren: de richting van het molecuul in het vlak van de microscoopglaasje, hoeveel het uit dat vlak is gekanteld, en hoe vrij het kan roteren. Omdat het alleen berust op geïntegreerde helderheid in plaats van op gedetailleerde patroonfitting, is de data-analyse snel en robuust, zelfs wanneer veel moleculen tegelijk licht uitzenden.
De methode testen op modelmembranen
Om te controleren of 4polar3D werkt zoals verwacht, testte het team het eerst op eenvoudige lipidemembranen die zijn gemarkeerd met een fluorescerende kleurstof die de neiging heeft uit te lijnen met de vetzuurketens. Op vlakke ondersteunde membranen mat de methode een voorkeurstoestand van kanteling van de kleurstofmoleculen en een brede wiebeling, in overeenstemming met eerdere, complexere benaderingen. Toen hetzelfde membraan rond kleine silicabolletjes werd gewikkeld, volgden de gemeten orientaties de kromming van de bol: moleculen nabij de onderzijde wezen meer naar de microscoop, terwijl die nabij de zijkanten meer parallel aan het oppervlak werden. Deze tests toonden aan dat 4polar3D nauwkeurig een breed scala aan kantelhoeken kan terugvinden en onderscheid kan maken tussen in-vlak en uit-vlak orientaties.
3D-actinearchitectuur blootleggen in leven-achtige cellen
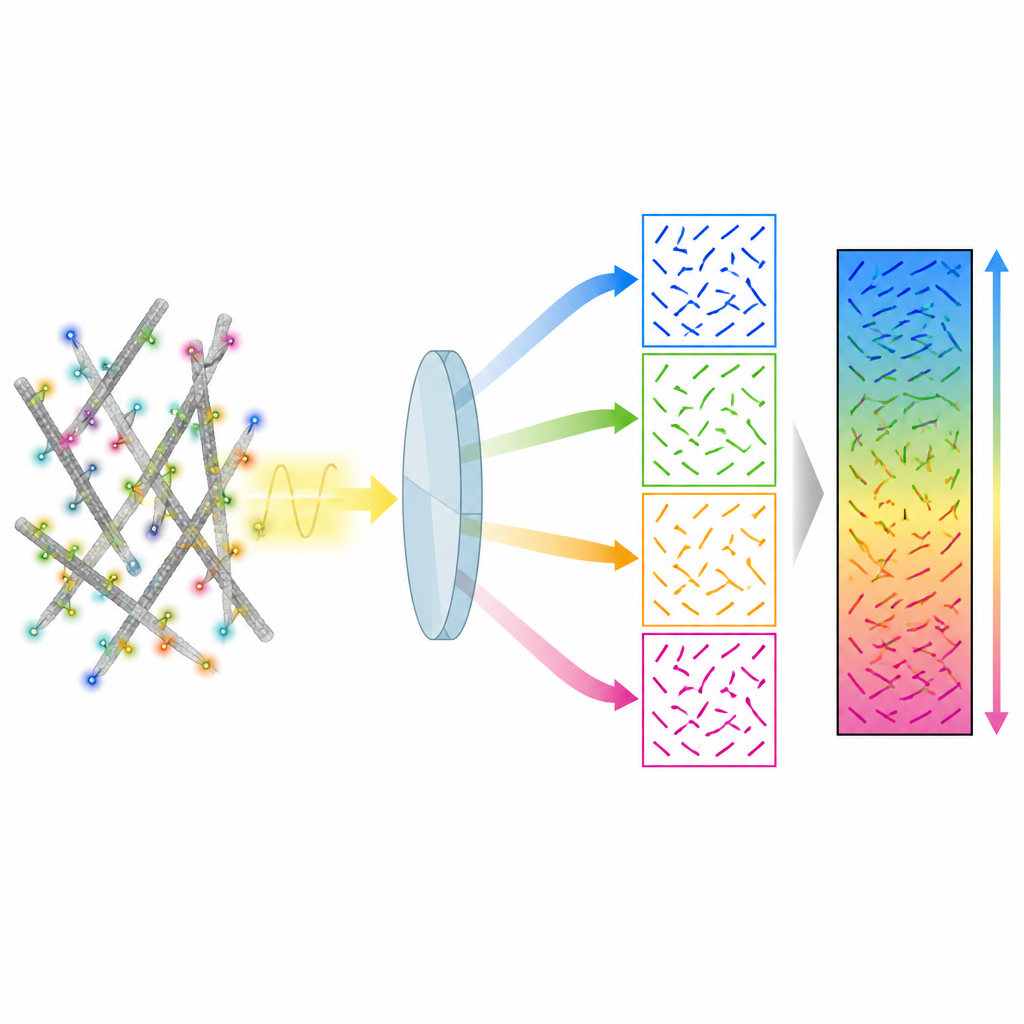
De onderzoekers richtten zich vervolgens op de dichte actinenetwerken die celbeweging en adhesie aandrijven. In snel bewegende melanomacellen is het dunne blad aan de voorkant van de cel, de lamellipodium, dicht gevuld met actinefilamenten. Met een fluorescerend label dat langs deze filamenten bindt, registreerde 4polar3D miljoenen gebeurtenissen van enkele moleculen en reconstrueerde een gedetailleerde kaart van filamentrichtingen. Dicht bij de rand toonde het actinenetwerk een mix van in-vlak vertakte filamenten, met een kenmerkende paarvoorkeur in richtingen, en een tweede populatie filamenten die uit het vlak gekanteld waren met meer gevarieerde orientaties. Verder naar achteren, in de overgangszone en in dikke stressvezels, werden filamenten grotendeels in het vlak en uitgelijnd langs heldere richtingen.
3D-structuur onthullen in kleine adhesieorganellen
De methode onderzocht ook podosomen, kleine adhesiestructuren in immuuncellen die kleiner zijn dan de diffractielimiet van licht. Door data van honderden podosomen te middelen, vonden de auteurs een duidelijk patroon: in het centrum waren veel actinefilamenten uit het vlak gekanteld en waarschijnlijk naar boven gericht, terwijl rond de randen in-vlak filamenten een radiale ring vormden die vanaf elk kernpunt naar buiten wees. Tussen aangrenzende podosomen ging dit geordende radiale patroon grotendeels verloren. Metingen van de schijnbare focus van de fluorescerende punten suggereerden dat uit-vlak filamenten in de kern hoger boven het glasoppervlak liggen dan de omliggende in-vlak ring, wat een beeld ondersteunt van een gelaagd, driedimensionaal actinegeraamte.
Wat dit betekent voor celbiologie
Samengevat biedt 4polar3D een praktische manier om in kaart te brengen hoe moleculen in drie dimensies gericht zijn over grote delen van een cel, met een relatief eenvoudige optische opstelling en snelle berekeningen. Hoewel het bij extreme kantelhoeken minder precies is dan sommige meer ingewikkelde methoden, werkt het goed voor de meeste orientaties en kan het, cruciaal, omgaan met drukbezette, biologisch relevante monsters. Door te onthullen hoe actinefilamenten in lamellipodia en podosomen in en uit het celvlak weven, maakt deze benadering routinematige studies mogelijk die de organisatie van vezels op nanoschaal verbinden met celbeweging, krachtgeneratie en signaaloverdracht.
Bronvermelding: Senthil Kumar, C.S., Valades Cruz, C.A., Sison, M. et al. 4polar3D single molecule imaging of 3D orientation in dense actin networks using ratiometric polarization splitting. Nat Commun 17, 4246 (2026). https://doi.org/10.1038/s41467-026-70852-y
Trefwoorden: single molecule imaging, actine cytoskelet, polarisatiemicroscopie, superresolutie, celmechanica