Clear Sky Science · de
4polar3D Einzelmolekül-Bildgebung der 3D-Orientierung in dichten Aktin-Netzwerken mittels ratiometrischer Polarisationsaufspaltung
Eine neue Möglichkeit, die verborgene Ordnung in Zellen zu sehen
In jeder lebenden Zelle bilden lange, dünne Proteinfilamente ein Gerüst, das der Zelle Form verleiht und ihre Bewegung unterstützt. Diese Fasern sind dicht gepackt und verheddert, sodass selbst fortgeschrittene Mikroskope oft nur einen verschwommenen Punktteppich zeigen. Die vorliegende Studie stellt eine neue Bildgebungsmethode vor, die nicht nur zeigt, wo diese winzigen Moleküle sind, sondern auch, wie sie im dreidimensionalen Raum ausgerichtet sind. So können Wissenschaftler die verborgene Architektur dieses inneren Gerüsts in intakten Zellen kartieren.
Warum die Blickrichtung zählt
Viele Proteine in Zellen verhalten sich wie winzige Pfeile: ihre Ausrichtung im Raum beeinflusst, wie sie miteinander wechselwirken, sich zusammenlagern und Kräfte erzeugen. Konventionelle Superauflösungsmikroskope können die Position einzelner fluoreszierender Moleküle sehr genau bestimmen, vernachlässigen aber meist deren Neigung oder Rotation. Bei dicht gepackten Strukturen wie Aktinfilamenten am Zellrand reichen Positionen allein nicht aus, um zu verstehen, wie Fasern angeordnet sind oder wie sie auf die Zellmembran drücken und ziehen. Eine Technik, die gleichzeitig Position und Orientierung über große Bereiche erfasst, kann die Lücke zwischen detailreichen Strukturmethoden wie der Elektronenmikroskopie und schnelleren optischen Verfahren für lebende Zellen schließen.
Ein einfacherer optischer Trick für 3D-Orientierung
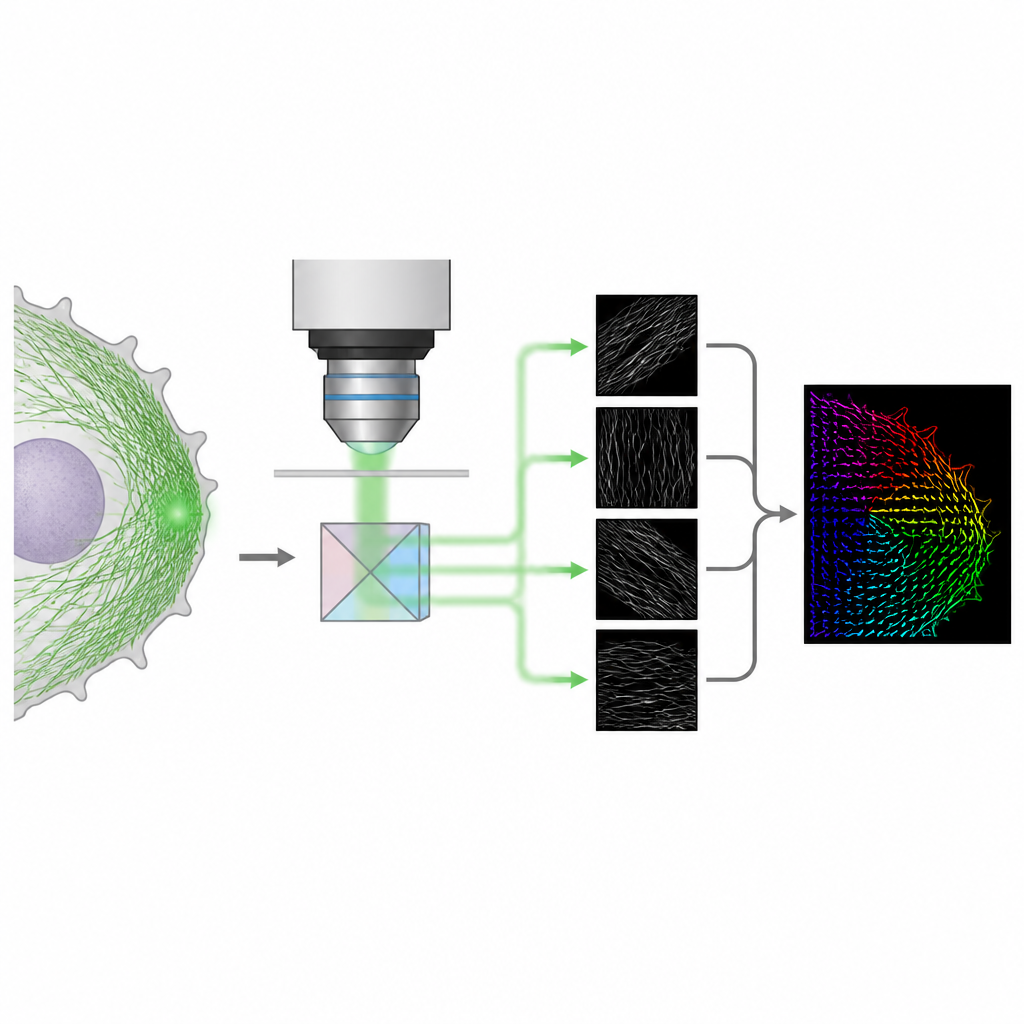
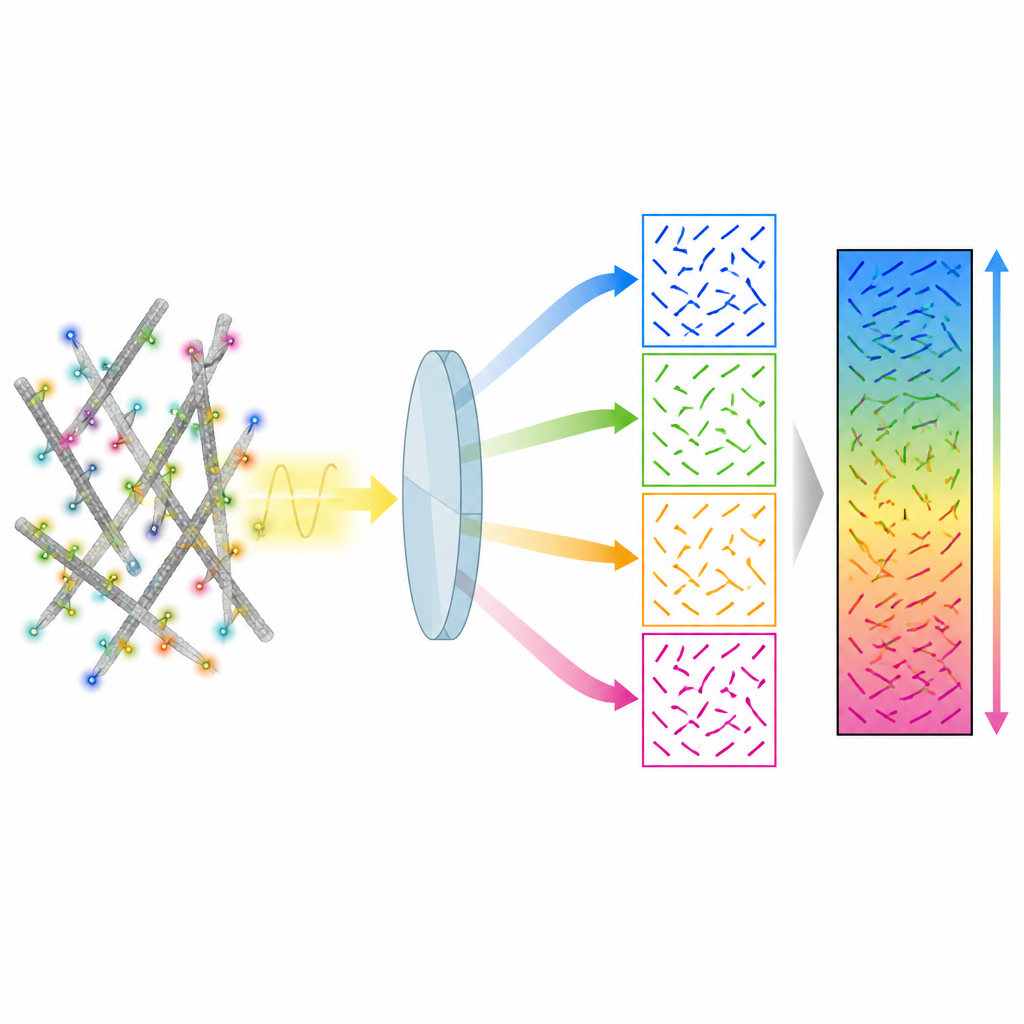
Die Autor:innen stellen eine Methode namens 4polar3D vor, die misst, wie einzelne fluoreszierende Moleküle ausgerichtet sind und wie stark sie wackeln, und sie gleichzeitig im Zellkontext lokalisiert. Anstatt das Lichtmuster jedes Moleküls mit komplexer Optik umzuformen, teilt das System das emittierte Licht in vier Strahlen auf, die jeweils durch eine andere Polarisation und numerische Apertur gefiltert werden. Durch den Vergleich der Helligkeit desselben Moleküls in diesen vier Kanälen extrahiert die Methode drei zentrale Eigenschaften: die Richtung des Moleküls in der Ebene des Objektträgers, wie stark es aus dieser Ebene geneigt ist, und wie frei es rotieren kann. Da die Analyse nur auf integrierter Helligkeit beruht und nicht auf aufwändigem Musterabgleich, ist die Auswertung schnell und robust, selbst wenn viele Moleküle gleichzeitig emittieren.
Test der Methode an Modellmembranen
Um zu überprüfen, dass 4polar3D wie erwartet funktioniert, testete das Team die Methode zunächst an einfachen Lipidmembranen, die mit einem fluoreszierenden Farbstoff markiert waren, der sich bevorzugt an die Fettsäureketten anlagert. Auf flachen, aufgestützten Membranen maß die Methode eine bevorzugte Neigung der Farbstoffmoleküle und ein breites Wackeln, im Einklang mit früheren, komplexeren Ansätzen. Wurde dieselbe Membran um winzige Silikaperlen gewickelt, folgten die gemessenen Orientierungen der Krümmung der Kugel: Moleküle nahe dem Boden zeigten eine stärkere Ausrichtung in Richtung des Mikroskops, während jene an den Seiten eher parallel zur Oberfläche lagen. Diese Tests zeigten, dass 4polar3D ein breites Spektrum von Neigungswinkeln akkurat rekonstruieren und zwischen in-Ebene- und außerhalb-der-Ebene-Orientierungen unterscheiden kann.
3D-Aktinarchitektur in lebensechten Zellen aufdecken
Anschließend richteten die Forschenden den Blick auf die dichten Aktin-Netzwerke, die Zellbewegung und -anhaftung antreiben. In schnell bewegenden Melanomzellen ist das dünne Blatt an der Zellvorderseite, das Lamellipodium, mit Aktinfilamenten dicht gepackt. Mit einem fluoreszenten Marker, der entlang dieser Filamente bindet, zeichnete 4polar3D Millionen einzelner Molekülereignisse auf und rekonstruierte eine detaillierte Karte der Filamentrichtungen. Nahe der äußersten Kante zeigte das Aktinnetz eine Mischung aus in-Ebene-verzweigten Filamenten, mit einem charakteristischen Paar bevorzugter Richtungen, sowie eine zweite Population von Filamenten, die aus der Ebene geneigt und in ihrer Orientierung variabler waren. Weiter hinten, in der Übergangszone und in dicken Stressfasern, lagen die Filamente überwiegend in der Ebene und waren entlang klarer Richtungen ausgerichtet.
3D-Struktur in winzigen Adhäsionsorganellen enthüllen
Die Methode untersuchte auch Podosome, winzige Adhäsionsstrukturen in Immunzellen, die kleiner sind als das Beugungslimit des Lichts. Durch das Mittelwertbilden von Daten aus Hunderten von Podosomen fanden die Autor:innen ein klares Muster: im Zentrum waren viele Aktinfilamente aus der Ebene geneigt und vermutlich nach oben gerichtet, während am Rand in-Ebene-Filamente einen radialen Ring bildeten, der vom Kern nach außen zeigte. Zwischen benachbarten Podosomen ging dieses geordnete radiale Muster größtenteils verloren. Messungen des scheinbaren Fokus der fluoreszierenden Punkte deuteten darauf hin, dass die außerhalb-der-Ebene-Filamente im Kern höher über der Glasoberfläche liegen als der umgebende in-Ebene-Ring, was ein Bild eines geschichteten, dreidimensionalen Aktingerüsts stützt.
Was das für die Zellbiologie bedeutet
Zusammenfassend bietet 4polar3D eine praktikable Möglichkeit, die dreidimensionale Ausrichtung von Molekülen über große Bereiche einer Zelle zu kartieren, mit einer relativ einfachen optischen Anordnung und schnellen Berechnungen. Zwar ist die Methode bei extremen Neigungswinkeln weniger genau als einige aufwändigere Verfahren, sie funktioniert jedoch gut für die meisten Orientierungen und kann vor allem dichte, biologisch relevante Proben bewältigen. Indem sie zeigt, wie Aktinfilamente im Lamellipodium und in Podosomen in und aus der Zell-Ebene weben, eröffnet dieser Ansatz routinemäßige Studien, die die nanoskalige Faserorganisation mit Zellbewegung, Kraftentstehung und Signalübertragung verknüpfen.
Zitation: Senthil Kumar, C.S., Valades Cruz, C.A., Sison, M. et al. 4polar3D single molecule imaging of 3D orientation in dense actin networks using ratiometric polarization splitting. Nat Commun 17, 4246 (2026). https://doi.org/10.1038/s41467-026-70852-y
Schlüsselwörter: Einzelmolekül-Bildgebung, Aktin-Zytoskelett, Polarisationsmikroskopie, Superauflösung, Zellmechanik