Clear Sky Science · ru
4polar3D-микроскопия одиночных молекул для измерения 3D-ориентации в густых сетях актина с использованием ритметрического расщепления поляризации
Новый способ увидеть скрытый порядок внутри клеток
Внутри каждой живой клетки длинные тонкие белковые филаменты образуют каркас, который задаёт форму клетки и помогает ей двигаться. Эти волокна плотно упакованы и переплетены, поэтому даже продвинутые микроскопы часто видят лишь размытые точки. В работе представлен новый метод визуализации, который позволяет увидеть не только положение этих крошечных молекул, но и их ориентацию в трёх измерениях, давая учёным возможность картировать скрытую архитектуру внутреннего каркаса в целых клетках.
Почему важно знать направление
Многие белки в клетках ведут себя как крошечные стрелки: их направление в пространстве влияет на взаимодействия, сборку и генерацию сил. Традиционные методы суперразрешения могут точно определять положение одиночных флуоресцентных молекул, но обычно игнорируют их наклон или вращение. Для плотных структур, таких как актиновые филаменты на краю клетки, одних только позиций недостаточно, чтобы понять, как волокна расположены или как они толкают и тянут мембрану. Метод, который фиксирует одновременно положение и ориентацию на больших площадях, может заполнить разрыв между детальными структурными подходами, как электронная микроскопия, и более быстрыми оптическими методами, применимыми в живых клетках.
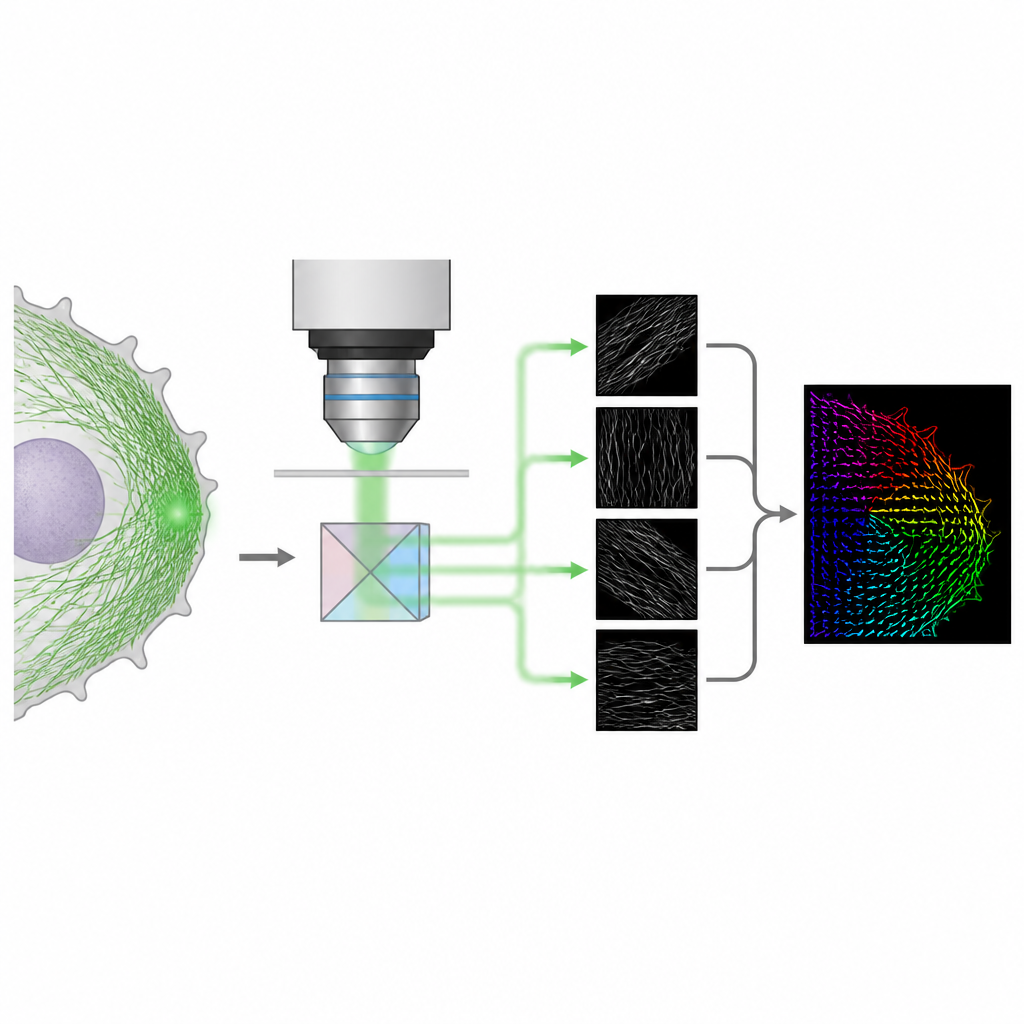
Проще оптический приём для 3D‑ориентации
Авторы предлагают метод под названием 4polar3D, который измеряет, как ориентированы одиночные флуоресцентные молекулы и насколько они «дрожат», одновременно определяя их положение в клетке. Вместо того чтобы формировать сложные световые картины от каждой молекулы с помощью запутанной оптики, система расщепляет испускаемый свет на четыре луча, каждый из которых фильтруется по разной поляризации и числовой апертуре. Сравнивая яркость одной и той же молекулы в этих четырёх каналах, метод извлекает три ключевых параметра: направление молекулы в плоскости предметного стекла, её наклон относительно этой плоскости и степень её свободного вращения. Поскольку анализ опирается на интегрированную яркость, а не на точную подгонку сложных шаблонов, обработка данных быстрая и устойчивая, даже когда многие молекулы светятся одновременно.
Тестирование метода на модельных мембранах
Чтобы проверить работоспособность 4polar3D, команда сначала испытала его на простых липидных мембранах, меченных флуоресцентным красителем, который склонен выстраиваться вдоль жирнокислотных цепей. На плоских опорных мембранах метод зафиксировал предпочтительный наклон молекул красителя и широкий разброс «дрожания», что согласуется с более ранними, более сложными подходами. Когда ту же мембрану обернули вокруг крошечных кремниевых шариков, измеренные ориентации следовали кривизне сферы: молекулы возле нижней части указывали больше в сторону микроскопа, тогда как на боках они становились более параллельны поверхности. Эти тесты показали, что 4polar3D может точно восстанавливать широкий диапазон углов наклона и различать ориентации в плоскости и вне её.
Раскрытие 3D‑архитектуры актина в клетках, близких к живым
Далее исследователи обратились к плотным актиновым сетям, которые обеспечивают движение клетки и прикрепление. В быстро движущихся меланоцитах тонкий лист на переднем крае клетки, называемый ламелиподием, заполнен актиновыми филаментами. С помощью флуоресцентной метки, связывающейся вдоль этих филаментов, 4polar3D записал миллионы событий одиночных молекул и восстановил детальную карту направлений филаментов. Ближе к самому краю сеть актина показывала смесь плоско расположенных ветвящихся филаментов с характерной парой предпочтительных направлений и вторую популяцию филаментов, наклонённых вне плоскости с более разнообразными ориентациями. Дальше, в переходной зоне и в толстых стрессовых волокнах, филаменты в основном располагались в плоскости и выстраивались вдоль чётких направлений.
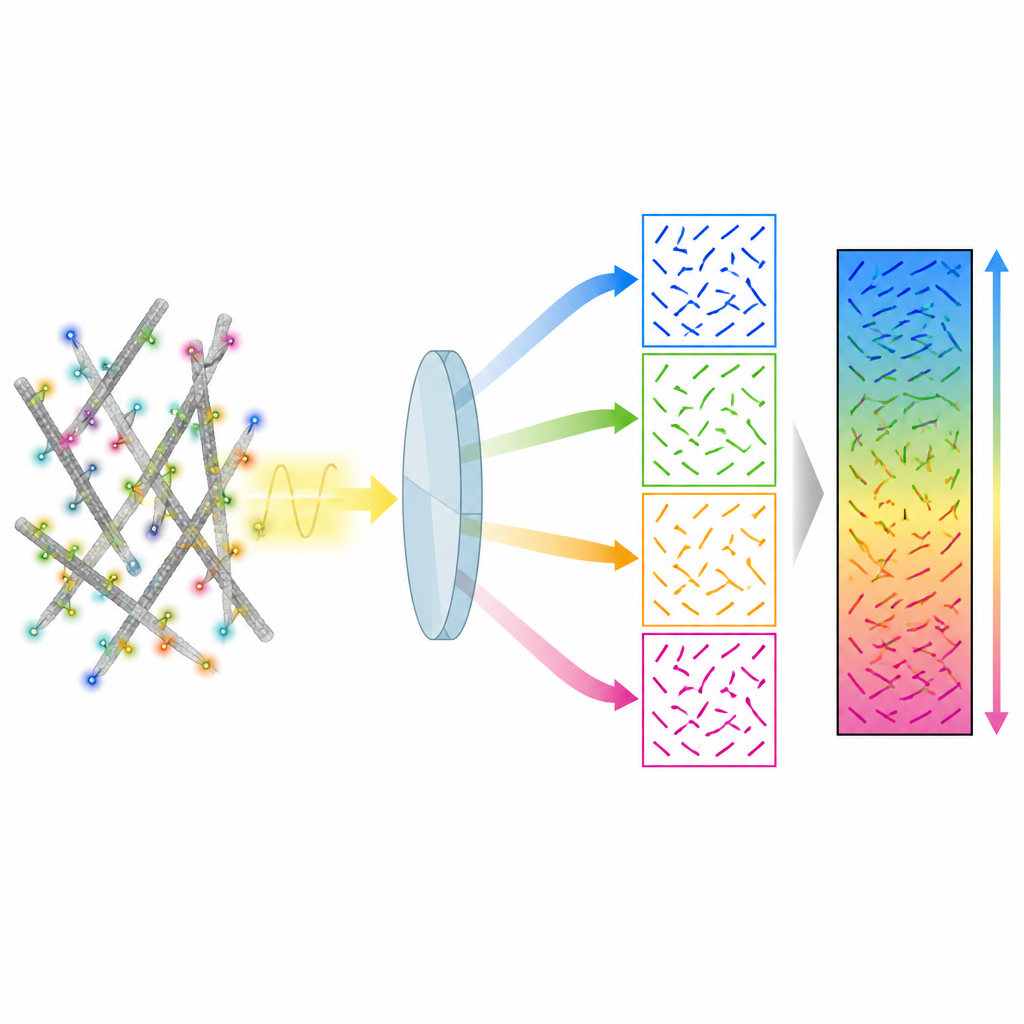
Выявление 3D‑структуры в крошечных органеллах прикрепления
Метод также исследовал подоcомы — крошечные структуры прикрепления в иммунных клетках, размеры которых меньше дифракционного предела света. Усредняя данные по сотням подосом, авторы обнаружили чёткую схему: в центре многие актиновые филаменты были наклонены вне плоскости и, вероятно, направлены вверх, тогда как по краям плоские филаменты формировали радиальное кольцо, направленное от каждого ядра. Между соседними подосомами этот упорядоченный радиальный рисунок в основном терялся. Измерения кажущейся фокусировки флуоресцентных пятен указывали, что внеплоскостные филаменты в ядре расположены выше над стеклом, чем окружающее плоское кольцо, что поддерживает представление о многослойном трёхмерном актиновом каркасе.
Что это значит для клеточной биологии
В итоге 4polar3D предлагает практичный способ картировать, куда направлены молекулы в трёх измерениях по большим участкам клетки, используя относительно простую оптическую схему и быстрые вычисления. Хотя метод уступает в точности при крайних углах наклона некоторым более сложным подходам, он хорошо работает для большинства ориентаций и, что важно, справляется с плотными образцами биологического значения. Раскрывая, как актиновые филаменты пронизывают плоскость клетки в ламелиподиях и подосомах, этот подход открывает путь к рутинным исследованиям, связывающим наномасштабную организацию волокон с движением клетки, генерацией сил и сигнализацией.
Цитирование: Senthil Kumar, C.S., Valades Cruz, C.A., Sison, M. et al. 4polar3D single molecule imaging of 3D orientation in dense actin networks using ratiometric polarization splitting. Nat Commun 17, 4246 (2026). https://doi.org/10.1038/s41467-026-70852-y
Ключевые слова: визуализация одиночных молекул, актиновый цитоскелет, поляризационная микроскопия, суперразрешение, механика клетки