Clear Sky Science · es
Imágenes 4polar3D de moléculas individuales para orientación 3D en redes densas de actina mediante división polarimétrica ratiométrica
Una nueva forma de ver el orden oculto dentro de las células
Dentro de cada célula viva, largos y delgados filamentos proteicos forman un andamiaje que da forma a la célula y le ayuda a moverse. Estas fibras están apiñadas y enredadas, por lo que incluso los microscopios avanzados a menudo solo muestran una mancha de puntos. Este estudio presenta un nuevo método de imagen que puede revelar no solo dónde están esas diminutas moléculas, sino cómo se orientan en tres dimensiones, permitiendo a los científicos mapear la arquitectura oculta de este andamiaje interno en células intactas.
Por qué importa observar la dirección
Muchas proteínas en las células actúan como pequeñas flechas: su dirección en el espacio afecta cómo interactúan, se ensamblan y generan fuerzas. Los microscopios de superresolución tradicionales pueden localizar la posición de moléculas fluorescentes individuales pero normalmente ignoran cómo están inclinadas o rotadas. Para estructuras densamente empaquetadas, como los filamentos de actina en el borde celular, conocer solo las posiciones no es suficiente para entender cómo se organizan las fibras o cómo empujan y tiran de la membrana celular. Una técnica que pueda capturar posición y orientación a la vez, sobre áreas extensas, puede salvar la distancia entre métodos estructurales detallados como la microscopía electrónica y métodos ópticos más rápidos usados en células vivas.
Un truco óptico más simple para la orientación 3D
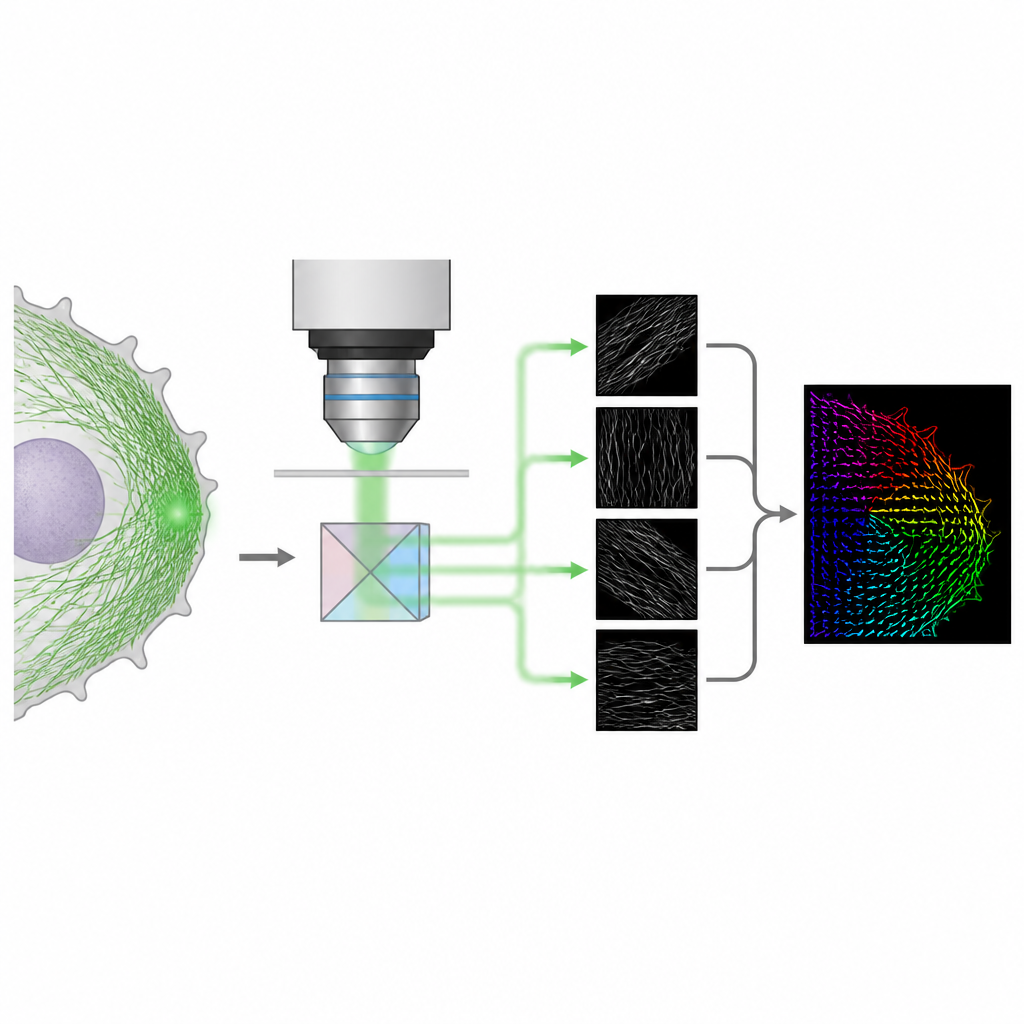
Los autores presentan un método llamado 4polar3D que mide cómo están orientadas las moléculas fluorescentes individuales y cuánto titubean, mientras también las localiza en la célula. En lugar de remodelar el patrón de luz de cada molécula con óptica compleja, el sistema divide la luz emitida en cuatro haces, cada uno filtrado por una polarización y una apertura numérica diferente. Al comparar cuán brillante aparece la misma molécula en estos cuatro canales, el método extrae tres propiedades clave: la dirección de la molécula en el plano del portaobjetos, cuánto se inclina fuera de ese plano y con qué libertad puede rotar. Dado que se basa solo en la intensidad integrada en lugar de ajustar patrones detallados, el análisis de datos es rápido y robusto, incluso cuando muchas moléculas emiten luz al mismo tiempo.
Comprobación del método en membranas modelo
Para verificar que 4polar3D funciona como se espera, el equipo lo probó primero en membranas lipídicas simples etiquetadas con un tinte fluorescente que tiende a alinearse con las cadenas de ácidos grasos. En membranas soportadas y planas, el método midió una inclinación preferente de las moléculas del tinte y un amplio titubeo, en acuerdo con enfoques anteriores más complejos. Cuando la misma membrana se envolvió alrededor de diminutas esferas de sílice, las orientaciones medidas siguieron la curvatura de la esfera: las moléculas cerca de la parte inferior apuntaban más hacia el microscopio, mientras que las situadas en los laterales se volvieron más paralelas a la superficie. Estas pruebas mostraron que 4polar3D puede recuperar con precisión una amplia gama de ángulos de inclinación y distinguir entre orientaciones en el plano y fuera del plano.
Revelando la arquitectura 3D de la actina en células de aspecto vivo
Los investigadores luego se centraron en las densas redes de actina que impulsan el movimiento celular y la adhesión. En células de melanoma de movimiento rápido, la delgada lámina en la parte frontal de la célula, llamada lamelipodio, está repleta de filamentos de actina. Usando una etiqueta fluorescente que se une a lo largo de estos filamentos, 4polar3D registró millones de eventos de moléculas individuales y reconstruyó un mapa detallado de las direcciones de los filamentos. Cerca del borde muy exterior, la red de actina mostró una mezcla de filamentos ramificados en el plano, con un par característico de direcciones preferidas, y una segunda población de filamentos inclinados fuera del plano con orientaciones más variadas. Más atrás, en la región de transición y en fibras de estrés gruesas, los filamentos se volvieron mayoritariamente en el plano y alineados en direcciones claras.
Descubriendo estructura 3D en pequeños organelos de adhesión
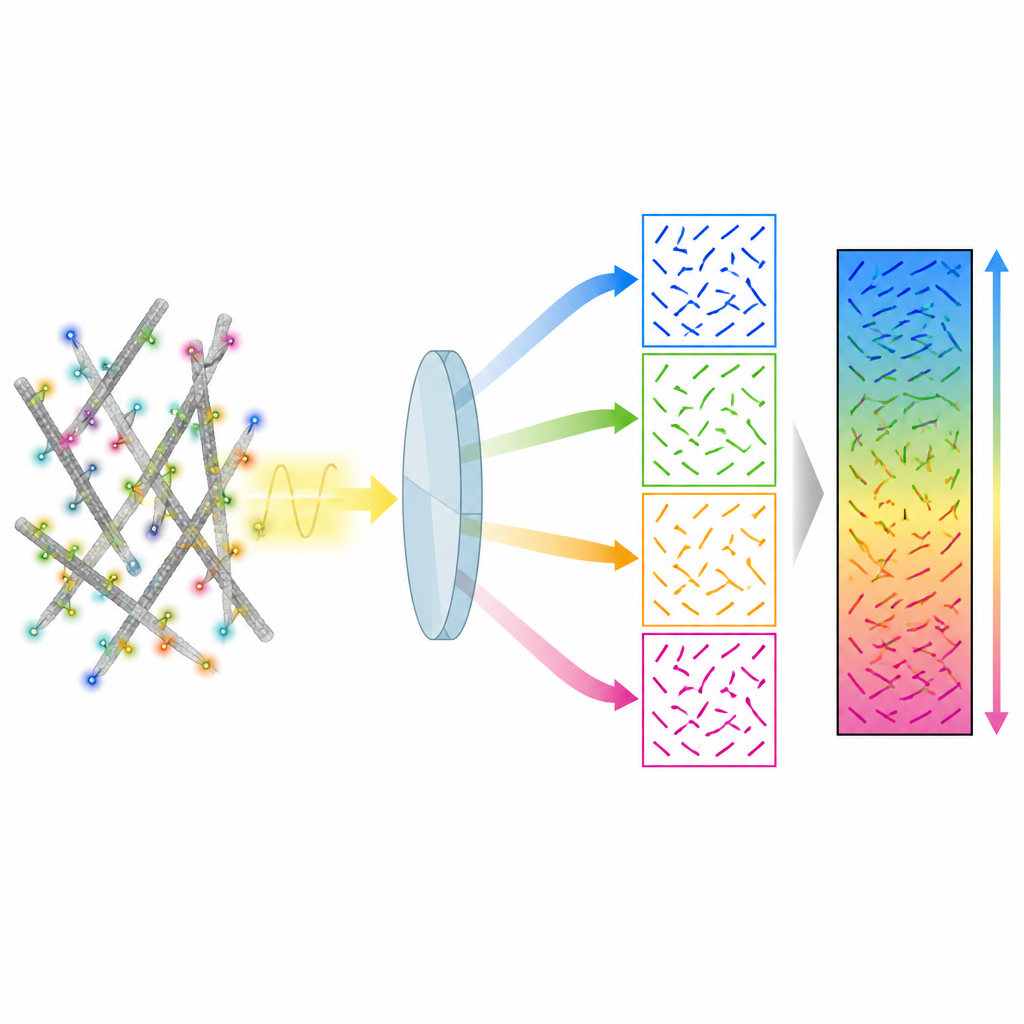
El método también investigó podosomas, pequeños organelos de adhesión en células inmunitarias que son más pequeños que el límite de difracción de la luz. Al promediar datos de cientos de podosomas, los autores encontraron un patrón claro: en el centro, muchos filamentos de actina estaban inclinados fuera del plano y probablemente se extendían hacia arriba, mientras que en los bordes, filamentos en el plano formaban un anillo radial que apuntaba hacia afuera desde cada núcleo. Entre podosomas vecinos, este patrón radial ordenado se perdía en gran medida. Las mediciones del foco aparente de los puntos fluorescentes sugirieron que los filamentos fuera del plano en el núcleo se sitúan más altos sobre la superficie de vidrio que el anillo en el plano circundante, apoyando la imagen de un andamiaje de actina estratificado y tridimensional.
Qué significa esto para la biología celular
En resumen, 4polar3D ofrece una manera práctica de cartografiar cómo se orientan las moléculas en tres dimensiones a lo largo de áreas extensas de una célula, usando un montaje óptico relativamente simple y cálculos rápidos. Aunque es menos preciso en ángulos de inclinación extremos que algunos métodos más elaborados, funciona bien para la mayoría de las orientaciones y, crucialmente, puede manejar muestras densas y biológicamente relevantes. Al revelar cómo los filamentos de actina se entrelazan dentro y fuera del plano celular en lamelipodios y podosomas, este enfoque abre la puerta a estudios rutinarios que vinculen la organización fibra a fibra a nanoescala con el movimiento celular, la generación de fuerzas y la señalización.
Cita: Senthil Kumar, C.S., Valades Cruz, C.A., Sison, M. et al. 4polar3D single molecule imaging of 3D orientation in dense actin networks using ratiometric polarization splitting. Nat Commun 17, 4246 (2026). https://doi.org/10.1038/s41467-026-70852-y
Palabras clave: imagen de molécula individual, citoesqueleto de actina, microscopía por polarización, superresolución, mecánica celular