Clear Sky Science · it
Imaging 4polar3D a singola molecola per l’orientamento 3D in reti dense di actina mediante suddivisione polarimetrica ratiometrica
Un nuovo modo per vedere l’ordine nascosto all’interno delle cellule
All’interno di ogni cellula vivente, lunghi e sottili filamenti proteici formano uno scheletro che conferisce forma alla cellula e ne facilita il movimento. Queste fibre sono affollate e aggrovigliate, quindi anche microscopi avanzati spesso vedono solo una macchia di punti. Questo studio introduce un nuovo metodo di imaging che può rivelare non solo dove si trovano queste minuscole molecole, ma anche come sono orientate nello spazio tridimensionale, permettendo agli scienziati di mappare l’architettura nascosta di questo impalcatura interna in cellule integre.
Perché osservare la direzione è importante
Molte proteine nelle cellule funzionano come piccole frecce: la loro direzione nello spazio influenza come interagiscono, si assemblano e generano forze. I microscopi a super-risoluzione tradizionali possono individuare la posizione di singole molecole fluorescenti ma di solito ignorano il loro angolo di inclinazione o rotazione. Per strutture densamente impaccate, come i filamenti di actina al margine cellulare, conoscere solo le posizioni non è sufficiente per capire come le fibre sono disposte o come spingono e tirano sulla membrana cellulare. Una tecnica che cattura contemporaneamente posizione e orientamento su aree ampie può colmare il divario tra metodi strutturali dettagliati, come la microscopia elettronica, e metodi ottici più veloci usati nelle cellule vitali.
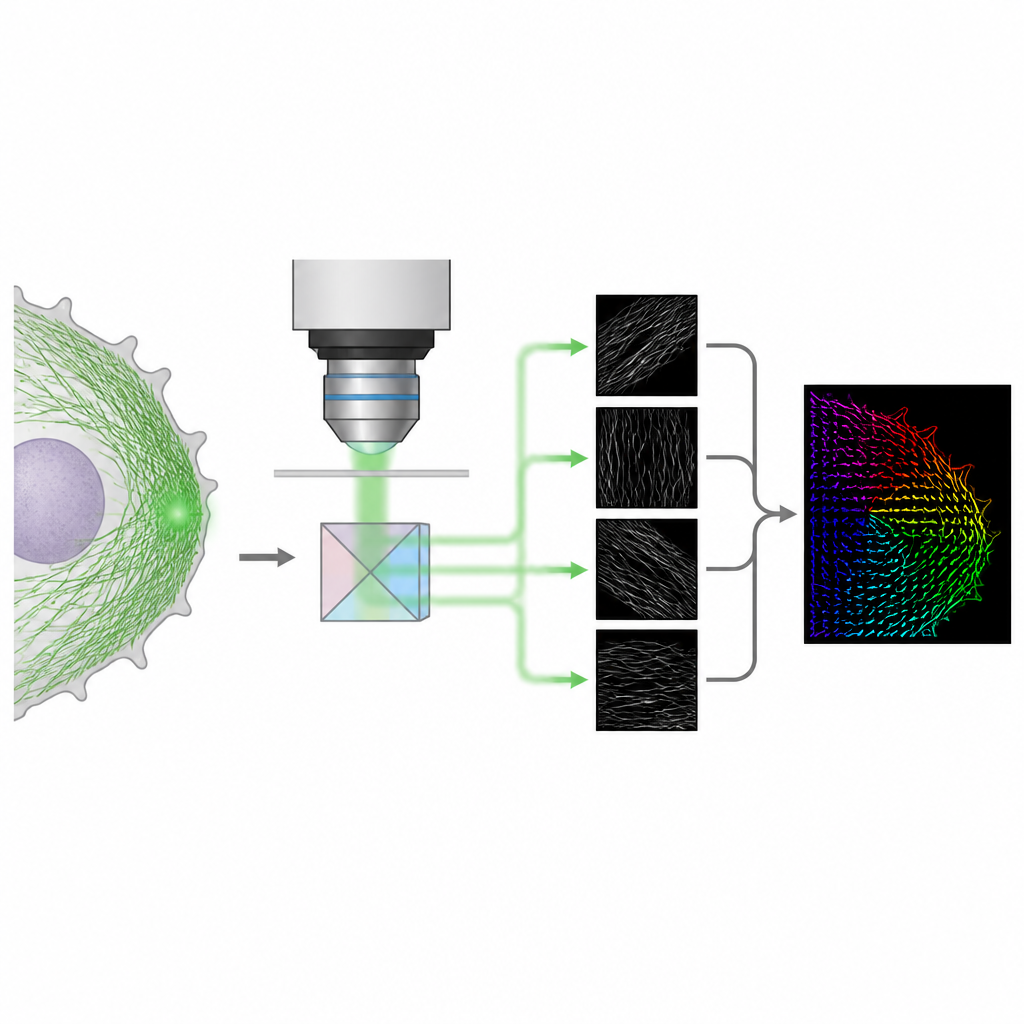
Un trucco ottico più semplice per l’orientamento 3D
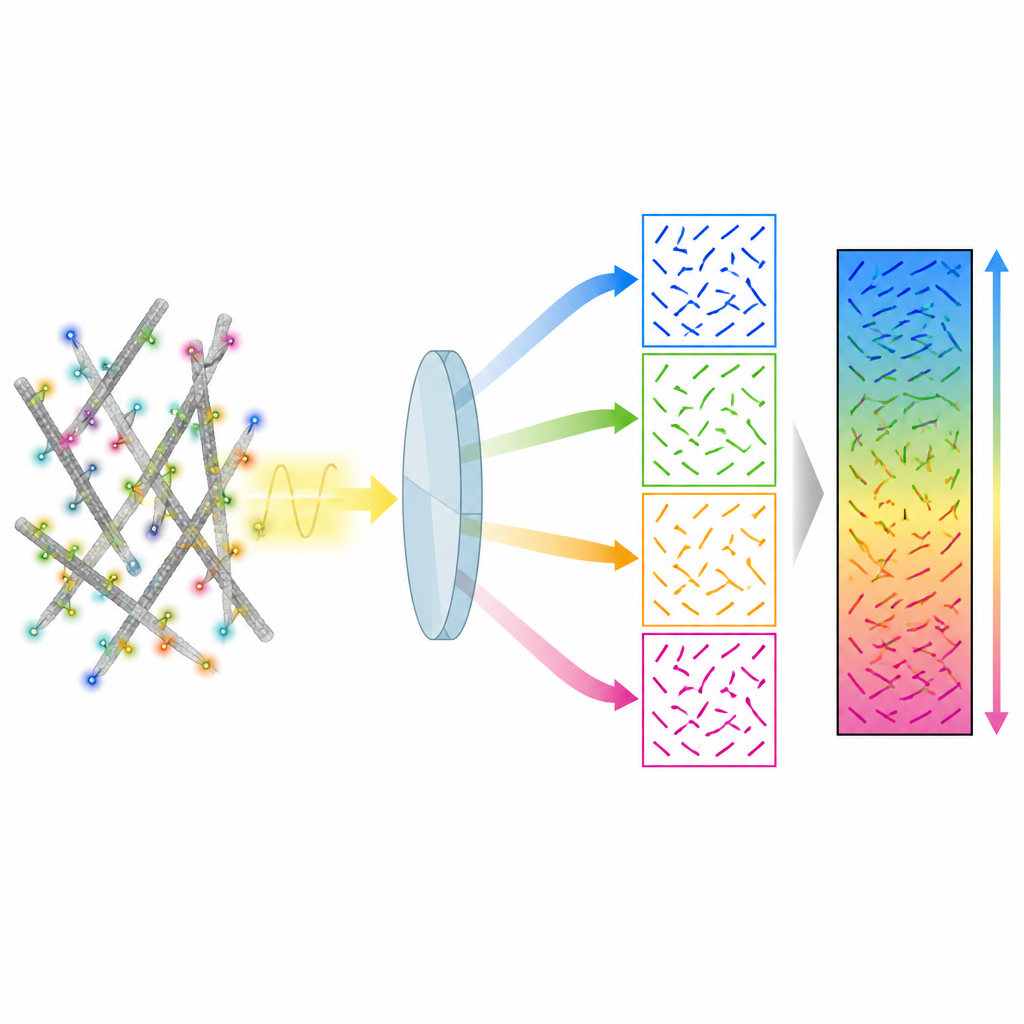
Gli autori presentano un metodo chiamato 4polar3D che misura l’orientamento delle singole molecole fluorescenti e il loro grado di tremolio, localizzandole anche all’interno della cellula. Invece di rimodellare il pattern di luce emesso da ciascuna molecola con ottiche complesse, il sistema divide la luce emessa in quattro fasci, ognuno filtrato da una polarizzazione e da un’apertura numerica diverse. Confrontando quanto luminosa appare la stessa molecola in questi quattro canali, il metodo estrae tre proprietà chiave: la direzione della molecola nel piano del vetrino, quanto essa è inclinata rispetto a quel piano e quanto può ruotare liberamente. Poiché si basa solo sulla brillantezza integrata anziché sull’adattamento di pattern dettagliati, l’analisi dei dati è rapida e robusta, anche quando molte molecole emettono luce contemporaneamente.
Testare il metodo su membrane modello
Per verificare che 4polar3D funzioni come previsto, il gruppo lo ha prima testato su semplici membrane lipidiche marcate con un colorante fluorescentе che tende ad allinearsi con le catene di acidi grassi. Su membrane supportate e piatte, il metodo ha misurato un’inclinazione preferita delle molecole di colorante e un ampio tremolio, in accordo con approcci precedenti più complessi. Quando la stessa membrana è stata avvolta attorno a piccole sfere di silice, le orientazioni misurate hanno seguito la curvatura della sfera: le molecole vicino al fondo puntavano più verso il microscopio, mentre quelle vicino ai lati diventavano più parallele alla superficie. Questi test hanno dimostrato che 4polar3D può recuperare accuratamente un’ampia gamma di angoli di inclinazione e distinguere tra orientamenti nel piano e fuori dal piano.
Rivelare l’architettura 3D dell’actina in cellule simili a quelle vive
I ricercatori si sono poi concentrati sulle dense reti di actina che guidano il movimento e l’adesione cellulare. In cellule di melanoma in rapido movimento, il sottile foglio alla parte anteriore della cellula, chiamato lamellipodio, è ricco di filamenti di actina. Usando un marcatore fluorescente che si lega lungo questi filamenti, 4polar3D ha registrato milioni di eventi a singola molecola e ricostruito una mappa dettagliata delle direzioni dei filamenti. Vicino al bordo estremo, la rete di actina mostrava una mescolanza di filamenti ramificati nel piano, con una coppia caratteristica di direzioni preferite, e una seconda popolazione di filamenti inclinati fuori dal piano con orientamenti più variabili. Più internamente, nella regione di transizione e nelle spesse fibre di stress, i filamenti risultavano per lo più nel piano e allineati lungo direzioni ben definite.
Scoprire la struttura 3D in piccoli organelli di adesione
Il metodo ha indagato anche i podosomi, minuscole strutture di adesione nelle cellule immunitarie più piccole del limite di diffrazione della luce. Mediando i dati di centinaia di podosomi, gli autori hanno trovato un pattern chiaro: al centro, molti filamenti di actina erano inclinati fuori dal piano e probabilmente si estendevano verso l’alto, mentre ai bordi, filamenti nel piano formavano un anello radiale che puntava verso l’esterno da ogni nucleo. Tra podosomi vicini, questo ordine radiale era in gran parte perduto. Le misure del fuoco apparente dei punti fluorescenti suggerivano che i filamenti fuori dal piano nel nucleo si trovano più in alto rispetto all’anello in-plane circostante, a sostegno di un quadro di impalcatura di actina stratificata e tridimensionale.
Qual è l’impatto per la biologia cellulare
In sintesi, 4polar3D offre un modo pratico per mappare come le molecole sono orientate in tre dimensioni su ampie aree di una cellula, utilizzando un allestimento ottico relativamente semplice e calcoli rapidi. Pur essendo meno preciso ad angoli di inclinazione estremi rispetto ad alcuni metodi più elaborati, funziona bene per la maggior parte delle orientazioni e, cosa cruciale, può gestire campioni affollati e biologicamente rilevanti. Rivelando come i filamenti di actina si intrecciano dentro e fuori dal piano cellulare in lamellipodi e podosomi, questo approccio apre la strada a studi di routine che collegano l’organizzazione delle fibre su scala nanometrica al movimento cellulare, alla generazione di forze e alla segnalazione.
Citazione: Senthil Kumar, C.S., Valades Cruz, C.A., Sison, M. et al. 4polar3D single molecule imaging of 3D orientation in dense actin networks using ratiometric polarization splitting. Nat Commun 17, 4246 (2026). https://doi.org/10.1038/s41467-026-70852-y
Parole chiave: imaging a singola molecola, citoscheletro di actina, microscopia polarimetrica, super risoluzione, meccanica cellulare