Clear Sky Science · fr
Imagerie 4polar3D de molécules uniques pour l’orientation 3D dans des réseaux d’actine denses via une séparation polarisée ratiométrique
Une nouvelle manière de voir l’ordre caché à l’intérieur des cellules
À l’intérieur de chaque cellule vivante, de longs filaments protéiques minces forment un échafaudage qui donne à la cellule sa forme et aide ses mouvements. Ces fibres sont compactes et emmêlées, si bien que même les microscopes avancés n’aperçoivent souvent qu’un flou de points. Cette étude présente une nouvelle méthode d’imagerie qui peut révéler non seulement où se trouvent ces minuscules molécules, mais aussi comment elles sont orientées en trois dimensions, permettant aux scientifiques de cartographier l’architecture cachée de cet échafaudage interne dans des cellules intactes.
Pourquoi la direction compte
Beaucoup de protéines dans les cellules se comportent comme de petites flèches : leur direction dans l’espace influence leurs interactions, leur assemblage et la génération de forces. Les microscopes super-résolution traditionnels peuvent localiser des molécules fluorescentes uniques mais ignorent généralement leur inclinaison ou leur rotation. Pour des structures densément emballées comme les filaments d’actine au bord cellulaire, connaître uniquement les positions ne suffit pas pour comprendre comment les fibres sont arrangées ou comment elles poussent et tirent sur la membrane. Une technique capable de capturer simultanément position et orientation, sur de grandes zones, peut combler le fossé entre des méthodes structurales détaillées comme la microscopie électronique et des méthodes optiques plus rapides utilisées sur des cellules vivantes.
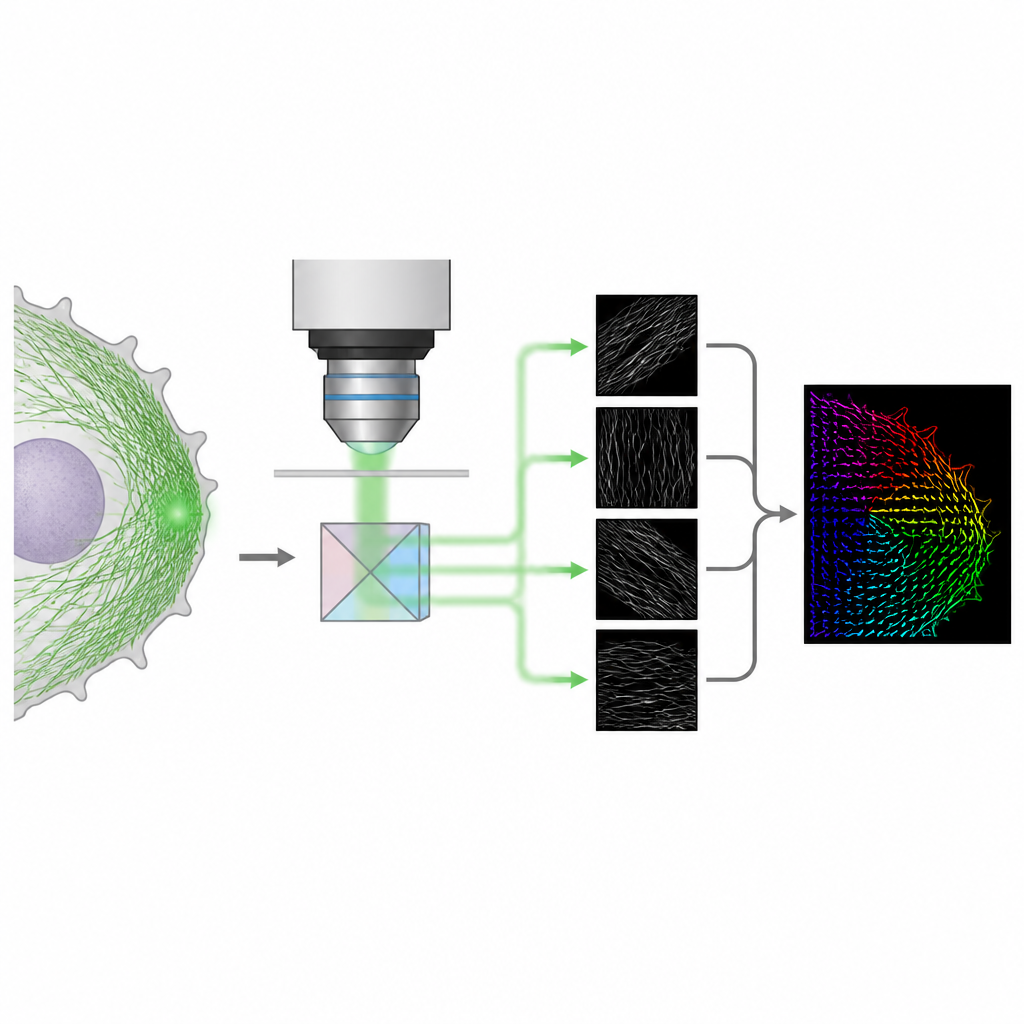
Une astuce optique plus simple pour l’orientation 3D
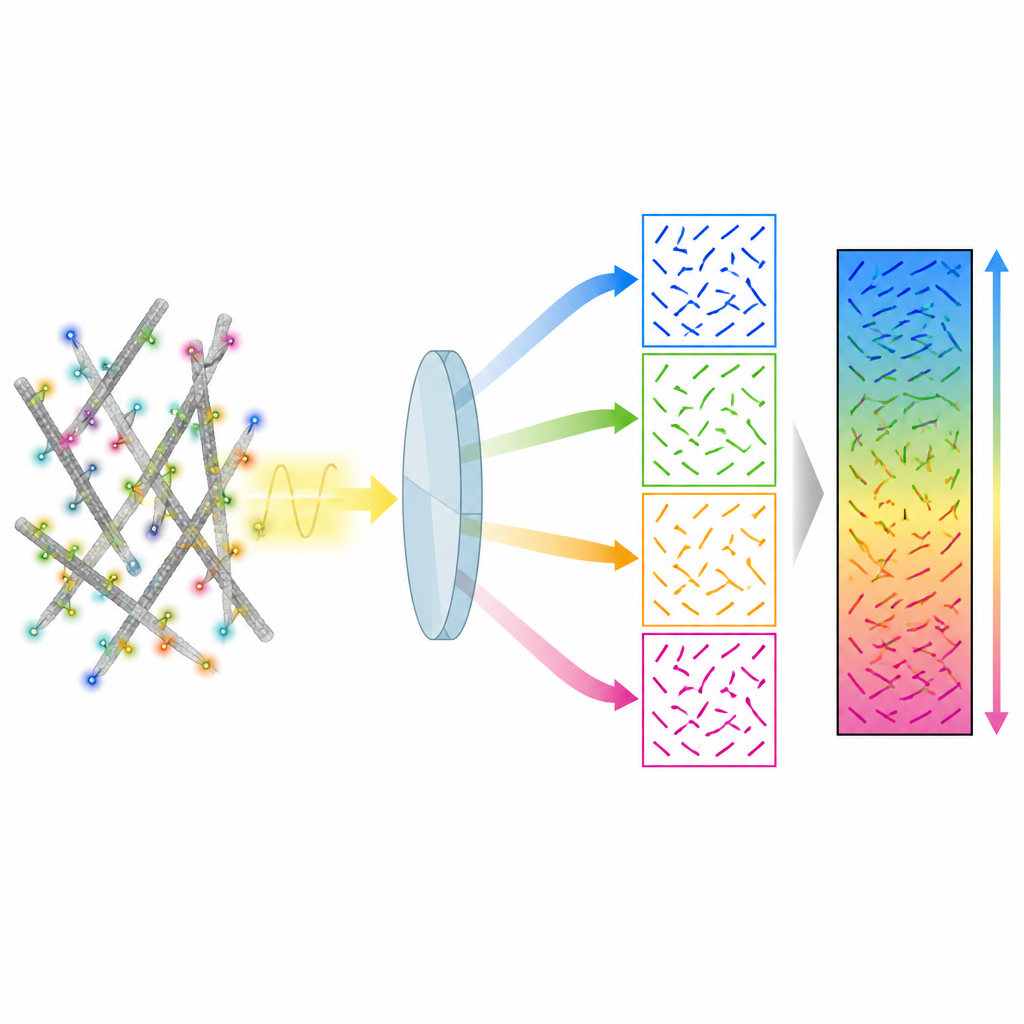
Les auteurs présentent une méthode appelée 4polar3D qui mesure l’orientation des molécules fluorescentes uniques et l’amplitude de leur fluctuation angulaire, tout en les localisant dans la cellule. Plutôt que de remodeler le motif lumineux émis par chaque molécule avec des optiques complexes, le système divise la lumière émise en quatre faisceaux, chacun filtré par une polarisation et une ouverture numérique différentes. En comparant l’intensité apparente de la même molécule dans ces quatre canaux, la méthode extrait trois propriétés clés : la direction de la molécule dans le plan de la lame microscopique, son inclinaison hors de ce plan et sa liberté de rotation. Parce qu’elle se base uniquement sur l’intensité intégrée plutôt que sur l’ajustement de motifs détaillés, l’analyse des données est rapide et robuste, même lorsque de nombreuses molécules émettent simultanément.
Tester la méthode sur des membranes modèles
Pour vérifier que 4polar3D fonctionne comme prévu, l’équipe l’a d’abord testée sur de simples membranes lipidiques marquées par une sonde fluorescente qui tend à s’aligner sur les chaînes d’acides gras. Sur des membranes supportées et planes, la méthode a mesuré une inclinaison préférentielle des molécules de la sonde et une fluctuation large, en accord avec des approches antérieures plus complexes. Lorsque la même membrane a été enroulée autour de petites billes de silice, les orientations mesurées ont suivi la courbure de la sphère : les molécules près du bas pointaient davantage vers le microscope, tandis que celles près des côtés devenaient plus parallèles à la surface. Ces tests ont montré que 4polar3D peut récupérer avec précision une large gamme d’angles d’inclinaison et distinguer entre orientations dans le plan et hors du plan.
Révéler l’architecture 3D de l’actine dans des cellules proches du vivant
Les chercheurs se sont ensuite intéressés aux réseaux d’actine denses qui gouvernent le mouvement et l’adhésion cellulaire. Dans des cellules de mélanome à déplacement rapide, la mince feuille à l’avant de la cellule, appelée lamellipode, est saturée de filaments d’actine. En utilisant une étiquette fluorescente se liant le long de ces filaments, 4polar3D a enregistré des millions d’événements de molécules uniques et reconstruit une carte détaillée des directions des filaments. Près du bord extrême, le réseau d’actine montrait un mélange de filaments branchés dans le plan, avec une paire caractéristique de directions préférentielles, et une seconde population de filaments inclinés hors du plan avec des orientations plus variées. Plus en arrière, dans la zone de transition et dans les fibres de tension épaisses, les filaments devenaient principalement dans le plan et alignés selon des directions nettes.
Mettre au jour la structure 3D dans de minuscules organelles d’adhésion
La méthode a également exploré les podosomes, de petites structures d’adhésion présentes dans les cellules immunitaires et plus petites que la limite de diffraction de la lumière. En moyennant les données de centaines de podosomes, les auteurs ont découvert un schéma clair : au centre, de nombreux filaments d’actine étaient inclinés hors du plan et s’étendaient vraisemblablement vers le haut, tandis qu’autour des bords, des filaments dans le plan formaient un anneau radial pointant vers l’extérieur de chaque cœur. Entre podosomes voisins, ce motif radial ordonné était en grande partie perdu. Les mesures de la mise au point apparente des taches fluorescentes suggéraient que les filaments hors du plan au centre se trouvaient plus haut au-dessus de la surface de verre que l’anneau in-plane environnant, soutenant l’idée d’un échafaudage d’actine stratifié et tridimensionnel.
Ce que cela signifie pour la biologie cellulaire
En résumé, 4polar3D offre une manière pratique de cartographier l’orientation des molécules en trois dimensions sur de larges zones d’une cellule, en utilisant un dispositif optique relativement simple et des calculs rapides. S’il est moins précis pour des angles d’inclinaison extrêmes que certaines méthodes plus élaborées, il fonctionne bien pour la plupart des orientations et, surtout, peut traiter des échantillons denses et biologiquement pertinents. En révélant comment les filaments d’actine s’entrelacent à l’intérieur et en dehors du plan cellulaire dans les lamellipodes et les podosomes, cette approche ouvre la voie à des études de routine reliant l’organisation des fibres à l’échelle nanométrique au mouvement cellulaire, à la génération de forces et à la signalisation.
Citation: Senthil Kumar, C.S., Valades Cruz, C.A., Sison, M. et al. 4polar3D single molecule imaging of 3D orientation in dense actin networks using ratiometric polarization splitting. Nat Commun 17, 4246 (2026). https://doi.org/10.1038/s41467-026-70852-y
Mots-clés: imagerie de molécules uniques, cytosquelette d’actine, microscopie par polarisation, super-résolution, mécanique cellulaire