Clear Sky Science · zh
提高 Magnets 光感受器 的性能
用光束塑造细胞
想象一下能像开关一样,用一束光轻松地开启或关闭基因。该研究展示了科学家如何改进一类流行的光感受蛋白“开关”——称为 Magnets 光感受器,使其对蓝光的响应更精确、更强大。改良后的开关能够帮助研究者在细菌甚至哺乳动物细胞中以更少的光、更低的损伤和更大灵活性来控制细胞行为。
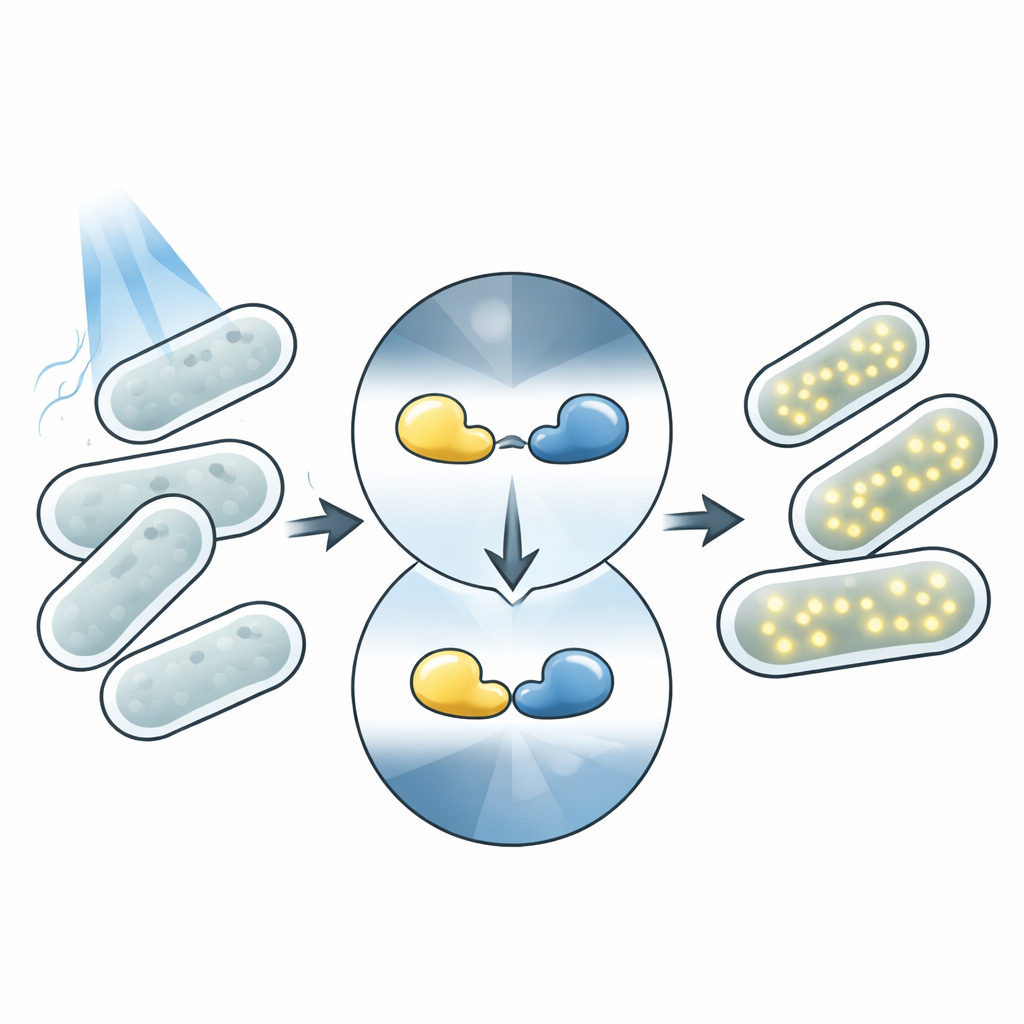
为何光是强大的控制旋钮
光是生物学的理想远程控制手段。与化学添加剂不同,光可以瞬时施加,也能同样快速移除,并可聚焦到微小区域而不接触细胞。许多生物天然含有在吸收光后改变构象并触发下游效应的蛋白质。现代光遗传学将这些蛋白重新用于可控部件:将一个光感头与一个执行模块(如酶或基因开关)融合。当光照射时,传感器改变构象并激活附着的功能。Magnets 光感受器是一对在蓝光下结合、黑暗中分离的蛋白,使其成为构建光控系统的主要工具。
Magnet 开关在细胞中的工作原理
在这项工作中,团队聚焦于一个蓝光响应系统,称为 Opto-T7RNAP。这里,Magnets 对被融合到分裂酶 T7 RNA 聚合酶的两个半链上,驱动目标基因的表达。在黑暗中,两个半链保持分离,基因大多沉默。置于蓝光下,Magnets 结构域相互结合,将酶的两半拉到一起,使基因开启并产生可方便测量的红色荧光蛋白。该设置将每个光感蛋白的 DNA 序列与可见输出紧密连接,使研究者仅通过测量细胞的发光强度就能读取成千上万变体的性能。
随机变异与精心选择
作者没有凭直觉去修改单个氨基酸,而是使用随机诱变在每个 Magnet 蛋白中引入变化,然后让数据揭示哪些版本表现最好。他们创建了大量突变的 nMag 与 pMag 库,并将它们导入携带 Opto-T7RNAP 和荧光报告基因的细菌中。通过荧光激活细胞分选,他们进行了多步骤筛选:首先富集在微弱蓝光下强烈发光的细胞,然后剔除在黑暗中发光过强的细胞,最后分离出单克隆进行详细测试。每个变体的发光水平要么通过流式细胞术逐细胞跟踪,要么通过自动分光光度计在大规模培养中随时间测量。
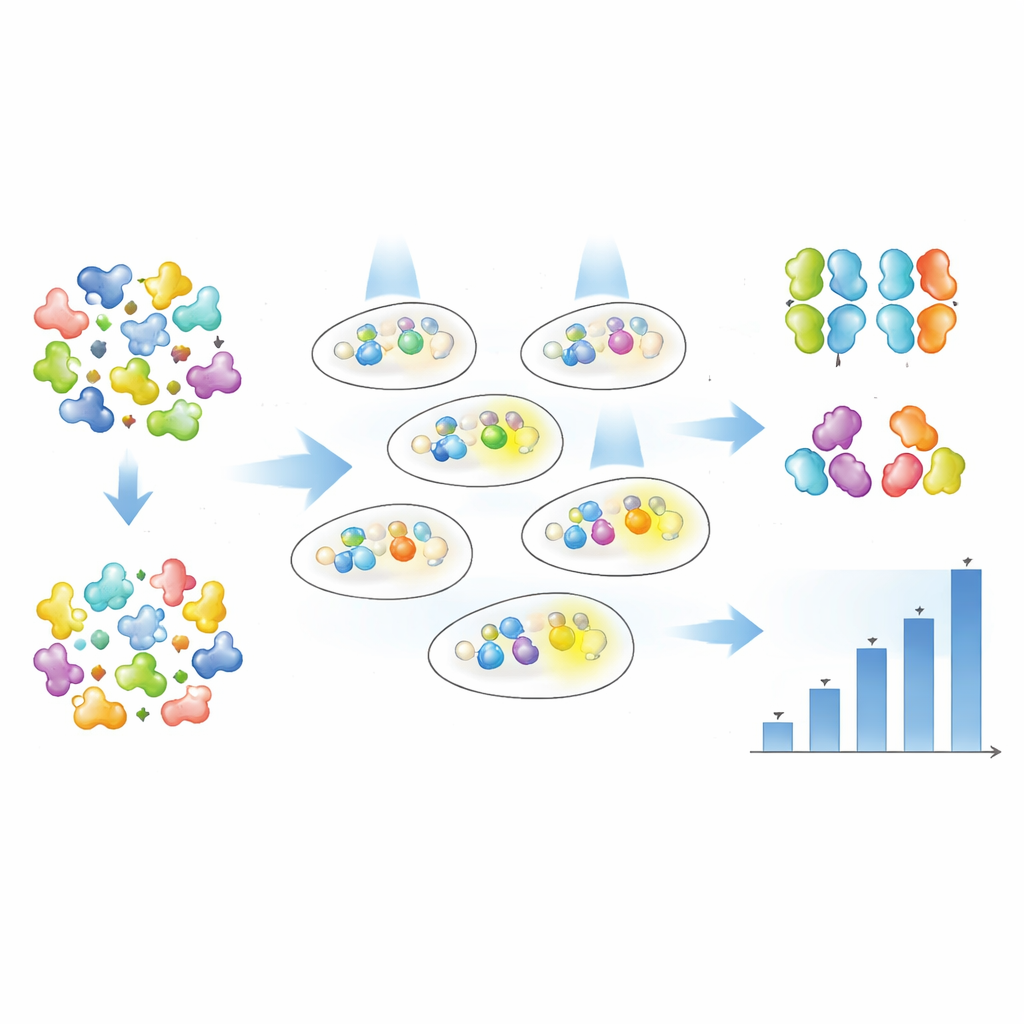
微调灵敏度与强度
仅通过一轮筛选,团队就发现了 19 个具有丰富不同行为的 Magnet 变体。有些突变体显著提高了系统的光敏感性,也就是说用远低的光强即可达到相同的基因产出。其他突变体主要提高在饱和光下基因的开启强度,还有些两者兼具。重要的是,作者展示了“需要多少光”(灵敏度)和“能产生多少基因产出”(激活度)可以在很大程度上独立调节。在某些变体中,半最大激活所需的光约为原来的一半,但最大产出保持相似;在另一些变体中,最大产出提高了几倍而灵敏度大致不变。通过在不同温度下比较多个变体,他们还识别出在接近体温条件下仍能保持更强活性并在细胞群体生长过程中表现稳健的版本。
光控生物学的新构件
对非专业读者而言,主要信息是这些科学家已将单一光开关扩展为完整的调光面板。取代单一固定的蓝光传感器,他们现在提供了一系列 Magnet 变体,要求更多或更少的光、产生更强或更温和的基因响应,或能在不同温度下良好工作。由于 Magnets 已广泛用于合成生物学并已被改造用于哺乳动物细胞,这些改良版本可以插入许多现有设计中。从实际角度看,这意味着需要温和、长期照明的实验可以使用高灵敏度变体,而必须避免室内光意外激活的应用则可选择低灵敏度变体。因此,该工作拓宽了用光精确塑造细胞行为的工具箱,对研究和生物技术具有重要价值。
引用: Baumschlager, A., Weber, Y., Cánovas, D. et al. Enhancing the performance of Magnets photosensors. Nat Commun 17, 4138 (2026). https://doi.org/10.1038/s41467-026-70695-7
关键词: 光遗传学, 光控基因表达, 蛋白质工程, 光感受蛋白, 合成生物学