Clear Sky Science · sv
Förbättring av prestanda hos Magnets-fotosensorer
Formge celler med ljusstrålar
Föreställ dig att kunna slå på och av gener med en ljusstråle lika enkelt som att vrida en strömbrytare. Denna studie visar hur forskare har förbättrat en populär familj av ljus-känsliga protein"brytare", kallade Magnets-fotosensorer, så att de reagerar mer precist och kraftfullt på blått ljus. Dessa uppgraderade brytare kan hjälpa forskare att styra cellbeteende med mindre ljus, mindre skada och större flexibilitet i både bakterier och däggdjursceller.
Varför ljus är en kraftfull kontrollknapp
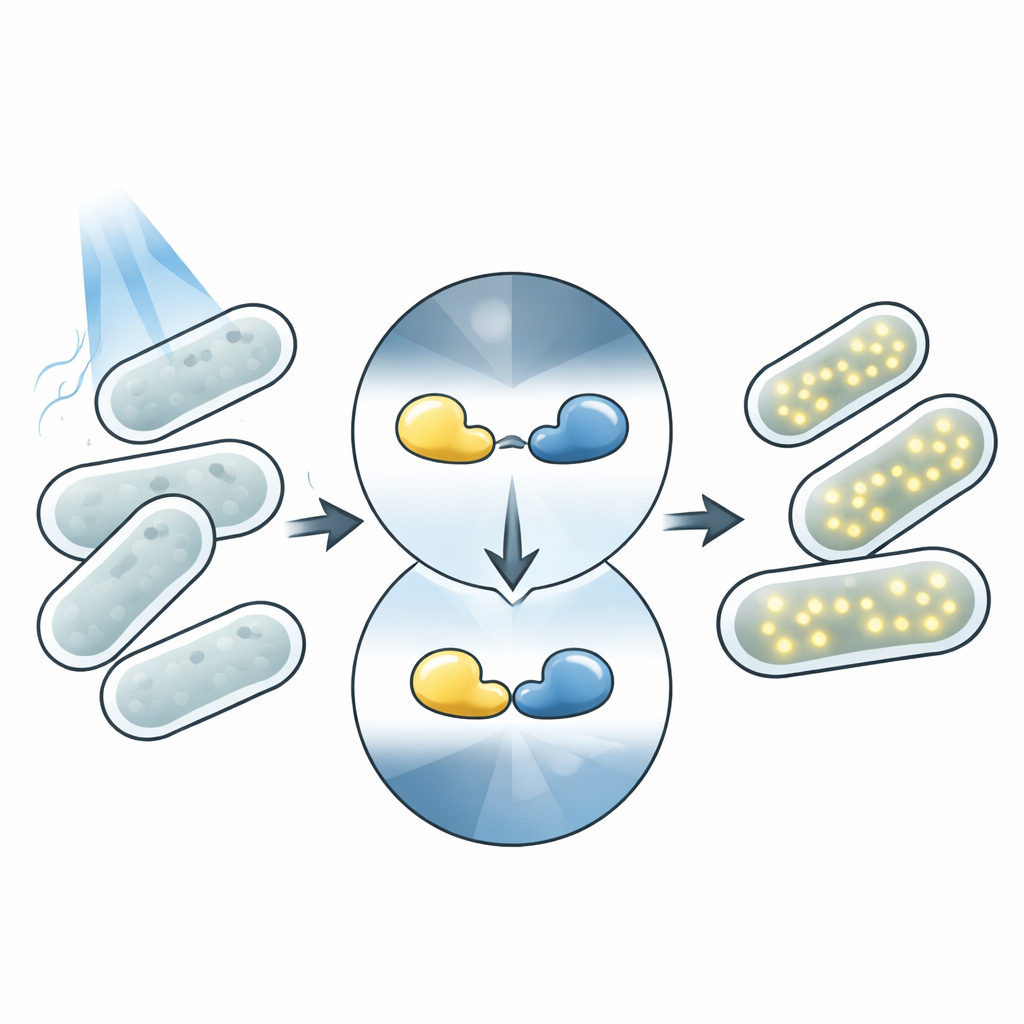
Ljus är en idealisk fjärrkontroll för biologi. Till skillnad från kemiska tillsatser kan ljus appliceras omedelbart, tas bort lika snabbt och fokuseras på små områden utan att röra cellerna. Många organismer har naturligt proteiner som ändrar form när de absorberar ljus, vilket utlöser efterföljande effekter. Modern optogenetik återanvänder dessa proteiner som kontrollerbara delar: ett ljussensoriskt "huvud" fogas samman med en "verkande" modul, såsom ett enzym eller en genbrytare. När ljus faller på sensorn ändrar den form och aktiverar den kopplade funktionen. Magnets-fotosensorer är ett par sådana proteiner som binds ihop under blått ljus och separerar i mörker, vilket gör dem till ett arbetsredskap för att bygga ljusstyrda system.
Hur Magnet-brytaren fungerar i celler
I detta arbete fokuserar teamet på ett blåljuskänsligt system kallat Opto-T7RNAP. Här är Magnets-paret förenat med två halvor av ett splittrat enzym, T7 RNA-polymeras, som driver uttrycket av en målgene. I mörker håller sig halvorna isär och genen är till största delen tyst. Under blått ljus binder Magnet-domänerna till varandra och drar enzymhalvorna samman så att genen slås på och producerar ett rött fluorescerande protein som enkelt kan mätas. Denna uppställning kopplar tätt DNA-sekvensen för varje ljussensoriskt protein till en synlig utsignal, vilket gör det möjligt för forskarna att avläsa prestandan hos tusentals varianter enbart genom att mäta hur starkt cellerna lyser.
Slumpmässiga förändringar och noggrann selektion
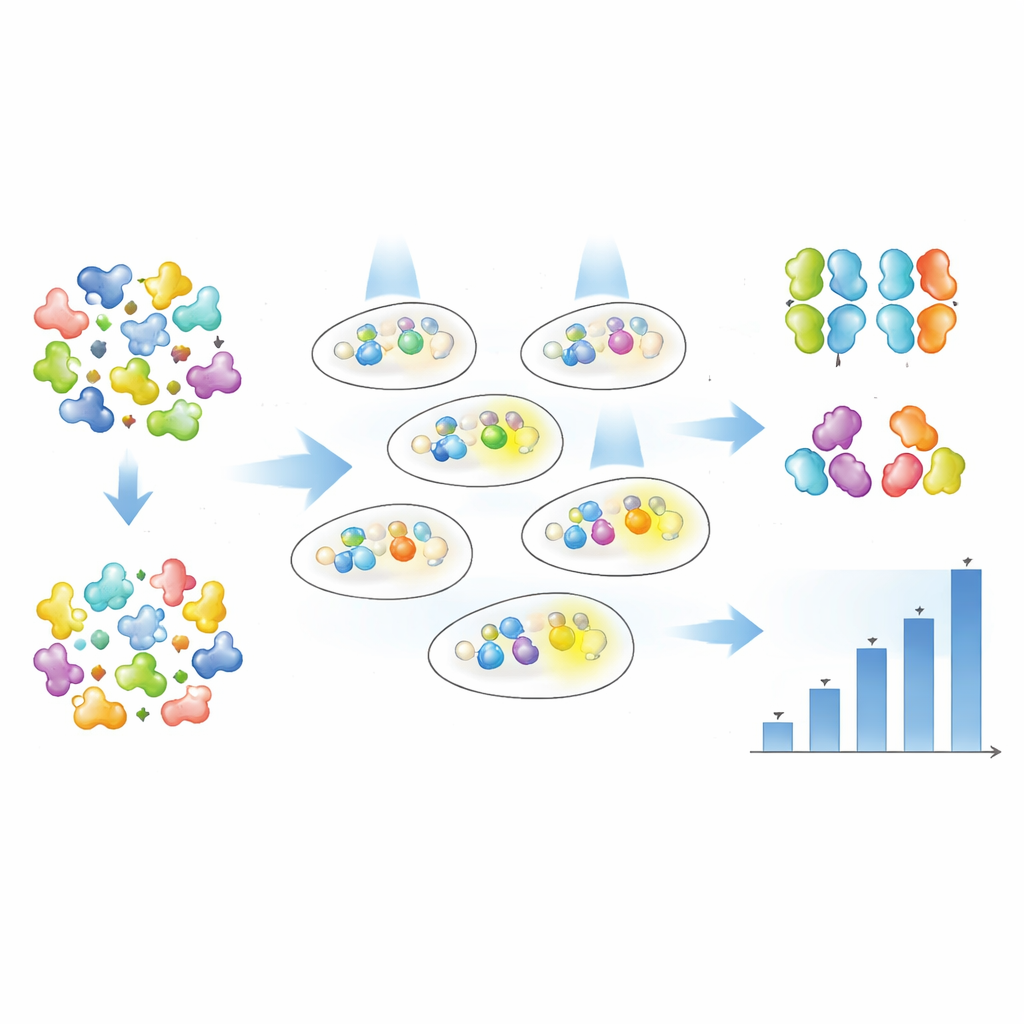
I stället för att gissa vilka enstaka aminosyror som bör ändras använde författarna random mutagenes för att införa förändringar i hela varje Magnet-protein och lät sedan data avslöja vilka versioner som fungerade bäst. De skapade stora bibliotek av muterade nMag- och pMag-varianter och införde dem i bakterier som bar Opto-T7RNAP och en fluorescerande rapportörgen. Med fluorescensaktiverad cellsortering genomförde de ett flerstegsselektion: först berikade de celler som lyste starkt vid svagt blått ljus, sedan sorterades celler bort som lyste för mycket i mörker, och till sist isolerades individuella kloner för detaljerade tester. Varje variant följdes vad gäller ljusstyrka antingen cell för cell med flödescytometri eller i bulkkulturer över tid med automatiserad spektrofotometri.
Finjustera känslighet och styrka
Redan efter en enda omgång screening fann teamet 19 distinkta Magnet-varianter med ett rikt spektrum av beteenden. Vissa mutanter gjorde systemet mycket mer ljuskänsligt, vilket innebär att samma genuttryck kan uppnås med betydligt lägre ljusintensitet. Andra ökade främst hur starkt genen slås på vid fullt ljus, och några gjorde båda delarna. Viktigt är att författarna visade att "hur mycket ljus som behövs" (känslighet) och "hur stort genuttrycket blir" (aktivering) i stor utsträckning kan justeras oberoende av varandra. I vissa varianter nåddes halvmaximal aktivering med ungefär halva ljusmängden, samtidigt som maximal utsignal förblev liknande; i andra ökade maximal utsignal flera gånger medan känsligheten förblev ungefär densamma. Genom att jämföra många varianter över temperaturer identifierade de även versioner som bibehåller starkare aktivitet vid kroppslika förhållanden och uppvisar robust beteende under cellpopulationens tillväxt.
Nya byggstenar för ljusstyrd biologi
För en icke-specialist är huvudbudskapet att dessa forskare har förvandlat en enda ljusbrytare till en hel dimmerpanel. I stället för en fast blåljussensor erbjuder de nu en meny av Magnet-varianter som kräver mer eller mindre ljus, ger starkare eller svagare genresponser, eller presterar väl över olika temperaturer. Eftersom Magnets redan är vida använda inom syntetisk biologi och har anpassats till däggdjursceller kan dessa förbättrade versioner kopplas in i många befintliga konstruktioner. I praktiska termer betyder det att experiment som kräver skonsam, långvarig belysning kan använda mycket känsliga varianter, medan tillämpningar som måste undvika oavsiktlig aktivering av rumsljus kan välja mindre känsliga. Arbetet breddar därmed verktygslådan för att precist forma cellbeteende med ljus inom forskning och bioteknik.
Citering: Baumschlager, A., Weber, Y., Cánovas, D. et al. Enhancing the performance of Magnets photosensors. Nat Commun 17, 4138 (2026). https://doi.org/10.1038/s41467-026-70695-7
Nyckelord: optogenetik, ljusstyrd genuttryck, proteinengineering, fotosensoriska proteiner, syntetisk biologi