Clear Sky Science · de
Verbesserung der Leistungsfähigkeit von Magnets-Photosensoren
Zellen mit Lichtstrahlen formen
Stellen Sie sich vor, Gene mit einem Lichtstrahl so einfach ein- und ausschalten zu können wie einen Schalter. Diese Studie zeigt, wie Forschende eine beliebte Familie lichtempfindlicher Protein„schalter“, die Magnets-Photosensoren, so verbessert haben, dass sie präziser und wirkungsvoller auf blaues Licht reagieren. Diese optimierten Schalter könnten Forschenden ermöglichen, das Verhalten von Zellen mit weniger Licht, weniger Schaden und größerer Flexibilität zu steuern — sowohl in Bakterien als auch in Säugerzellen.
Warum Licht ein starkes Steuerinstrument ist
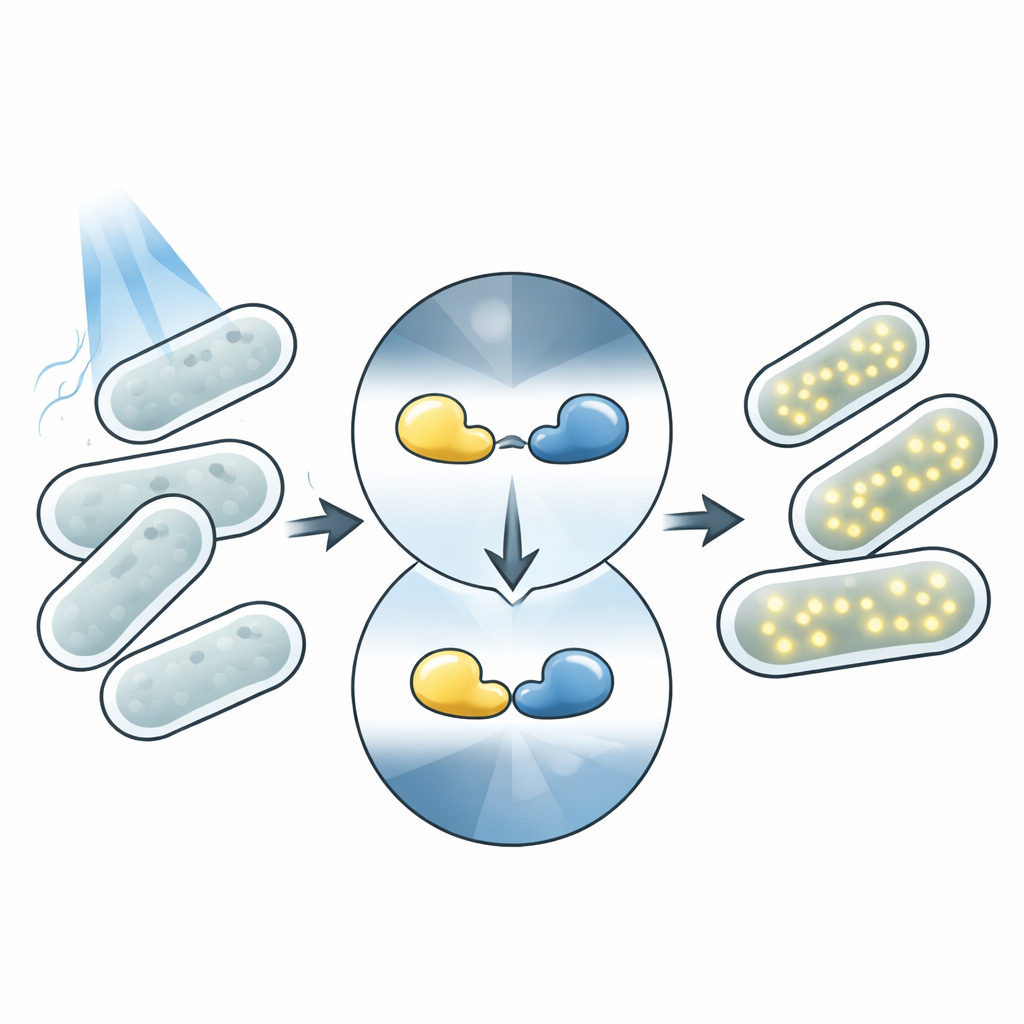
Licht ist eine ideale Fernsteuerung für die Biologie. Anders als chemische Zusätze lässt sich Licht sofort zuschalten, genauso schnell wieder entfernen und auf winzige Bereiche fokussieren, ohne die Zellen zu berühren. Viele Organismen enthalten von Natur aus Proteine, die ihre Form ändern, wenn sie Licht absorbieren, und dadurch nachgelagerte Effekte auslösen. Die moderne Optogenetik nutzt diese Proteine als steuerbare Bausteine: ein lichtempfindlicher „Kopf“ wird mit einem „Aktions“-Modul wie einem Enzym oder einem Gen-Schalter verbunden. Wenn Licht eintrifft, ändert der Sensor seine Form und aktiviert die angehängte Funktion. Magnets-Photosensoren sind ein Paar solcher Proteine, die sich unter blauem Licht anlagern und im Dunkeln wieder trennen — was sie zu einem bewährten Werkzeugsatz für lichtgesteuerte Systeme macht.
Wie der Magnet-Schalter in Zellen funktioniert
In dieser Arbeit konzentriert sich das Team auf ein blaulichtempfindliches System namens Opto-T7RNAP. Hier ist das Magnets-Paar an zwei Hälften eines geteilten Enzyms, der T7-RNA-Polymerase, gekoppelt, die die Expression eines Zielgens antreibt. Im Dunkeln bleiben die Hälften getrennt und das Gen ist größtenteils still. Unter blauem Licht binden die Magnet-Domänen aneinander, ziehen die Enzymhälften zusammen, sodass das Gen eingeschaltet wird und ein rot fluoreszierendes Protein produziert, das leicht messbar ist. Diese Anordnung verknüpft die DNA-Sequenz jedes lichtempfindlichen Proteins eng mit einer sichtbaren Ausgabe, sodass die Forschenden die Leistung tausender Varianten allein daran ablesen können, wie stark die Zellen leuchten.
Zufällige Veränderungen und sorgfältige Auswahl
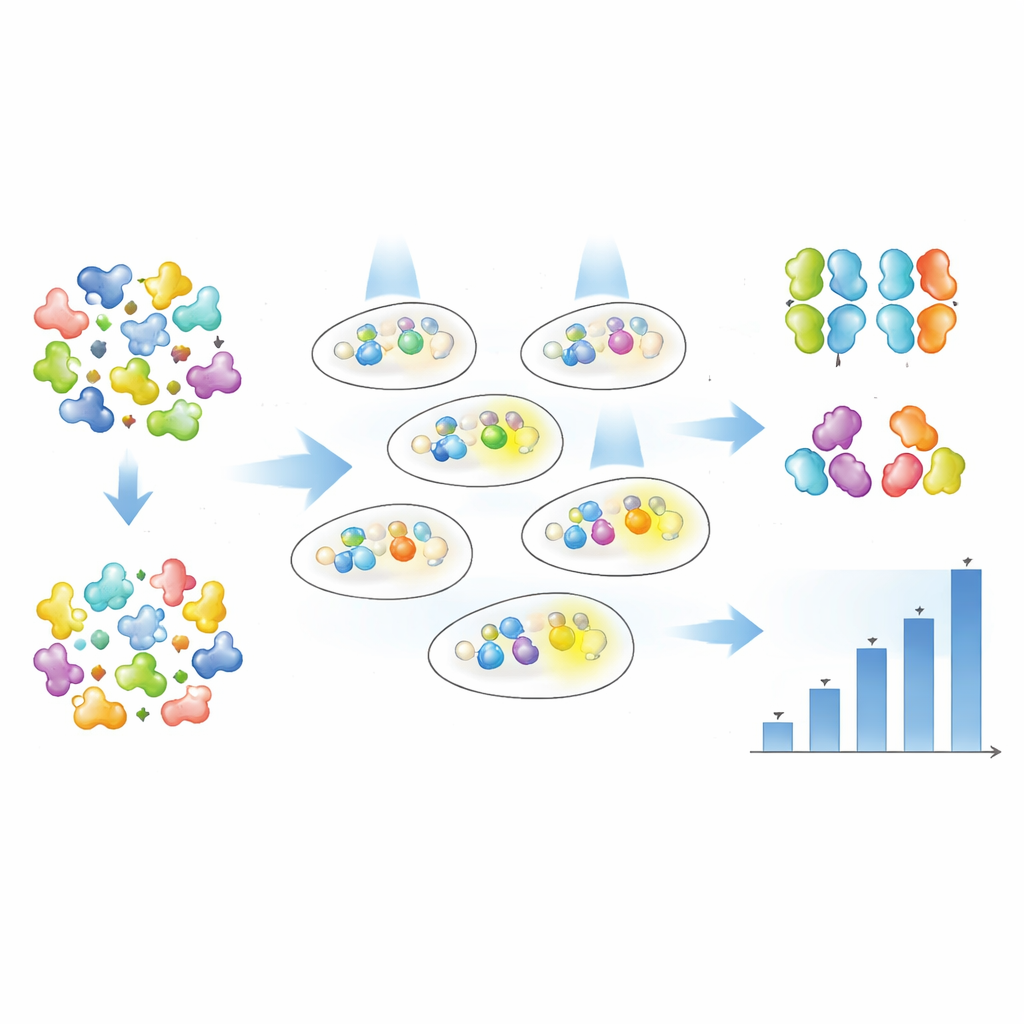
Anstatt zu raten, welche einzelnen Aminosäuren man verändern sollte, nutzten die Autorinnen und Autoren gerichtete Zufallsmutagenese, um Veränderungen über das gesamte Magnet-Protein zu verteilen, und ließen die Daten zeigen, welche Versionen am besten funktionierten. Sie erzeugten große Bibliotheken mutierter nMag- und pMag-Varianten und führten diese in Bakterien ein, die Opto-T7RNAP und das fluoreszente Reporter-Gen trugen. Mittels Durchflusszytometrie mit Fluoreszenzsortierung führten sie eine mehrstufige Selektion durch: zunächst Anreicherung von Zellen, die unter schwachem Blaulicht stark leuchteten, dann Aussortieren von Zellen, die im Dunkeln zu stark leuchteten, und schließlich Isolierung einzelner Klone für detaillierte Tests. Der Leuchtgrad jeder Variante wurde entweder zellweise per Durchflusszytometrie oder in Populationskulturen über die Zeit mit automatischer Spektralphotometrie verfolgt.
Feinabstimmung von Empfindlichkeit und Stärke
Bereits nach einer Screening-Runde fand das Team 19 unterschiedliche Magnet-Varianten mit einem breiten Spektrum an Verhaltensweisen. Einige Mutanten machten das System deutlich lichtempfindlicher, sodass für denselben Genoutput wesentlich geringere Lichtintensitäten ausreichen. Andere erhöhten vor allem, wie stark das Gen bei voller Beleuchtung eingeschaltet wird, und manche bewirkten beides. Wichtig ist, dass die Autorinnen und Autoren zeigten, dass „wie viel Licht nötig ist“ (Empfindlichkeit) und „wie viel Genoutput man erhält“ (Aktivierung) weitgehend unabhängig voneinander einstellbar sind. Bei manchen Varianten wurde die halbmaximale Aktivierung mit etwa der Hälfte der Lichtmenge erreicht, während der maximale Output ähnlich blieb; bei anderen erhöhte sich der Maximalwert um das Mehrfache, während die Empfindlichkeit in etwa gleich blieb. Durch den Vergleich vieler Varianten über verschiedene Temperaturen identifizierten sie außerdem Versionen, die bei körperähnlichen Bedingungen stärkere Aktivität beibehalten und während des Populationswachstums robust arbeiten.
Neue Bausteine für lichtgesteuerte Biologie
Für Nicht-Spezialistinnen und Nicht-Spezialisten lautet die zentrale Botschaft: Diese Forschenden haben einen einzelnen Lichtschalter in ein ganzes Dimmer-Panel verwandelt. Statt eines festen Blaulicht-Sensors steht nun eine Palette von Magnet-Varianten zur Verfügung, die mehr oder weniger Licht benötigen, stärkere oder mildere Genantworten erzeugen oder bei unterschiedlichen Temperaturen gut funktionieren. Da Magnets bereits in der synthetischen Biologie weit verbreitet sind und an Säugerzellen angepasst wurden, lassen sich diese verbesserten Versionen in viele bestehende Konzepte einbauen. Praktisch bedeutet das: Experimente, die schonende, langzeitige Beleuchtung erfordern, können hochempfindliche Varianten nutzen, während Anwendungen, die versehentliche Aktivierung durch Raumlicht vermeiden müssen, weniger empfindliche Varianten wählen können. Die Arbeit erweitert damit das Werkzeugspektrum, um das Verhalten von Zellen mittels Licht in Forschung und Biotechnologie präzise zu formen.
Zitation: Baumschlager, A., Weber, Y., Cánovas, D. et al. Enhancing the performance of Magnets photosensors. Nat Commun 17, 4138 (2026). https://doi.org/10.1038/s41467-026-70695-7
Schlüsselwörter: Optogenetik, lichtgesteuerte Genexpression, Proteinengineering, photosensorische Proteine, synthetische Biologie