Clear Sky Science · pl
Poprawa wydajności fotosensorów Magnets
Kształtowanie komórek wiązkami światła
Wyobraź sobie, że możesz włączać i wyłączać geny wiązką światła tak łatwo, jak przełącznik. W tym badaniu naukowcy pokazują, jak ulepszyli popularną rodzinę świetlnych „przełączników” białkowych, zwanych fotosensorami Magnets, aby reagowały precyzyjniej i silniej na światło niebieskie. Ulepszone przełączniki mogą pomóc badaczom kontrolować zachowanie komórek przy użyciu mniejszej ilości światła, powodując mniej szkód i dając większą elastyczność zarówno u bakterii, jak i u komórek ssaczych.
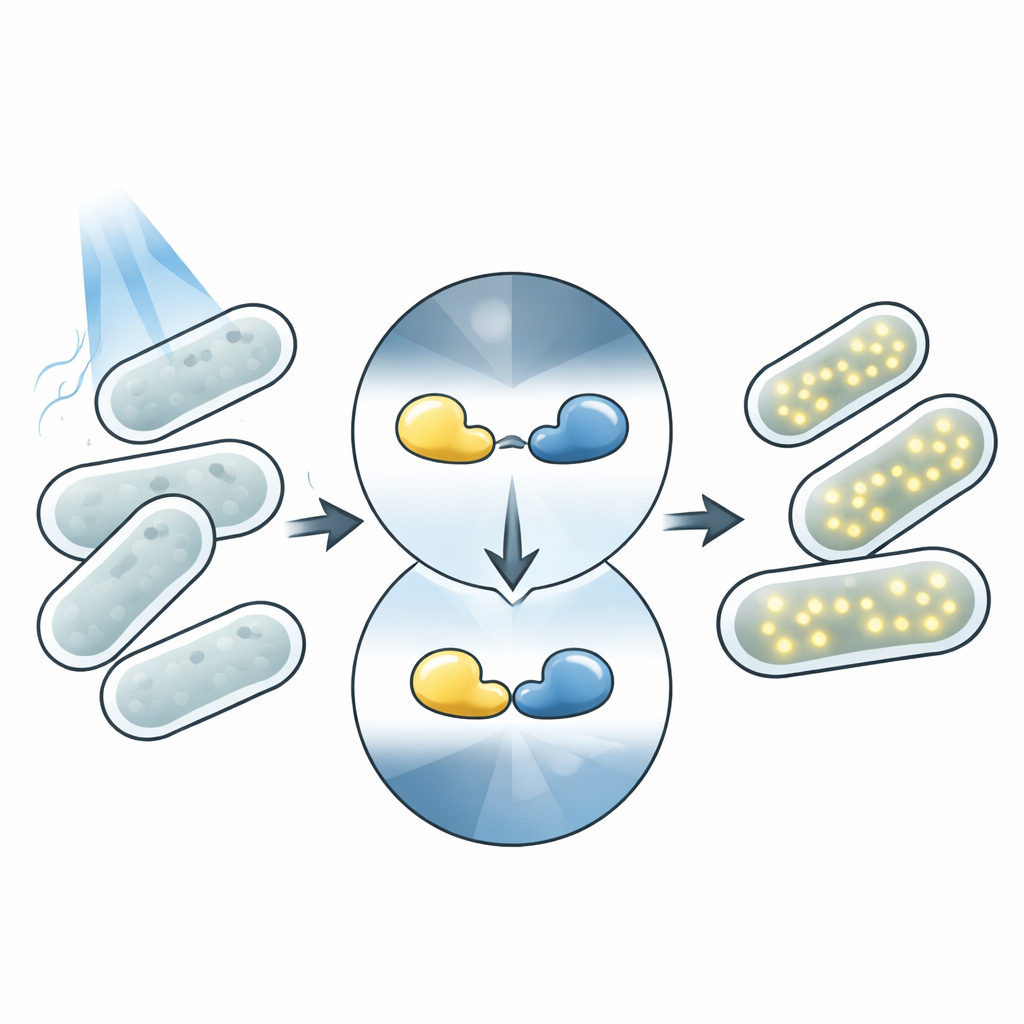
Dlaczego światło to potężny regulator
Światło to idealny pilot do sterowania procesami biologicznymi. W przeciwieństwie do dodatków chemicznych, można je zastosować natychmiast, równie szybko usunąć i skupić na niewielkich obszarach bez bezpośredniego kontaktu z komórkami. Wiele organizmów naturalnie zawiera białka, które zmieniają kształt po absorpcji światła, wywołując dalsze efekty. Współczesna optogenetyka wykorzystuje te białka jako sterowalne moduły: światłoczuła „główka” jest połączona z modułem wykonawczym, takim jak enzym czy przełącznik genowy. Gdy pada światło, sensor zmienia konformację i aktywuje dołączoną funkcję. Fotosensory Magnets to para takich białek, które łączą się pod wpływem światła niebieskiego i rozdzielają w ciemności, co czyni je uniwersalnym narzędziem do budowy systemów sterowanych światłem.
Jak działa przełącznik Magnet w komórkach
W tej pracy zespół koncentruje się na systemie reagującym na światło niebieskie, nazwanym Opto-T7RNAP. Para Magnets jest tutaj połączona z dwiema połówkami rozdzielonego enzymu T7 RNA polimerazy, który napędza ekspresję docelowego genu. W ciemności połówki pozostają oddzielone i gen jest w większości nieaktywny. Pod wpływem światła niebieskiego domeny Magnets wiążą się ze sobą, ściągając połówki enzymu razem, co powoduje włączenie genu i produkcję czerwonego białka fluorescencyjnego, które można łatwo zmierzyć. Takie zestawienie ściśle łączy sekwencję DNA każdego białka światłoczułego z widocznym sygnałem wyjściowym, pozwalając badaczom ocenić wydajność tysięcy wariantów po prostu mierząc, jak intensywnie świecą komórki.
Losowe zmiany i staranny dobór
Zamiast zgadywać, które pojedyncze aminokwasy modyfikować, autorzy zastosowali losową mutagenezę, wprowadzając zmiany w całym białku Magnet, a następnie pozwolili danym wykazać, które wersje działają najlepiej. Stworzyli duże biblioteki zmutowanych wariantów nMag i pMag i wprowadzili je do bakterii zawierających Opto-T7RNAP oraz gen raportowy fluorescencyjny. Za pomocą sortowania komórek w oparciu o fluorescencję wykonali selekcję wieloetapową: najpierw wzbogacili komórki silnie świecące przy słabym świetle niebieskim, potem odrzucili te, które świeciły zbyt mocno w ciemności, a na końcu wyizolowali pojedyncze klony do szczegółowych testów. Poziom świecenia każdego wariantu śledzono albo pojedynczo metodą cytometrii przepływowej, albo w hodowlach masowych w czasie za pomocą zautomatyzowanej spektrofotometrii.
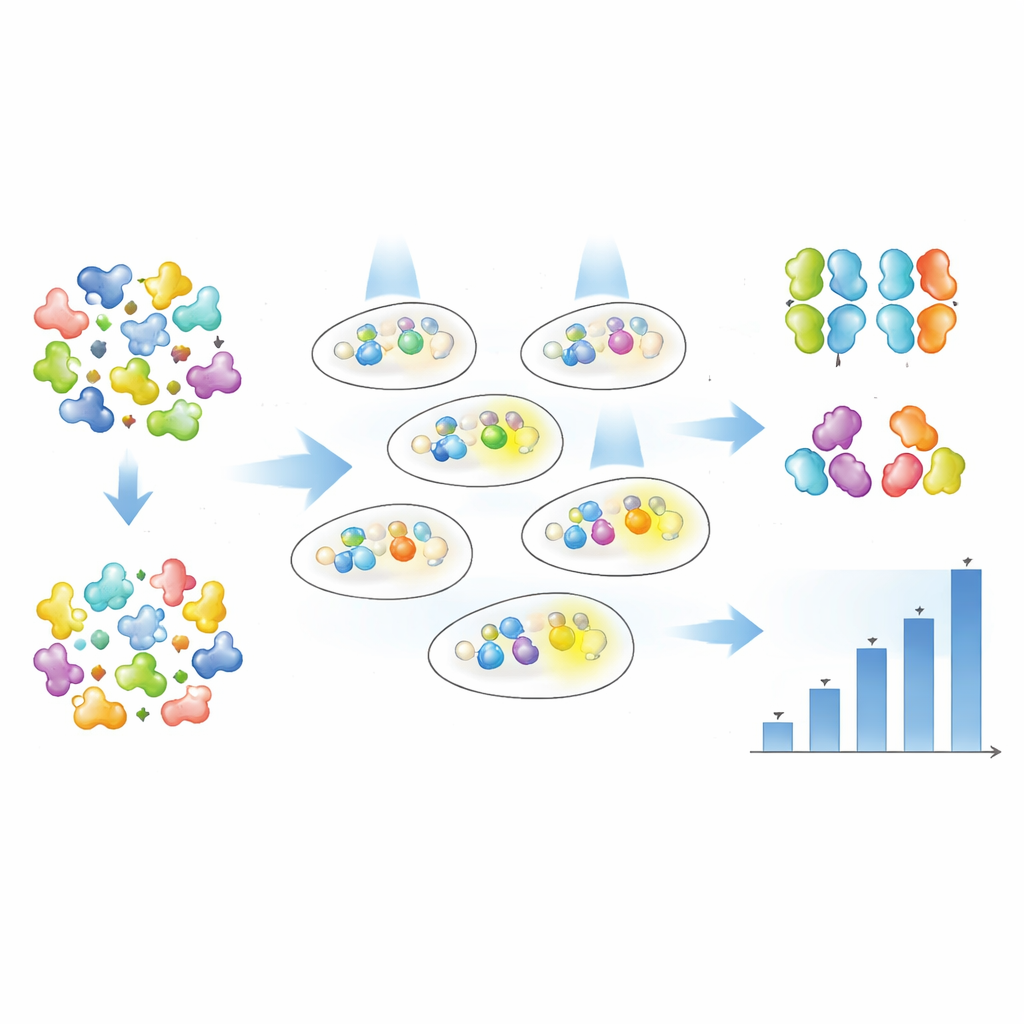
Dostrajanie czułości i siły działania
Już po jednej rundzie przesiewu zespół znalazł 19 odrębnych wariantów Magnet o różnorodnych właściwościach. Niektóre mutacje znacząco zwiększyły czułość na światło, co oznacza, że ten sam poziom ekspresji genu można osiągnąć przy znacznie niższej intensywności światła. Inne głównie zwiększały siłę włączenia genu przy pełnym oświetleniu, a niektóre robiły obie rzeczy równocześnie. Co ważne, autorzy pokazali, że „ile światła jest potrzebne” (czułość) i „jaki jest poziom odpowiedzi genowej” (aktywacja) można w dużej mierze regulować niezależnie. W niektórych wariantach aktywacja półmaksymalna była osiągana przy mniej więcej połowie światła, przy zachowaniu podobnego maksymalnego wyjścia; w innych maksymalny sygnał zwiększył się wielokrotnie przy zachowaniu podobnej czułości. Porównując wiele wariantów w różnych temperaturach, zidentyfikowali również wersje, które utrzymują silniejszą aktywność w warunkach podobnych do warunków ciała i zachowują stabilne działanie przez cały okres wzrostu populacji komórek.
Nowe cegiełki dla biologii sterowanej światłem
Dla laika główny wniosek jest taki, że naukowcy zamienili pojedynczy przełącznik świetlny w cały panel ściemniaczy. Zamiast jednego stałego sensora światła niebieskiego oferują teraz zestaw wariantów Magnet, które wymagają więcej lub mniej światła, generują silniejszą lub słabszą odpowiedź genową albo działają dobrze w różnych temperaturach. Ponieważ Magnets są już szeroko stosowane w biologii syntetycznej i zostały dostosowane do komórek ssaczych, ulepszone wersje można włączyć do wielu istniejących projektów. W praktyce oznacza to, że eksperymenty wymagające delikatnego, długotrwałego naświetlania mogą korzystać z wysoce czułych wariantów, natomiast zastosowania, które muszą unikać przypadkowej aktywacji przez światło w pomieszczeniu, mogą użyć wariantów mniej czułych. Praca poszerza zatem zestaw narzędzi do precyzyjnego modelowania zachowania komórek za pomocą światła w badaniach i biotechnologii.
Cytowanie: Baumschlager, A., Weber, Y., Cánovas, D. et al. Enhancing the performance of Magnets photosensors. Nat Commun 17, 4138 (2026). https://doi.org/10.1038/s41467-026-70695-7
Słowa kluczowe: opto-genetyka, światłocontrolled ekspresja genów, inżynieria białek, białka fotosensoryczne, biologia syntetyczna