Clear Sky Science · pt
Melhorando o desempenho dos fotossensores Magnets
Moldando células com feixes de luz
Imagine poder ligar e desligar genes com um feixe de luz tão facilmente quanto acionar um interruptor. Este estudo mostra como cientistas aprimoraram uma família popular de "interruptores" proteicos sensíveis à luz, chamados fotossensores Magnets, para que respondam de forma mais precisa e potente à luz azul. Esses interruptores melhorados podem ajudar pesquisadores a controlar o comportamento celular com menos luz, menos danos e maior flexibilidade em bactérias e até em células de mamíferos.
Por que a luz é um poderoso botão de controle
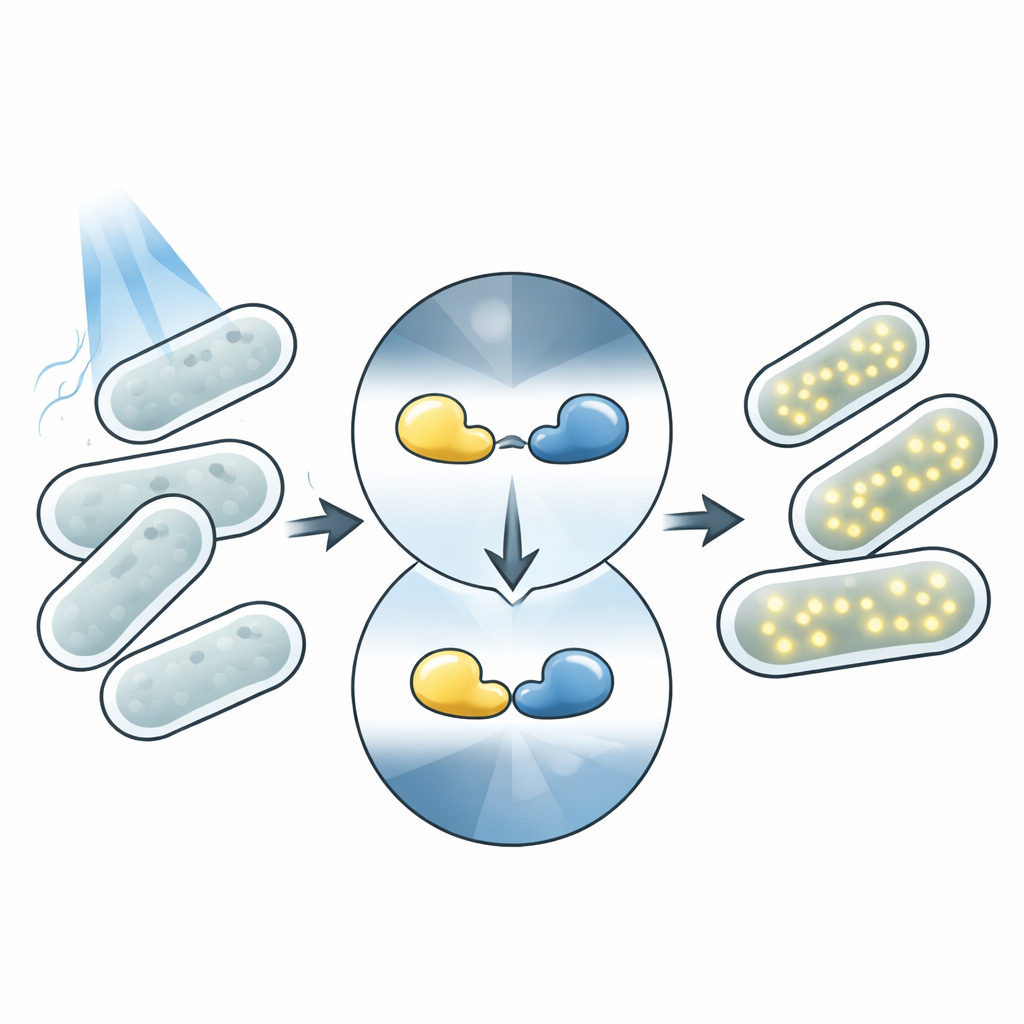
A luz é um controle remoto ideal para a biologia. Ao contrário de aditivos químicos, a luz pode ser aplicada instantaneamente, removida com igual rapidez e focalizada em regiões minúsculas sem tocar as células. Muitos organismos contêm naturalmente proteínas que mudam de forma ao absorver luz, desencadeando efeitos a jusante. A optogenética moderna reutiliza essas proteínas como peças controláveis: uma "cabeça" sensora de luz é fundida a um módulo de "ação", como uma enzima ou um interruptor gênico. Quando a luz incide, o sensor muda de conformação e ativa a função acoplada. Os fotossensores Magnets são um par dessas proteínas que se unem sob luz azul e se separam no escuro, tornando-se uma ferramenta robusta para construir sistemas controlados por luz.
Como o interruptor Magnet funciona nas células
Neste trabalho, a equipe concentra-se em um sistema sensível à luz azul chamado Opto-T7RNAP. Aqui, o par Magnets é fundido às duas metades de uma enzima dividida, a RNA polimerase T7, que dirige a expressão de um gene alvo. No escuro, as metades permanecem separadas e o gene fica majoritariamente silencioso. Sob luz azul, os domínios Magnets se ligam entre si, aproximando as metades da enzima de modo que o gene é ativado e produz uma proteína fluorescente vermelha que pode ser medida facilmente. Essa configuração liga de forma estreita a sequência de DNA de cada proteína sensora a uma saída visível, permitindo aos pesquisadores avaliar o desempenho de milhares de variantes simplesmente medindo o brilho das células.
Mudança aleatória e seleção cuidadosa
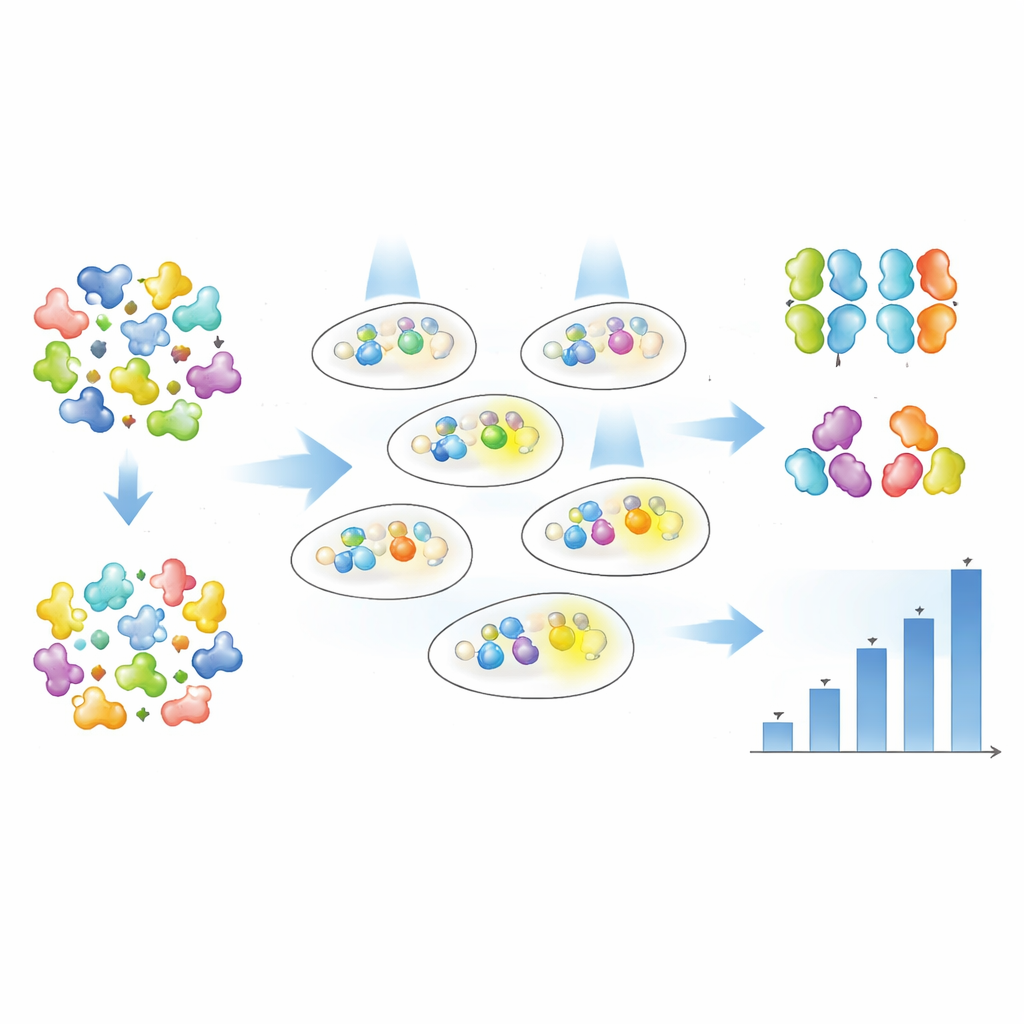
Em vez de adivinhar quais aminoácidos individuais modificar, os autores usaram mutagênese aleatória para introduzir mudanças em todo o comprimento de cada proteína Magnet e então deixaram os dados revelar quais versões funcionavam melhor. Eles criaram grandes bibliotecas de variantes mutadas de nMag e pMag e as introduziram em bactérias que carregavam o Opto-T7RNAP e o gene repórter fluorescente. Usando separação celular por fluorescência (FACS), realizaram uma seleção em múltiplas etapas: primeiro enriquecendo células que brilhavam fortemente sob luz azul fraca, depois descartando células que brilhavam demais no escuro e, por fim, isolando clones individuais para testes detalhados. O nível de brilho de cada variante foi acompanhado tanto célula a célula por citometria de fluxo quanto em culturas em larga escala ao longo do tempo com espectrofotometria automatizada.
Ajustando sensibilidade e intensidade
A partir de apenas uma rodada de triagem, a equipe encontrou 19 variantes distintas de Magnets com uma rica diversidade de comportamentos. Alguns mutantes tornaram o sistema muito mais sensível à luz, o que significa que a mesma saída gênica podia ser alcançada com intensidade de luz bem menor. Outros aumentaram principalmente a força com que o gene era ativado na luz plena, e alguns fizeram ambos. Importante, os autores demonstraram que “quanto de luz é necessário” (sensibilidade) e “quanto de saída gênica você obtém” (ativação) podem ser ajustados de forma largamente independente. Em algumas variantes, a ativação meia-maximal foi atingida com aproximadamente metade da luz, enquanto a saída máxima permaneceu similar; em outras, a saída máxima aumentou várias vezes enquanto a sensibilidade permaneceu mais ou menos igual. Ao comparar muitas variantes em diferentes temperaturas, eles também identificaram versões que mantêm atividade mais forte em condições próximas às do corpo e exibem comportamento robusto ao longo do crescimento da população celular.
Novos blocos de construção para biologia controlada por luz
Para um não especialista, a mensagem principal é que esses cientistas transformaram um único interruptor de luz em um painel inteiro de dimerização. Em vez de um sensor fixo de luz azul, eles agora oferecem um cardápio de variantes Magnets que exigem mais ou menos luz, produzem respostas gênicas mais fortes ou mais suaves, ou funcionam bem em diferentes temperaturas. Como os Magnets já são amplamente usados em biologia sintética e foram adaptados para células de mamíferos, essas versões aprimoradas podem ser integradas a muitos projetos existentes. Em termos práticos, isso significa que experimentos que necessitam de iluminação suave e de longo prazo podem usar variantes altamente sensíveis, enquanto aplicações que precisam evitar ativação acidental pela luz ambiente podem usar variantes menos sensíveis. O trabalho amplia, portanto, a caixa de ferramentas para esculpir com precisão o comportamento celular com luz na pesquisa e na biotecnologia.
Citação: Baumschlager, A., Weber, Y., Cánovas, D. et al. Enhancing the performance of Magnets photosensors. Nat Commun 17, 4138 (2026). https://doi.org/10.1038/s41467-026-70695-7
Palavras-chave: optogenética, expressão gênica controlada por luz, engenharia de proteínas, proteínas fotossensoriais, biologia sintética