Clear Sky Science · fr
Amélioration des performances des photosenseurs Magnets
Façonner les cellules avec des faisceaux de lumière
Imaginez pouvoir activer et désactiver des gènes avec un faisceau de lumière aussi simplement qu’un interrupteur. Cette étude montre comment des chercheurs ont amélioré une famille populaire d’« interrupteurs » protéiques sensibles à la lumière, appelés photosenseurs Magnets, pour qu’ils répondent de manière plus précise et plus puissante à la lumière bleue. Ces interrupteurs optimisés pourraient permettre aux chercheurs de contrôler le comportement cellulaire avec moins de lumière, moins de dommages et davantage de souplesse, tant chez les bactéries que chez les cellules de mammifères.
Pourquoi la lumière est un puissant bouton de commande
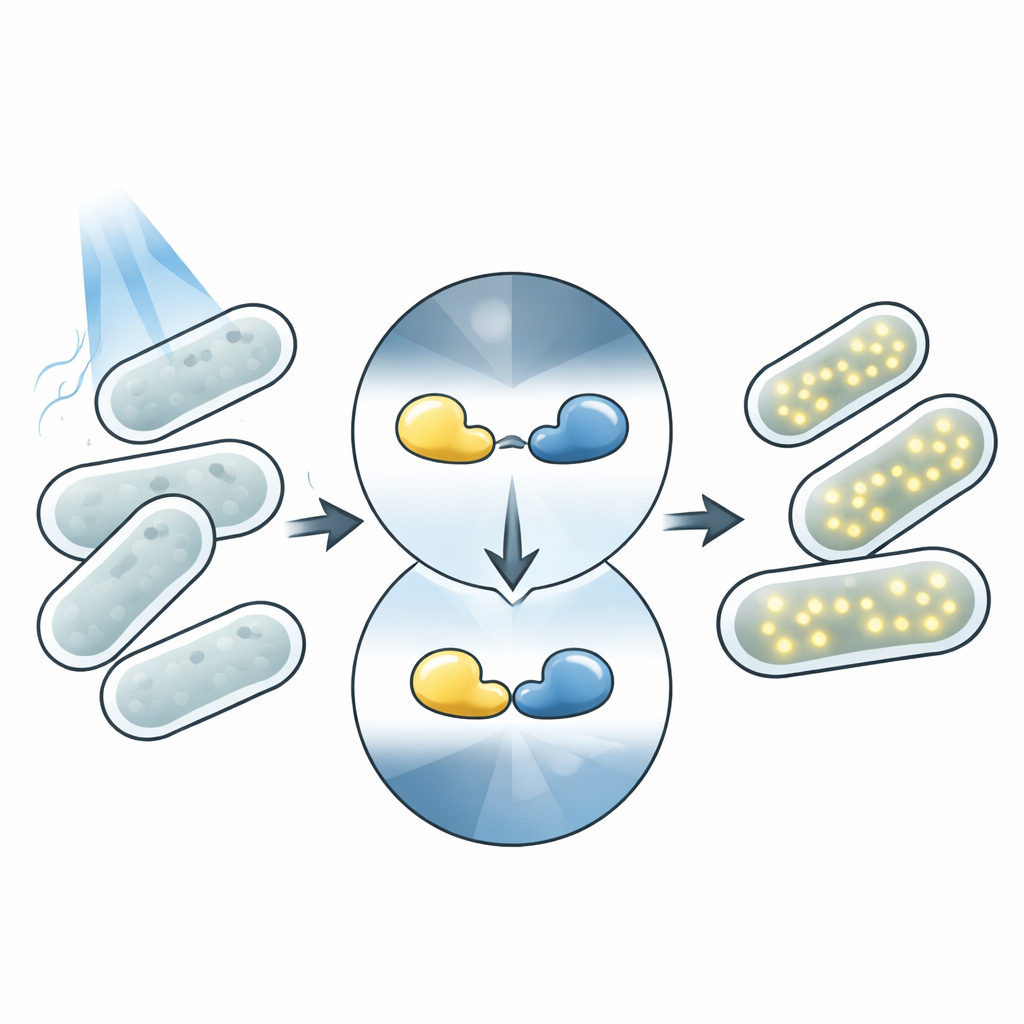
La lumière est une télécommande idéale pour la biologie. Contrairement aux additifs chimiques, elle peut être appliquée instantanément, retirée tout aussi vite et focalisée sur de petites régions sans toucher les cellules. De nombreux organismes contiennent naturellement des protéines qui changent de conformation lorsqu’elles absorbent de la lumière, déclenchant des effets en aval. L’optogénétique moderne réutilise ces protéines comme éléments contrôlables : une « tête » détectrice de lumière est fusionnée à un module d’« action » comme une enzyme ou un commutateur génique. Quand la lumière brille, le capteur change de forme et active la fonction attachée. Les photosenseurs Magnets sont une paire de protéines de ce type qui s’assemblent sous lumière bleue et se dissocient dans l’obscurité, ce qui en fait un outil phare pour construire des systèmes contrôlés par la lumière.
Comment l’interrupteur Magnet fonctionne dans les cellules
Dans ce travail, l’équipe se concentre sur un système réactif à la lumière bleue appelé Opto-T7RNAP. Ici, la paire Magnets est fusionnée aux deux moitiés d’une enzyme scindée, l’ARN polymérase T7, qui pilote l’expression d’un gène cible. Dans l’obscurité, les moitiés restent séparées et le gène est majoritairement silencieux. Sous lumière bleue, les domaines Magnets se lient entre eux, rapprochant les moitiés de l’enzyme de sorte que le gène s’active et produit une protéine fluorescente rouge facilement mesurable. Cette configuration relie étroitement la séquence d’ADN de chaque protéine détectrice à une sortie visible, permettant aux chercheurs d’évaluer les performances de milliers de variantes simplement en mesurant l’intensité de la fluorescence des cellules.
Changements aléatoires et sélection rigoureuse
Plutôt que de deviner quels acides aminés uniques modifier, les auteurs ont utilisé la mutagenèse aléatoire pour introduire des changements tout au long de chaque protéine Magnet, puis ont laissé les données révéler quelles versions fonctionnaient le mieux. Ils ont créé de larges bibliothèques de variantes nMag et pMag mutées et les ont introduites dans des bactéries portant l’Opto-T7RNAP et le gène rapporteur fluorescent. À l’aide du tri cellulaire par flux de fluorescence, ils ont effectué une sélection en plusieurs étapes : d’abord enrichir les cellules qui brillaient fortement sous une faible lumière bleue, puis écarter celles qui brillaient trop dans l’obscurité, et enfin isoler des clones individuels pour des tests détaillés. Le niveau de fluorescence de chaque variante a été suivi soit cellule par cellule par cytométrie en flux, soit en cultures en vrac au fil du temps par spectrophotométrie automatisée.
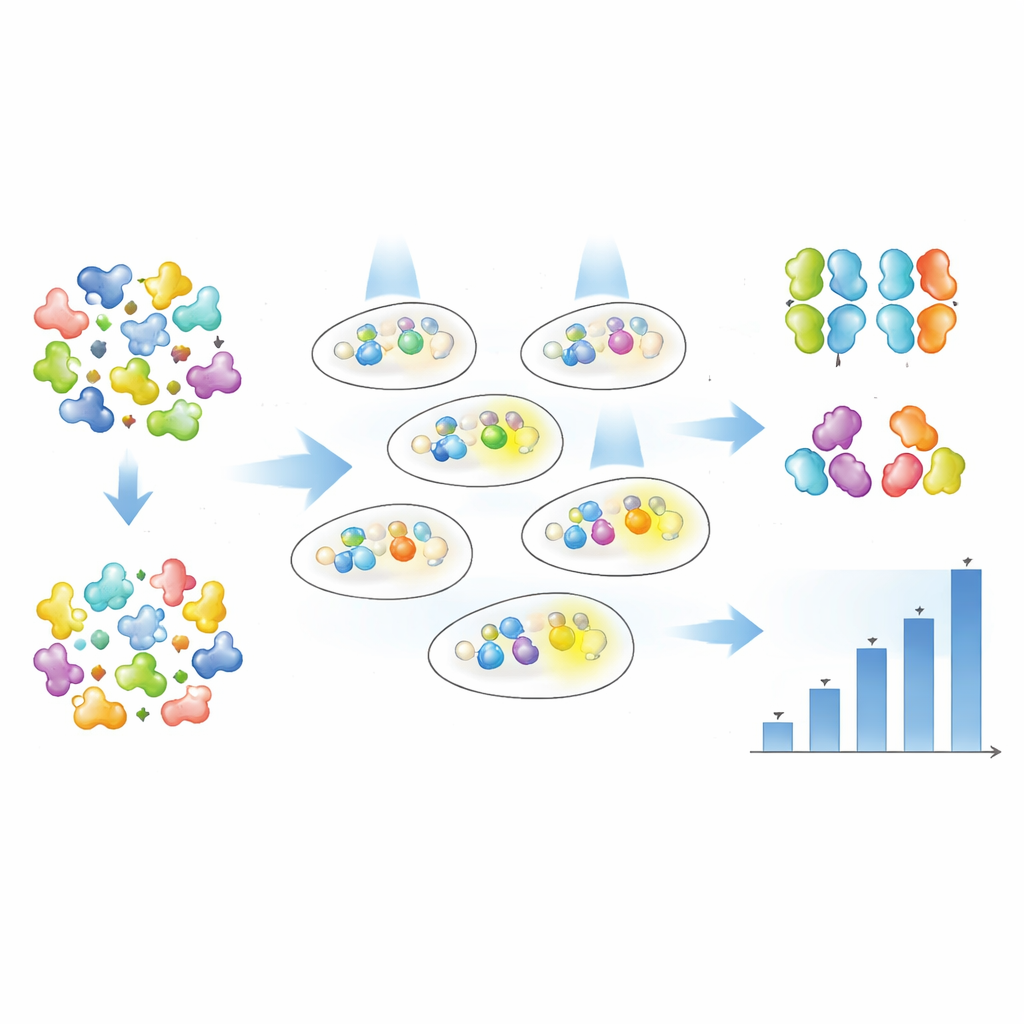
Ajuster finement la sensibilité et la puissance
Après une seule série de criblage, l’équipe a trouvé 19 variantes distinctes des Magnets présentant une riche palette de comportements. Certains mutants ont rendu le système beaucoup plus sensible à la lumière, ce qui signifie qu’un même niveau d’expression génique pouvait être atteint avec une intensité lumineuse bien plus faible. D’autres ont principalement augmenté l’intensité d’activation du gène à luminosité maximale, et certaines ont fait les deux. De manière importante, les auteurs montrent que « la quantité de lumière nécessaire » (sensibilité) et « l’importance de la réponse génique » (activation) peuvent être réglées en grande partie de manière indépendante. Pour certaines variantes, l’activation à mi‑puissance était atteinte avec environ la moitié de la lumière, alors que le rendement maximal restait similaire ; pour d’autres, le rendement maximal augmentait de plusieurs fois tandis que la sensibilité demeurait approximativement la même. En comparant de nombreuses variantes à différentes températures, ils ont aussi identifié des versions qui conservent une activité plus forte dans des conditions proches de la température corporelle et présentent un comportement robuste au cours de la croissance de la population cellulaire.
Nouveaux blocs de construction pour la biologie contrôlée par la lumière
Pour un non-spécialiste, le message principal est que ces chercheurs ont transformé un interrupteur lumineux unique en un véritable panneau de gradation. Au lieu d’un capteur bleu fixe, ils proposent désormais un menu de variantes Magnets qui requièrent plus ou moins de lumière, produisent des réponses géniques plus ou moins fortes, ou fonctionnent bien à différentes températures. Parce que les Magnets sont déjà largement utilisés en biologie synthétique et ont été adaptés aux cellules de mammifères, ces versions améliorées peuvent être intégrées dans de nombreux dispositifs existants. En termes pratiques, cela signifie que les expériences nécessitant un éclairage doux et prolongé peuvent utiliser des variantes très sensibles, tandis que les applications devant éviter une activation accidentelle par la lumière ambiante peuvent choisir des variantes moins sensibles. Ce travail élargit ainsi la boîte à outils pour sculpter précisément le comportement cellulaire à la lumière en recherche et biotechnologie.
Citation: Baumschlager, A., Weber, Y., Cánovas, D. et al. Enhancing the performance of Magnets photosensors. Nat Commun 17, 4138 (2026). https://doi.org/10.1038/s41467-026-70695-7
Mots-clés: optogénétique, expression génique contrôlée par la lumière, ingénierie des protéines, protéines photosensorielles, biologie synthétique