Clear Sky Science · nl
Verbeteren van de prestaties van Magnets-fotosensoren
Cellen vormgeven met bundels licht
Stel je voor dat je genen met een lichtbundel aan- en uit kunt zetten net zo eenvoudig als een schakelaar omzetten. Deze studie laat zien hoe wetenschappers een veelgebruikte familie lichtgevoelige eiwit"schakelaars", genaamd Magnets-fotosensoren, hebben verbeterd zodat ze preciezer en krachtiger op blauw licht reageren. Deze verbeterde schakelaars kunnen onderzoekers helpen het gedrag van cellen te regelen met minder licht, minder schade en meer flexibiliteit in zowel bacteriën als in zoogdiercellen.
Waarom licht een krachtig regelwiel is
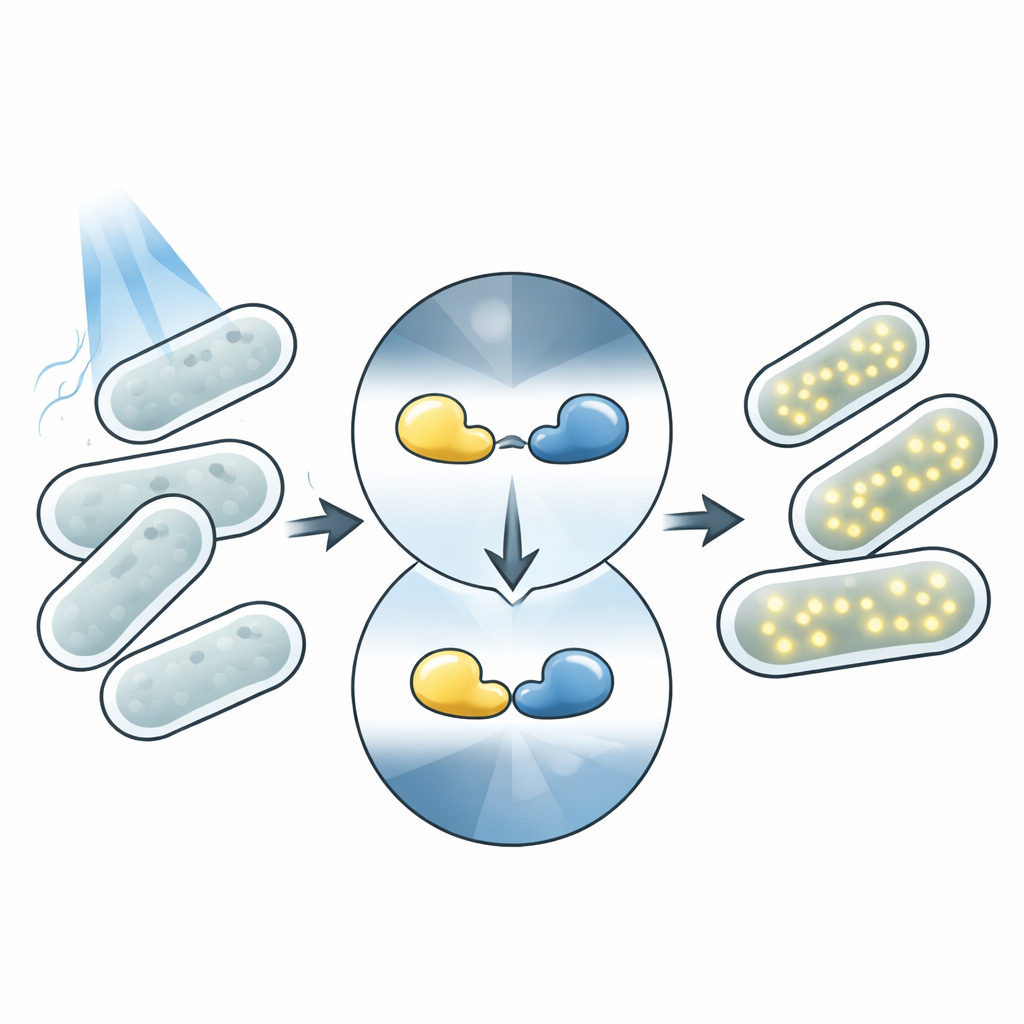
Licht is een ideaal afstandsbedieningsmiddel voor de biologie. In tegenstelling tot chemische toevoegingen kan licht direct worden aangezet, net zo snel worden verwijderd en worden gericht op zeer kleine gebieden zonder de cellen aan te raken. Veel organismen bevatten van nature eiwitten die van vorm veranderen wanneer ze licht absorberen, wat downstream-effecten activeert. Moderne optogenetica hergebruikt deze eiwitten als controleerbare onderdelen: een lichtgevoelige "kop" wordt gefuseerd aan een "actie"module zoals een enzym of gen-schakelaar. Wanneer er licht schijnt, verandert de sensor van vorm en activeert de gekoppelde functie. Magnets-fotosensoren zijn een paar van zulke eiwitten die bij blauw licht aan elkaar kleven en in het donker uit elkaar vallen, waardoor ze een werkpaard zijn voor het bouwen van lichtgestuurde systemen.
Hoe de Magnet-schakelaar in cellen werkt
In dit werk richt het team zich op een blauwlicht-gevoelig systeem genaamd Opto-T7RNAP. Hier is het Magnets-paar gefuseerd aan twee helften van een gesplitst enzym, T7 RNA-polymerase, dat de expressie van een targetgen aandrijft. In het donker blijven de helften gescheiden en is het gen grotendeels stil. Onder blauw licht binden de Magnet-domeinen aan elkaar, waardoor de enzymhelften worden samengebracht en het gen wordt aangezet en een rood fluorescerend eiwit produceert dat eenvoudig kan worden gemeten. Deze opzet koppelt de DNA-sequentie van elk lichtgevoelig eiwit nauw aan een zichtbare output, waardoor de onderzoekers de prestaties van duizenden varianten kunnen aflezen door simpelweg te meten hoe fel de cellen oplichten.
Willekeurige verandering en zorgvuldige selectie
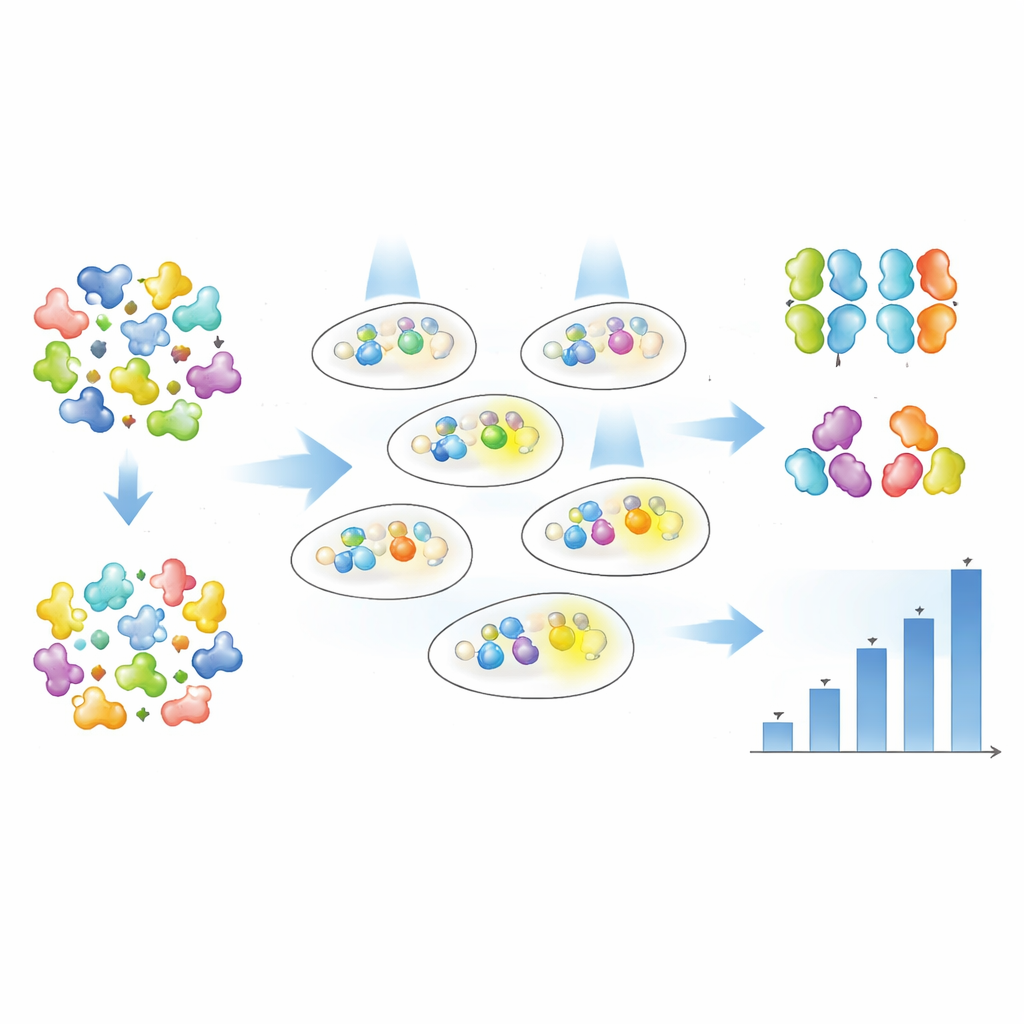
In plaats van te gokken welke enkele aminozuren aangepast moesten worden, gebruikten de auteurs willekeurige mutagenese om veranderingen door het hele Magnet-eiwit in te voeren en lieten ze vervolgens de data aantonen welke versies het beste werkten. Ze creëerden grote bibliotheken van gemuteerde nMag- en pMag-varianten en brachten die in bacteriën met het Opto-T7RNAP-systeem en het fluorescente rapportergen. Met behulp van fluorescentie-geactiveerde celsortering voerden ze een meerstapsselectie uit: eerst verrijkten ze cellen die sterk oplichtten bij zwak blauw licht, daarna verwijderden ze cellen die te veel oplichtten in het donker, en tenslotte isoleerden ze individuele klonen voor gedetailleerde tests. Het oplichtniveau van elke variant werd gevolgd ofwel cel-voor-cel met flowcytometrie of in bulkculturen in de tijd met geautomatiseerde spectrofotometrie.
Fijn afstemmen van gevoeligheid en sterkte
Al na één ronde van screening vond het team 19 verschillende Magnet-varianten met een rijke mix van gedragingen. Sommige mutanten maakten het systeem veel gevoeliger voor licht, wat betekent dat dezelfde genuitvoer bereikt kon worden met veel lagere lichtintensiteit. Andere verhoogden voornamelijk hoe sterk het gen werd aangezet bij volle belichting, en sommige deden beide. Belangrijk is dat de auteurs aantonen dat "hoeveel licht nodig is" (gevoeligheid) en "hoeveel genuitvoer je krijgt" (activatie) grotendeels onafhankelijk van elkaar kunnen worden afgesteld. In sommige varianten werd half-maximale activatie bereikt met ongeveer de helft van het licht, terwijl de maximale output vergelijkbaar bleef; bij andere nam de maximale output meerdere keren toe terwijl de gevoeligheid min of meer gelijk bleef. Door veel varianten bij verschillende temperaturen te vergelijken identificeerden ze ook versies die sterkere activiteit behouden bij lichaamstemperatuur en robuust gedrag vertonen gedurende de groei van de cellulaire populatie.
Nieuwe bouwstenen voor lichtgestuurde biologie
Voor een niet-specialist is de kernboodschap dat deze wetenschappers één enkele lichtschakelaar hebben omgevormd tot een volledig dimmerpaneel. In plaats van één vaste blauwlichtsensor bieden ze nu een assortiment Magnet-varianten die meer of minder licht vereisen, sterkere of mildere genreacties produceren, of goed presteren bij verschillende temperaturen. Omdat Magnets al veel gebruikt worden in de synthetische biologie en zijn aangepast aan zoogdiercellen, kunnen deze verbeterde versies in veel bestaande ontwerpen worden geïntegreerd. In praktische zin betekent dit dat experimenten die zachte, langdurige belichting nodig hebben zeer gevoelige varianten kunnen gebruiken, terwijl toepassingen die per ongeluk activeren door kamerlamplicht moeten vermijden, minder gevoelige varianten kunnen gebruiken. Het werk vergroot daarmee de gereedschapskist om cellulair gedrag nauwkeurig te vormen met licht in onderzoek en biotechnologie.
Bronvermelding: Baumschlager, A., Weber, Y., Cánovas, D. et al. Enhancing the performance of Magnets photosensors. Nat Commun 17, 4138 (2026). https://doi.org/10.1038/s41467-026-70695-7
Trefwoorden: optogenetica, lichtgestuurde genexpressie, proteïne-engineering, fotosensorische eiwitten, synthetische biologie