Clear Sky Science · es
Mejorando el rendimiento de los fotosensores Magnets
Moldeando células con haces de luz
Imagínese poder encender y apagar genes con un haz de luz tan fácilmente como accionar un interruptor. Este estudio muestra cómo los científicos han mejorado una familia popular de “interruptores” proteicos sensibles a la luz, llamados fotosensores Magnets, para que respondan con mayor precisión y potencia a la luz azul. Estos interruptores mejorados podrían ayudar a los investigadores a controlar el comportamiento celular con menos luz, menos daño y más flexibilidad, tanto en bacterias como en células de mamífero.
Por qué la luz es una perilla de control poderosa
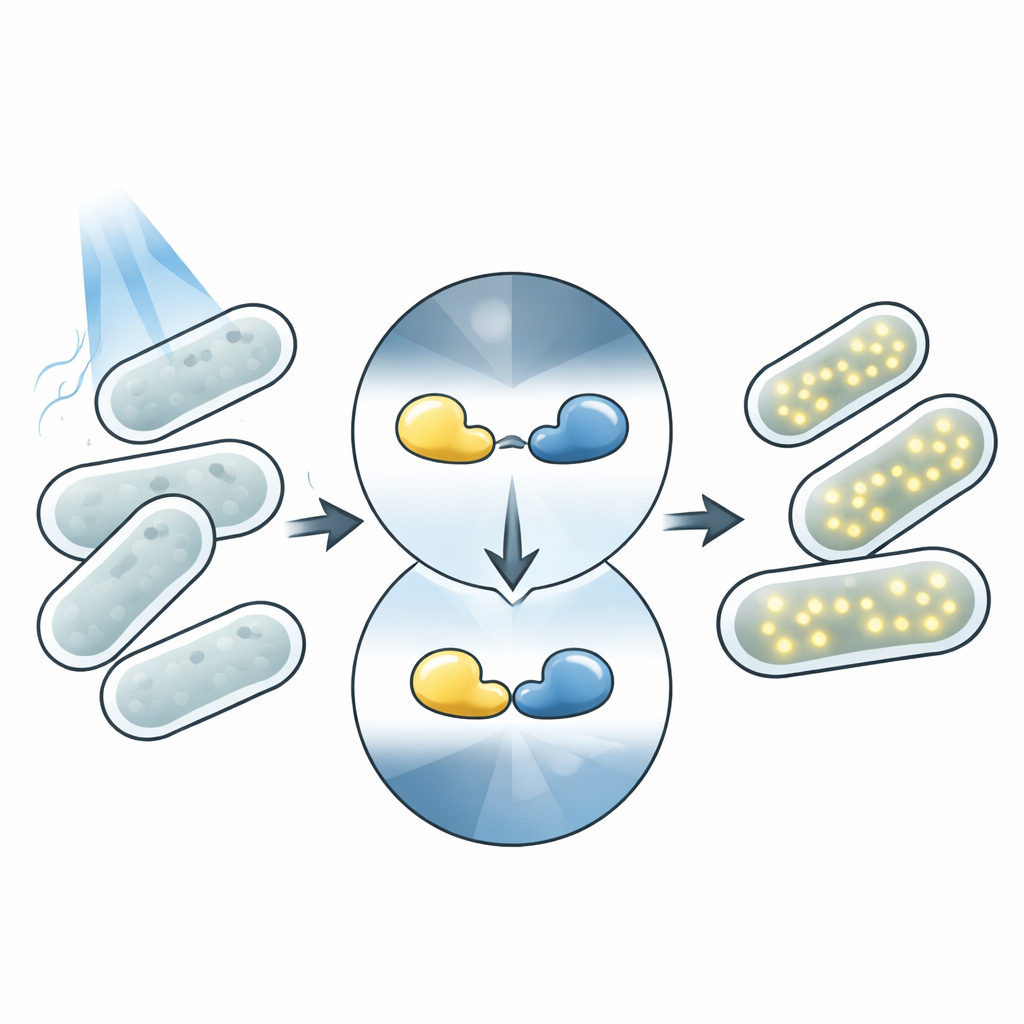
La luz es un control remoto ideal para la biología. A diferencia de los aditivos químicos, la luz puede aplicarse al instante, retirarse igual de rápido y concentrarse en regiones diminutas sin tocar las células. Muchos organismos contienen de forma natural proteínas que cambian de forma al absorber luz, desencadenando efectos a continuación. La optogenética moderna reutiliza estas proteínas como piezas controlables: una “cabeza” sensora de luz se fusiona con un módulo de acción, como una enzima o un interruptor génico. Cuando incide la luz, el sensor cambia de forma y activa la función unida. Los fotosensores Magnets son un par de tales proteínas que se unen bajo luz azul y se separan en la oscuridad, lo que las convierte en una herramienta de uso frecuente para construir sistemas controlados por luz.
Cómo funciona el interruptor Magnet en las células
En este trabajo, el equipo se centra en un sistema sensible a la luz azul llamado Opto-T7RNAP. Aquí, el par Magnets se fusiona a dos mitades de una enzima dividida, la ARN polimerasa T7, que impulsa la expresión de un gen diana. En la oscuridad, las mitades permanecen separadas y el gen está mayormente silencioso. Bajo luz azul, los dominios Magnets se unen entre sí, acercando las mitades de la enzima para que el gen se active y produzca una proteína fluorescente roja que puede medirse fácilmente. Esta configuración vincula estrechamente la secuencia de ADN de cada proteína sensora a una señal visible, lo que permite a los investigadores evaluar el rendimiento de miles de variantes simplemente midiendo la intensidad del brillo celular.
Cambio aleatorio y selección cuidadosa
En lugar de adivinar qué aminoácidos individuales modificar, los autores usaron mutagénesis al azar para introducir cambios a lo largo de cada proteína Magnet y luego dejaron que los datos revelaran qué versiones funcionaban mejor. Crearon grandes bibliotecas de variantes mutadas de nMag y pMag e introdujeron estas bibliotecas en bacterias que contenían el Opto-T7RNAP y el gen reportero fluorescente. Usando clasificación por citometría de flujo basada en fluorescencia, realizaron una selección en varios pasos: primero enriquecieron las células que brillaban intensamente bajo luz azul tenue, luego descartaron las que brillaban demasiado en la oscuridad y, finalmente, aislaron clones individuales para pruebas detalladas. El nivel de brillo de cada variante se siguió bien célula por célula mediante citometría, bien en cultivos masivos a lo largo del tiempo con espectrofotometría automatizada.
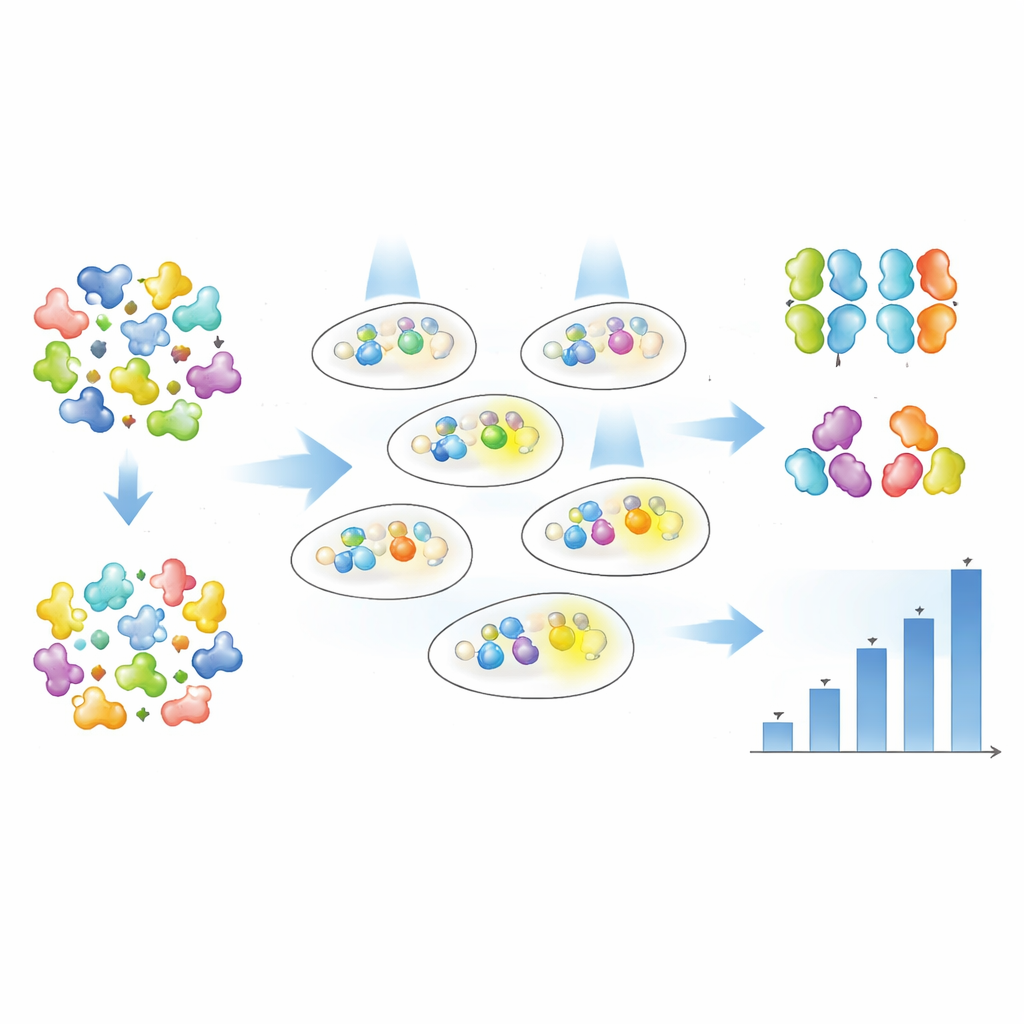
Ajuste fino de sensibilidad y potencia
Con solo una ronda de cribado, el equipo encontró 19 variantes distintas de Magnet con una rica variedad de comportamientos. Algunos mutantes hicieron el sistema mucho más sensible a la luz, lo que significa que la misma salida génica podía alcanzarse con una intensidad luminosa mucho menor. Otros aumentaron principalmente la fuerza con la que el gen se activaba con luz plena, y algunos hicieron ambas cosas. Es importante que los autores demostraron que “cuánta luz se necesita” (sensibilidad) y “cuánta salida génica se obtiene” (activación) pueden ajustarse en gran medida de forma independiente. En algunas variantes, la activación a la mitad del máximo se alcanzó con aproximadamente la mitad de la luz, mientras que la salida máxima permaneció similar; en otras, la salida máxima aumentó varias veces mientras la sensibilidad se mantuvo aproximadamente igual. Al comparar muchas variantes a distintas temperaturas, también identificaron versiones que conservan una actividad más fuerte en condiciones semejantes a las corporales y que muestran un comportamiento robusto durante el crecimiento de la población celular.
Nuevos bloques de construcción para la biología controlada por luz
Para un no especialista, el mensaje principal es que estos científicos han convertido un único interruptor de luz en todo un panel regulable. En lugar de un sensor fijo de luz azul, ahora ofrecen un menú de variantes Magnets que requieren más o menos luz, producen respuestas génicas más intensas o más suaves, o funcionan bien a distintas temperaturas. Dado que los Magnets ya se usan ampliamente en biología sintética y se han adaptado a células de mamífero, estas versiones mejoradas pueden integrarse en muchos diseños existentes. En términos prácticos, eso significa que experimentos que necesitan iluminación suave y prolongada pueden usar variantes muy sensibles, mientras que aplicaciones que deben evitar una activación accidental por la luz ambiental pueden optar por variantes menos sensibles. El trabajo amplía así la caja de herramientas para esculpir con precisión el comportamiento celular mediante luz en investigación y biotecnología.
Cita: Baumschlager, A., Weber, Y., Cánovas, D. et al. Enhancing the performance of Magnets photosensors. Nat Commun 17, 4138 (2026). https://doi.org/10.1038/s41467-026-70695-7
Palabras clave: optogenética, expresión génica controlada por luz, ingeniería de proteínas, proteínas fotosensibles, biología sintética